Атом водорода.
Простейшим атомом (А) явл. А водорода, состоящий из протона и Э, связанных гл. обр. электростатическим кулоновским взаимодействием. Качественно подобен А водорода водородоподобный ион, т.е. система, состоящая из ядра с зарядом Z и одного Э. Схема У.э. А водорода показана на рис. 1. Энергия уровней в нерелятивистском приближении дается выражением:
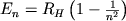 , (2)
, (2)
где 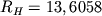 эВ - Ридберга постоянная для А водорода, величина n наз. главным квантовым числом и может принимать значения n =1, 2, 3,....,
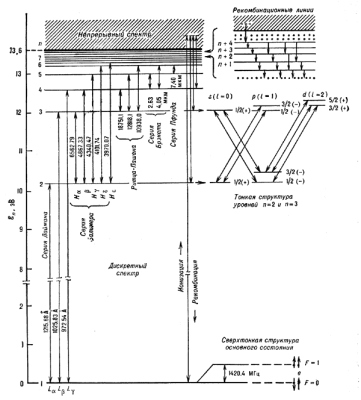
эВ - Ридберга постоянная для А водорода, величина n наз. главным квантовым числом и может принимать значения n =1, 2, 3,...., 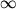 . У.э., соответствующие различным n, показаны в левой части рисунка; при увеличении n они сгущаются к границе ионизации 13,6 эВ. Переходы между У.э. с различными значениями n приводят к образованию спкетра, состоящего из отчетливо выраженных спектральных серий (для серий Брэкета и Пфунда длины волн на рис. даны в микрометрах, для остальных - в ангстремах). Наблюдение и излучение этих линий играет важную роль в исследовании атмосфер звезд. В результате существенного улучшения чувствительности астрономич. приемников ИК-излучения удалось наблюдать линии, принадлежащие сериям Брэкета и Пфунда, к-рые образуются в компактных зонах HII, окружающих очень молодые звезды.
. У.э., соответствующие различным n, показаны в левой части рисунка; при увеличении n они сгущаются к границе ионизации 13,6 эВ. Переходы между У.э. с различными значениями n приводят к образованию спкетра, состоящего из отчетливо выраженных спектральных серий (для серий Брэкета и Пфунда длины волн на рис. даны в микрометрах, для остальных - в ангстремах). Наблюдение и излучение этих линий играет важную роль в исследовании атмосфер звезд. В результате существенного улучшения чувствительности астрономич. приемников ИК-излучения удалось наблюдать линии, принадлежащие сериям Брэкета и Пфунда, к-рые образуются в компактных зонах HII, окружающих очень молодые звезды.
|
Рис. 1. Схема энергетических уровней атома водорода. Длины волн даны в 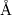 . Для серий Брэкета и Пфунда в мкм. . Для серий Брэкета и Пфунда в мкм.
|
На рис. 1 показаны также переходы между уровнями, лежащими в дискретном и непрерывном спектре: свободно-связанные переходы - рекомбинация и обратные связанно-свободные переходы - ионизация.
Рекомбинация атомов на У.э. с большмим значениями n и последующие каскадные переходы на нижележащие уровни приводят к образованию линий, получивших название рекомбинационных (см. Рекомбинационные радиолинии). Нек-рые из таких переходов показаны в верхней правой части рис. 1.
Электрон в А в общем случае обладает орбитальным МКД l, к-рый может принимать целочисленные значения в интервале 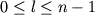 . В атомной спектроскопии принято обозначать состояния, соответствующие различным значениям l =0, 1, 2,..., буквами латинского алфавита s, p, d, f, g (и далее в порядке букв латинского алфавита). Например, состояние n =1, l =0 обозначается как 1s, состояние n =3, l =2 - 3d. Так, к У.э. n =1 относится одно состояние 1s, к У.э. n =2 - состояния 2s, 2p, к У.э. n =3 - состояния 3s, 3p, 3d, и т.д.
. В атомной спектроскопии принято обозначать состояния, соответствующие различным значениям l =0, 1, 2,..., буквами латинского алфавита s, p, d, f, g (и далее в порядке букв латинского алфавита). Например, состояние n =1, l =0 обозначается как 1s, состояние n =3, l =2 - 3d. Так, к У.э. n =1 относится одно состояние 1s, к У.э. n =2 - состояния 2s, 2p, к У.э. n =3 - состояния 3s, 3p, 3d, и т.д.
Согласно (2), в нерелятивистском приближении энергия уровня с квантовым числом n не зависит от l и ml (ml - проекция орбитального МКД на к.-л. ось). Т.о., в этом приближении уровень n оказывается вырожденным. Кратность этого вырождения есть n 2. Независимость энергии от ml легко объясняется тем, что в поле, обладающим сферич. симметрией (таково кулоновское поле ядра), все направления в пространстве равноправны, и поэтому энергия не может зависеть от ориентации МКД в пространстве. Что касается независимости энергии от l, то она связана только со спецификой кулоновского взаимодействия между ядром и Э. Вырождение по l снимается, когда при расчете энергии атомного У.э. учитываются такие релятивистские поправки, как зависимость массы Э от скорости (см. Релятивистские частицы) и спин-орбитальное взаимодействие, т.е. взаимодействие, зависящее от величин и взаимной ориентации орбитального и спинового МКД Э. Учет этих поправок дает следующую ф-лу для энергии уровня:
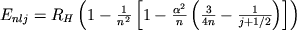 , (3)
, (3)
где 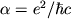 =1/137 - постоянная тонкой структуры, j - полный МКД, слагающийся из орбитального и спинового МКД. Согласно правилам сложения МКД, j может принимать два значения:
=1/137 - постоянная тонкой структуры, j - полный МКД, слагающийся из орбитального и спинового МКД. Согласно правилам сложения МКД, j может принимать два значения: 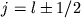 . Т.о., каждое состояние с
. Т.о., каждое состояние с 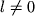 расщепляется на два уровня с различными энергиями. Эти расщепления много меньше, чем расстояния между У.э. с различными значениями n, и наз. тонкими расщеплениями (тонкая структура). Тонкая структура У.э. с n =2 и n =3 в А водорода показана на рис. 1. Справа от каждого У.э. указаны значения j и четность уровня, а стрелками показаны переходы, ответственные за линию H
расщепляется на два уровня с различными энергиями. Эти расщепления много меньше, чем расстояния между У.э. с различными значениями n, и наз. тонкими расщеплениями (тонкая структура). Тонкая структура У.э. с n =2 и n =3 в А водорода показана на рис. 1. Справа от каждого У.э. указаны значения j и четность уровня, а стрелками показаны переходы, ответственные за линию H  (самая длинноволновая линия в серии Бальмера). Аналогичная структура имеется у всех уровней n >0, l >0. Величина тонкого расщепления убывает с ростом n как 1/n 3. Поэтому оно особенно важно для нижних состояний.
(самая длинноволновая линия в серии Бальмера). Аналогичная структура имеется у всех уровней n >0, l >0. Величина тонкого расщепления убывает с ростом n как 1/n 3. Поэтому оно особенно важно для нижних состояний.
Расщепление еще меньшей величины (сверхтонкое расщепление) обязано взаимодействию магн. моментов ядра и Э. Это расщепление показано на рис. 1 для осн. состояния А водорода. Магн. моменты Э и ядра (в данном случае протона) пропорциональны их спинам. Поскольку спин протона I =1/2, то полный МКД А в осн. состоянии (при учете ядерного спина он обычно обозначается буквой F) может принимать два значения: F =1 (спины e и p параллельны) и F =0 (спины e и p антипараллельны). Энергии этих сверхтонких подуровней различны, а переходы между ними приводят к образованию радиолинии водорода 21 см.
Многоэлектронные атомы.
В многоэлектронных атомах помимо кулоновского взаимодействия каждого Э с ядром имеются также взаимодействия Э друг с другом и обменное взаимодействие, связанное с неразличимостью Э при их квантовомеханическом описании. Движение каждого из Э можно рассматривать происходящим в нек-ром усредненном поле, создаваемом ядром и всеми др. Э. Для приближенного описания можно использовать квантовые числа n и l, однако в данном случае вырождение по l отсутствует даже в нерелятивистском приближении. Тем не менее каждый У.э. с данными n и l еще остается вырожденным по проекции орбитального и спинового МКД. Кратность этого вырождения равна (2 s +1)(2 l +1)=2(2 l +1), т.к. для электрона s =1/2. Согласно принципу Паули, в каждом из этих состояний может находится только по одному Э. Поэтому максимально возможное число состояний в А с данными n и l равно 2(2 l +1) и эти состояния, называемые эквивалентными, образуют электронную оболочку. Электронная оболочка наз. замкнутой, если все возможные состояния в ней заполнены. Совокупность 2 n 2 состояний с одним и тем же n, но разными l наз. электронным слоем (напр., K-слой, содержащий 2 Э при n =1, L-слой, содержащий 8 Э при n =2, M-слой, содержащий 18 Э при n =3). закономерностями в последовательном заполнении электронных оболочек объясняется периодичность изменения св-в элементов. Последовательность, в к-рой возрастают энергии Э с заданными n и l, следующая: 1 s, 2 s, 2 p, 3 s, 3 p, 3 d,... и т.д. (здесь буквы лат. алфавита, как и ранее, относятся к значениям орбитального МКД l =0, 1, 2,...). Совокупность всех атомных Э, находящихся в определенных энергетич. состояниях, наз. электронной конфигурацией А. Для ее описания указывают, каким образом при возрастании n Э рапределяются по оболочкам. Для этого перечисляют все электронные оболочки, в к-рых есть Э, а именно: указывают главное квантовое число n, лат. буквуЮ соответствующую значению орбитального МКД l, и (сверху справа от этой буквы) число Э в данной оболочке. Напр., конфигурация 1 s 2 2 s 2 2 p 2 осн. состояния А углерода означает, что в первом электронном слое находится два s -электрона, во втором слое находится два Э в s -оболочке и два Э в p -оболочке.
Электронная конфигурация определяет энергию А лишь приближенно. Для дальнейшего уточнения этой величины необходимо знать, какой тип связи МКД Э реализуется в А. Опыт показывает, что в легких А, где релятивистские эффекты сравнительно малы, реализуется т.н. LS -тип связи (часто ее называют также нормальной или связью Рассела-Саундерса). В этом случае все орбитальные МКД Э складываются в орбитальный МКД L, а все электронные спины суммируются в момент S. Моменты L и S складываются в полный МКД электронной оболочки J. В тяжелых А, где релятивистские эффекты существенны (спин-орбитальное и спин-спиновое взаимодействия), реализуется т.н. jj -связь, а именно: орбитальный j и спиновой s МКД каждого Э складываются в полный МКД электронной оболочки А J. Следует отметить, что, вообще говоря, чистых типов связи в реальных А не бывает и указанные типы - это предельные случаи, с хорошей точностью реализуемые для легких (LS) и тяжелых (jj) А. В астрофизич. приложениях наибольший интерес представляет рассмотрение У.э. в А с LS -связью моментов в электронных оболочках. Поэтому она описана здесь более подробно (о jj -связи см. раздел 4 и лит. при статье).
|
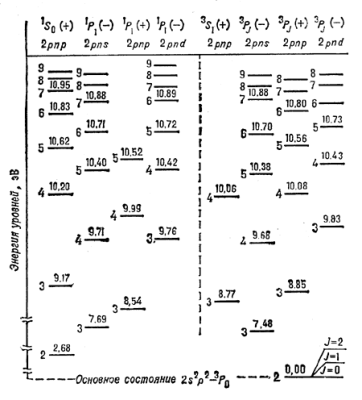
| Рис. 2. Участок энергетического спектра атома углерода. Числа, стоящие над чертой, к-рая обозначает уровень, дают его энергию в эВ. Главные квантовые числа n указаны слева от обозначения уровней. |
Если в электронной оболочке А реализуется LS -связь, то У.э., соответствующий данной электронной конфигурации, расщепляется на целый ряд уровней, характеризуемых значениями L и S, наз. спектральными термами. Для обозначения термов обычно используются заглавные буквы лат. алфавита. Значения L =0, 1, 2,... соответствуют термы S, P, D, F, G и т.д. Вместо значения спина S указывают мультиплетность терма, равную 2 S +1, к-рая ставится слева вверху у знака терма. Если мультиплетность равна 1, терм наз. синглетным, 2 - дублетным, 3 - триплетным и т.д. Эмпирически установленоЮ что наименьшей энергией обладает терм с наибольшим возможным для данной электронной конфигурации значением S и наибольшим (возможным при этом S) значением L (правило Хунда). Релятивистские эффекты, и прежде всего спин-орюитальное взаимодействие, приводят к расщеплению терма с данными L и S на ряд уровней, соответствующих различным возможным значениям J полного МКД (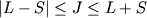 ). Это расщепление наз. тонким или мультиплетным. Для характеристики состояния при наличии тонкой структуры наряду с электронной конфигурацией, термом и мультиплетностью указывают также значение полного МКД J, к-рое ставится справа внизу у обозначения терма. Напр., осн. состояние А углерода есть 1 s 2 2 s 2 2 p 2 - 3 P 0, т.е. электронная конфигурация осн. состояния А углерода есть 1 s 2 2 s 2 2 p 2, полный орбитальный МКД L =1, полный спиновый МКД S =1, полный МКД электронной оболочки J =0. На рис. 2 приведен участок энергетич. спектра А углерода. В верхней части рис. термы, мультиплетности, значения полных моментов J, четности и электронные конфигурации. Все уровни разбиваются на две группы с различными мультиплетностями: синглеты (S =0) и триплеты (S =1). Радиац. переходы между этими двумя группами уровней (интеркомбинационные переходы) явл. запрещенными. Для терма 3 P 0 показана тонкая структура.
). Это расщепление наз. тонким или мультиплетным. Для характеристики состояния при наличии тонкой структуры наряду с электронной конфигурацией, термом и мультиплетностью указывают также значение полного МКД J, к-рое ставится справа внизу у обозначения терма. Напр., осн. состояние А углерода есть 1 s 2 2 s 2 2 p 2 - 3 P 0, т.е. электронная конфигурация осн. состояния А углерода есть 1 s 2 2 s 2 2 p 2, полный орбитальный МКД L =1, полный спиновый МКД S =1, полный МКД электронной оболочки J =0. На рис. 2 приведен участок энергетич. спектра А углерода. В верхней части рис. термы, мультиплетности, значения полных моментов J, четности и электронные конфигурации. Все уровни разбиваются на две группы с различными мультиплетностями: синглеты (S =0) и триплеты (S =1). Радиац. переходы между этими двумя группами уровней (интеркомбинационные переходы) явл. запрещенными. Для терма 3 P 0 показана тонкая структура.
В межзвездной среде наблюдается большое количество УФ- и оптич. линий, соответстсвующих различным переходам в многоэлектронных А и ионах. Ряд переходов из возбужденных состояний в нижние электронные слои (K-, L- слои) в тяжелых А приводит к излучению в рентг. области спектра.
Наличие тонкой структуры у многих А играет большую роль в астрофизич. явлениях. Напр., в А углерода и кислорода уровни тонкой структуры легко возбуждаются при столкновениях этих А с др. частицами в облаках межзвездного газа. Излучательная деактивация уровней тонкой структуры, сопровождающаяся излучением фотонов, способствует выводу тепловой энергии из газово-пылевых облаков. Этот процесс может оказаться особенно важным на начальном этапе звездообразования при уплотнении газовых конденсаций, в к-рых начинается гравитац. сжатие протозвезд. Переходы между уровнями тонкой структцры А и ионов кислорода, углерода, серы, аргона, неона и др. наблюдаются в межзвездной среде в ИК-диапазоне.
Как и в А водорода, в многоэлектронных А имеются сверхтонкие расщепления У.э. Переходы между уровнями сверхтонкой структуры попадают в радиодиапазон. Напр., длина волны такого перехода в А азота равна 11,5 м. Предпринимаются поиски этой линии в межзвездной среде.
Рекомбинация многоэлектронных А на У.э. с большими значениями n и последующие излучательные переходы между этими уровнями приводят к образованию рекомбинац. линий. Из-за того что массы ядер сложных А больше, чем масса ядра А водорода, рекомбинац. линии этих А слегка сдвинуты относительно соответстсвующих водородных линий в коротковолновую область спектра.
 2015-05-06
2015-05-06 1724
1724








