1. Реальный газ – это газ: б) свойства которого зависят от взаимодействия частиц и их собственного объема; в) свойства которого зависят от взаимодействия частиц и их собственного объема, что особенно проявляется при высоких давлениях и низких температурах;
2. Уравнение состояния реальных газов (уравнение Ван-дер-Ваальса) для произвольной массы газа имеет вид:
б) 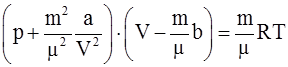 ;
;
3. С учётом только поправки на собственный объем молекул 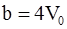 , где
, где 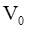 – суммарный собственный объем молекул газа, уравнение состояния реального газа можно записать так (для моля или киломоля):
– суммарный собственный объем молекул газа, уравнение состояния реального газа можно записать так (для моля или киломоля):
а) 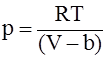 ; б)
; б) 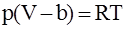 ;
;
4. С учётом поправки на дополнительное (внутреннее) давление, возникающее за счёт межмолекулярного взаимодействия (поправки 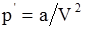 ), уравнение состояния реального газа можно записать так (для моля или киломоля): в)
), уравнение состояния реального газа можно записать так (для моля или киломоля): в) 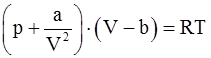 ;
;
5. Внутренняя энергия реального газа представляет собой сумму: в) сумму кинетических энергий поступательного и вращательного движения молекул газа Wk и потенциальной энергии их взаимодействия Wp.
6. Потенциальная энергия взаимодействия одного моля молекул реального газа: б) отрицательна;
7. Молекулярные силы, создающие внутреннее давление p', являются силами: б) притяжения;
8. Изменение потенциальной энергии реального газа (для моля) равно: в) работе, которую совершает моль газа, обладающий внутренним давлением p' при расширении от объёма V1 до V2.
9. Изменение потенциальной энергии реального газа (для моля) определяется соотношением:
а) 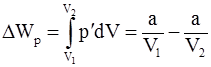 ; б)
; б) 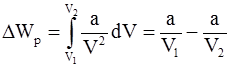 ; в)
; в) 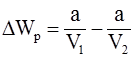 ;
;
10. В некотором приближении кинетическую энергию молекул одного моля реального газа, согласно теореме о равном распределении энергии по степеням свободы, можно определить по формуле: б) 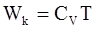 ;
;
11. Внутренняя энергия одного моля реального газа определяется соотношением: а) 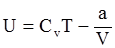 ;
;
12. Изменение температуры реального газа при адиабатическом расширении определяется соотношением:
б) 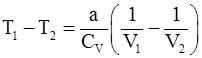 ;
;
13. При адиабатическом расширении реального газа его температура: б) убывает;
14. При адиабатическом сжатии реального газа его температура: а) возрастает;
15. Эффект Джоуля-Томсона – это изменение температуры реального газа при расширении через пористую перегородку. При этом, если газ при расширении охлаждается, эффект Джоуля-Томсона называется: б) положительным;
16. Эффект Джоуля-Томсона – это изменение температуры реального газа при расширении через пористую перегородку. При этом, если газ при расширении нагревается, эффект Джоуля-Томсона называется: а) отрицательным;
17. Фаза в термодинамике – это: б) равновесное состояние вещества, отличающееся по физическим свойствам от других возможных равновесных состояний того же вещества;
18. Фазовые превращения – переход вещества из одной фазы в другую: в) связанный с качественными изменениями свойств вещества при изменении внешних условий.
19. Фазовое равновесие – это: а) одновременное существование термодинамически равновесных фаз в многофазной системе;
20. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Точка О соответствует равновесию:
| в) трёх фаз – твёрдой, жидкой и газообразной; | 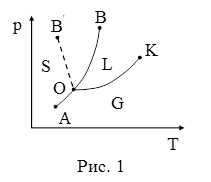
|
21. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Точка К соответствует равновесию:
| г) жидкой и газообразной фаз. | 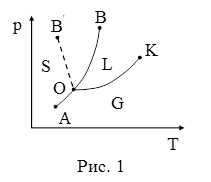
|
22. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Точка В соответствует равновесию:
| в) твёрдой и жидкой фаз веществ, у которых температура плавления растёт с увеличением давления; | 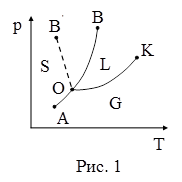
|
23. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Точка В' соответствует равновесию:
| г) твёрдой и жидкой фаз веществ, у которых температура плавления уменьшается с увеличением давления. | 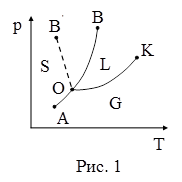
|
24. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Каждая точка кривой ОА соответствует равновесию:
| а) твердой и газообразной фаз вещества; | 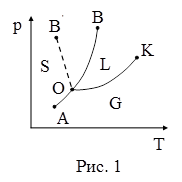
|
25. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Каждая точка кривой ОК соответствует равновесию:
| г) жидкой и газообразной фаз вещества. | 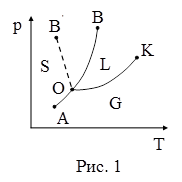
|
26. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Каждая точка кривой ОВ соответствует равновесию:
| б) твёрдой и жидкой фаз веществ, у которых температура плавления растёт с увеличением давления; | 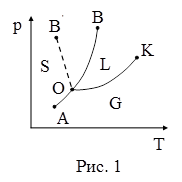
|
27. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Любая точка диаграммы состояния изображает равновесное состояние вещества при данных значениях давления и температуры. Каждая точка кривой ОВ' соответствует равновесию:
| а) твёрдой и жидкой фаз веществ, у которых температура плавления уменьшается с увеличением давления; | 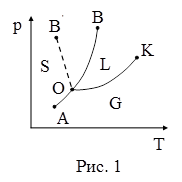
|
28. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Кривые, характеризующие равновесное состояние вещества при данных значениях температуры и давления, делят плоскость диаграммы состояния на области существования каждой из трёх фаз. Область S – это область существования:
| а) твёрдой фазы вещества; | 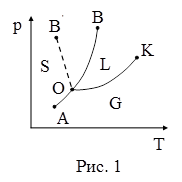
|
29. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Кривые, характеризующие равновесное состояние вещества при данных значениях температуры и давления, делят плоскость диаграммы состояния на области существования каждой из трёх фаз. Область L – это область существования:
| б) жидкой фазы вещества; . | 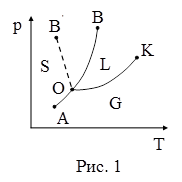
|
30. Диаграмма состояния (диаграмма равновесия, фазовая диаграмма) – геометрическое изображение равновесных состояний термодинамической системы при разных параметрах состояния, определяющих эти состояния, – даёт информацию о фазовом составе системы в зависимости от параметров состояния. На рисунке 1 представлена одна из возможных диаграмм состояния. Кривые, характеризующие равновесное состояние вещества при данных значениях температуры и давления, делят плоскость диаграммы состояния на области существования каждой из трёх фаз. Область G – это область существования:
| в) газообразной фазы вещества; | 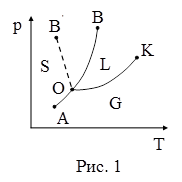
|
31. Правило фаз Гиббса: «В веществе, состоящем из n компонентов, одновременно может существовать не более чем:
б) (n + 2) равновесных фаз»;
32. Уравнение Клапейрона-Клаузиуса 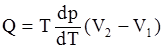 определяет изменение температуры фазового перехода при: в) бесконечно малом изменении давления.
определяет изменение температуры фазового перехода при: в) бесконечно малом изменении давления.
33. Уравнение Клапейрона-Клаузиуса 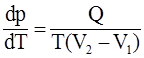 определяет изменение температуры фазового перехода при: в) бесконечно малом изменении давления.
определяет изменение температуры фазового перехода при: в) бесконечно малом изменении давления.
34. Уравнение Клапейрона-Клаузиуса 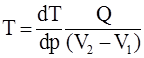 определяет изменение температуры фазового перехода при: в) бесконечно малом изменении давления.
определяет изменение температуры фазового перехода при: в) бесконечно малом изменении давления.
35. Метастабильное состояние – это состояние неустойчивого равновесия физической макроскопической системы (фазы). Не переходя в более устойчивое (при данных условиях) состояние (фазу), в таком состоянии система: б) может находиться длительное время;
36. Критическая точка – точка на диаграмме состояния, соответствующая критическому состоянию вещества. Состояние вещества в критической точке характеризуется критическими значениями: а) температуры Tk, давления pk и объема Vk;
37. Критическая точка в случае двухфазного равновесия – это точка окончания: а) кривой равновесия фаз; б) поверхности равновесия фаз; в) кривой или поверхности равновесия фаз.
38. Фазовый переход первого рода характеризуется тем, что при его осуществлении: а) поглощается или выделяется определенное количество теплоты, которое называют теплотой фазового перехода; б) поглощается определенное количество теплоты, которое называют теплотой фазового перехода; в) выделяется определенное количество теплоты, которое называют теплотой фазового перехода.
39. Фазовый переход первого рода характеризуется тем, что при его осуществлении значение таких термодинамических величин вещества, как плотность, концентрация компонентов, изменяется: б) скачком;
40. Фазовый переход второго рода – это такой переход, при котором некоторая физическая величина, равная нулю с одной стороны от точки перехода, постепенно при удалении от точки перехода в другую сторону: а) растет;
41. Фазовый переход второго рода – это такой переход, при котором плотность вещества: в) изменяется непрерывно.
42. Фазовый переход второго рода – это такой переход, при котором: а) не происходит выделения тепла; б) не происходит поглощения тепла; б)…. в) не происходит поглощения или выделения тепла.
 2015-05-06
2015-05-06 1060
1060
