1. Гетерополярная (электровалентная) связь или ионное взаимодействие
Характерна для соединений, в которых происходит полная отдача электрона одним атомом и приобретение его другим. При этом атомы превращаются в ионы с завершенными оболочками
Примеры гетерополярной связи в органической химии:
 О
СН3 - С
О-К+
ацетат калия О
СН3 - С
О-К+
ацетат калия
| СН3 – О-Nа+ метилат натрия |
 НС С-Na+
ацетиленид натрия НС С-Na+
ацетиленид натрия
|
2. Гомеополярная (ковалентная) атомная связь
Образуется путем обобществления электронов. При этом химическая связь возникает за счет электронной пары, принадлежащей одновременно двум атомам
Различают два механизма образования ковалентной связи:
а. Коллигация (обменный механизм)
Каждый из атомов предоставляет по одному электрону в общее пользование.

 Н3С× + × СН3 Н3С× СН3 СН3
Н3С× + × СН3 Н3С× СН3 СН3
б. Координация (донорно-акцепторный механизм)
Один из атомов (донор) предоставляет в общее пользование электронную пару, а другой (акцептор) имеет в своей оболочке вакантную орбиталь.
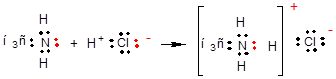
Взаимодействие метиламина с хлороводородом приводит к механизму координации
Метиламин – донор
Протон – акцептор
В хлориде метиламмония все N-H связи равны, отличие только в механизме образования.
 2015-05-06
2015-05-06 1627
1627








