Для изображения строения моносахаридов используют проекционные формулы Фишера. В формулах Фишера цепь углеродных атомов располагается в одну линию. Нумерация цепи начинается с атома углерода альдегидной группы (в случае альдоз) или с крайнего атома углерода, к которому ближе располагается кетогруппа (в случае кетоз). Атомы водорода и группы –ОН у асимметрических атомов «С» располагаются слева и справа от углеродной цепи.
В зависимости от пространственного расположения атомов «Н» и ОН-групп у 4-го атома углерода у пентоз и 5-го атома углерода у гексоз моносахариды относят к D- или L-ряду.
Моносахарид относят к D-ряду, если ОН-группа у этих атомов располагается справа от цепи:
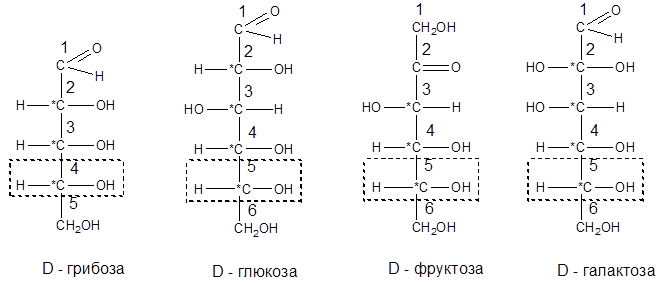
Рассмотренные выше структуры моносахаридов являются ациклическими. Однако моносахариды могут существовать также в циклических формах. Циклические формы образуются в результате взаимодействия карбонильной группы и одной из гидроксильных групп с образованием внутренних полуацеталей.
Альдегидная или кетонная группа гексоз и пентоз взаимодействует с гидроксильными группами у С-4 или С-5. В результате образуются пяти- или шестичленные циклы. Эти циклы структурно аналогичны кислородосодержащим гетероциклам пирану и фурану:

Поэтому циклические формы гексоз и пентоз соответственно называются пиранозными и фуранозными.
| Полуацетальный (гликозидный) гидроксил | |


| D-глюкопираноза Циклическая форма | |
| D-глюкоза Ациклическая (альдегидная) форма | |
В растворах моносахаридов происходит миграция протона между гидроксо- и карбонильной группой, при этом устанавливается подвижное равновесие между ациклической и циклической формами.
Подвижное равновесие между взаимопревращающимися структурными изомерами (таутомерами) называется таутомерией.
Циклические формы принято изображать перспективными формулами Хеуо́рса.
Для перехода от формул Фишера к формулам Хеуорса нужно знать следующие правила:
1. Изображаем цикл в виде плоского многоугольника (при этом цикл находится в плоскости, перпендикулярной плоскости изображения). Нумерацию атомов углерода в цикле производим по часовой стрелке. (Символы атомов углерода обычно не записываются).
2. Атомы и группы атомов, которые в формуле Фишера находятся справа от цепи, в формуле Хеуорса располагаются под плоскостью цикла, и наоборот. Исключение составляет группа -СН2ОН у 5-го атома углерода в гексозах, которая в случае D-гексоз всегда располагается над плоскостью цикла.
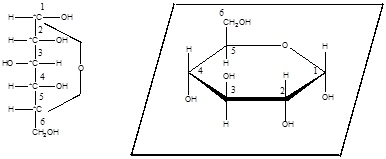

В циклических формах моносахаридов появляется еще один асимметрический атом углерода (С-1 у альдоз и С-2 у кетоз). Этот асимметрический атом углерода называется аномерным. Изомеры углеводов, отличающиеся расположением атомов и атомных групп у аномерного атома углерода, называются аномерами. Стереоизомер (пространственный изомер), в котором группа –ОН у аномерного атома «С» располагается под плоскостью цикла, называется α-аномером, а стереоизомер с противоположным расположением ОН-группы называется β-аномером:
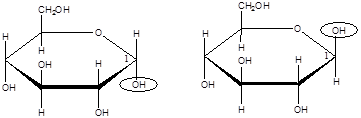
Аномеры не могут непосредственно превращаться друг в друга. Переход от одного аномера к другому возможен только через промежуточное образование ациклической формы моносахарида.
Таким образом, в растворе глюкозы присутствуют различные таутомерные формы, находящиеся в динамическом равновесии:
| Глюкоза (альдегидная форма) | |
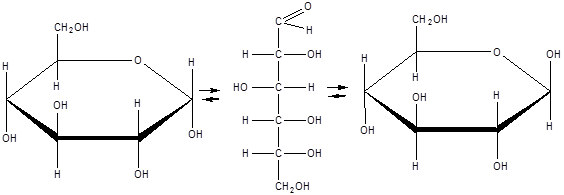
| β-глюкопираноза (β-глюкоза) | |
| α-глюкопираноза (α-глюкоза) | |
 Важнейшей кетогексозой является D-фруктоза (изомер D-глюкозы). Для циклических форм фруктозы характерны фуранозные структуры. Фуранозный цикл образуется в результате взаимодействия карбонильной (кетонной) группы со спиртовой группой при 5-м углеродном атоме.
Важнейшей кетогексозой является D-фруктоза (изомер D-глюкозы). Для циклических форм фруктозы характерны фуранозные структуры. Фуранозный цикл образуется в результате взаимодействия карбонильной (кетонной) группы со спиртовой группой при 5-м углеродном атоме.

Среди пентоз наиболее известны D-рибоза, у которой нет гидроксильной группы при втором углеродном атоме. Эти моносахариды входят в состав рибо- и дезоксирибонуклеиновых кислот (РНК и ДНК) в фуранозной форме.
| D-Рибоза (альдегидная форма) | |
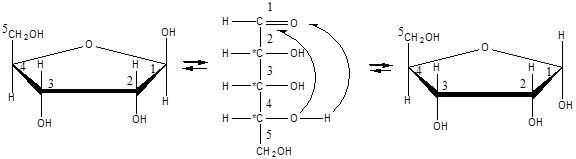
| 2-Дезокси-α-D-рибофураноза | |
| 2-Дезокси-D-рибоза (альдегидная форма) | |
| 2-Дезокси-β-D-рибофураноза | |
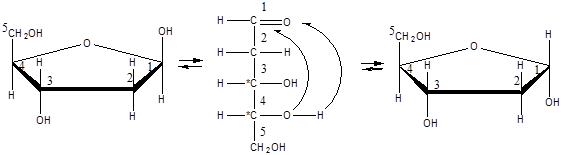
Физические свойства
Моносахариды представляют собой бесцветные кристаллические вещества, сладкие на вкус, хорошо растворимые в воде, нерастворимые в эфире, плохо растворимые в спирте. Сладость моносахаридов различна. Например, фруктоза слаще глюкозы в три раза.
Химические свойства
Моносахариды – это соединения со смешанными функциями.
В растворах существует динамическое равновесие между несколькими таутомерными формами моносахаридов, поэтому в зависимости от условий и реагентов они могут реагировать в открытой или циклической форме. При этом равновесие смещается в сторону образования той формы, которая вступает во взаимодействие.
Химические свойства моносахаридов обусловлены наличием:
а) карбонильной группы в открытых формах моносахаридов;
б)спиртовых гидроксильных групп как в открытых, так и в циклических формах моносахаридов;
в) полуацетальной гидроксильной группы в циклических формах моносахаридов.
Рассмотрим химические свойства моносахаридов на примере важнейшего из них – глюкозы.
I. Реакции с участием альдегидной группы глюкозы, т.е. свойства глюкозы как альдегида.
1. Восстановление (гидрирование) с образованием многоатомного спирта:
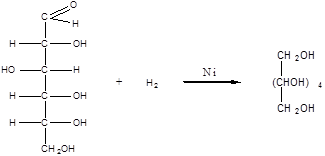
О
В ходе этой реакции карбонильная группа –С– восстанавливается и образуется новая спиртовая группа – ОН.
2. Окисление
Глюкоза легко окисляется. В зависимости от характера окислителей получаются различные продукты.
1) Окисление под действием слабых (мягких) окислителей с образованием глюконовой кислоты.
К числу таких реакций относятся качественные реакции на глюкозу как альдегид: реакции с аммиачным раствором оксида серебра (I) Ag2O (реакция «серебряного зеркала») и реакция с гидроксидом меди (II) Cu(OH)2 в щелочной среде при нагревании:
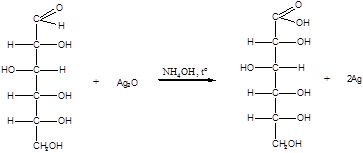
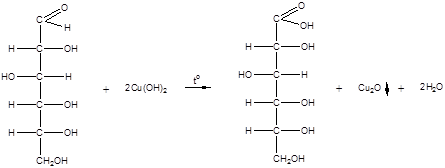
В ходе этих реакций альдегидная группа 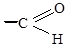 окисляется до карбоксильной группы
окисляется до карбоксильной группы 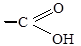 .
.
2) Окисление под действием сильных окислителей (например, азотной кислоты HNO3) c образованием двухосновной глюкаровой кислоты:
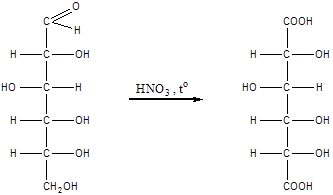
В ходе этой реакции и альдегидная группа 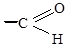 и первичная спиртовая группа – CH2OH окисляется до карбоксильных групп
и первичная спиртовая группа – CH2OH окисляется до карбоксильных групп 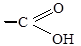 .
.
II. Реакции глюкозы с участием гидроксильных групп (т.е. свойства глюкозы как многоатомного спирта).
1. Взаимодействие с Cu(OH)2 на холоду с образованием глюконата меди (II) (качественная реакция на глюкозу как многоатомный спирт):
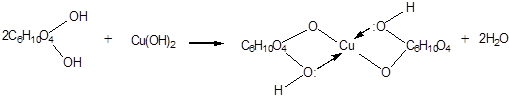
| Глюконат меди (II) (темно-синий раствор) | |
2. Взаимодействие с ангидридами или галогенангидридами кислот с образованием сложных эфиров:
| Пентаацетил- α-глюкоза (пентаацетат- α-глюкозы) | |
(Ас - ацетил - 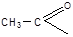 ) ) | |
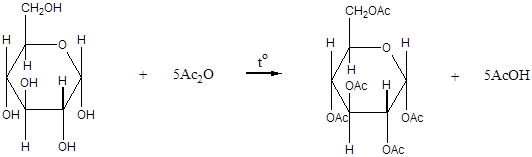
3. Взаимодействие с галогеналканами с образованием простых эфиров:
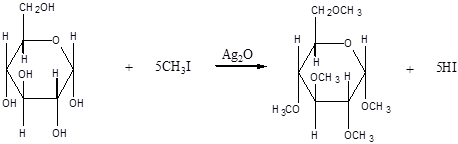
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции HI.
4. Взаимодействие со спиртами с образованием гликозидов.
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения. В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.

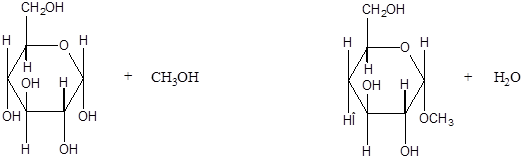
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы связаны остатки самых различных соединений.
III. Брожение (ферментация) моносахаридов
Брожение – это расщепление моносахаридов под влиянием биологических катализаторов – ферментов, вырабатываемых микроорганизмами. Разные микроорганизмы вызывают различные виды брожения. Название вида брожения определяется названием образующихся продуктов брожения.
Брожение – сложный многостадийный биохимический процесс. Ниже приводятся лишь суммарные уравнения различных типов брожения глюкозы.
1. Спиртовое брожение:

С
6Н
12О
6 2С
2Н
5ОН + 2СО
2 2.
Маслянокислое брожение: 

С
6Н
12О
6 СН
3-СН
2-СН
2-СООН + 2Н
2 + 2СО
2 3. Молочнокислое брожение:

| Молочная кислота (образуется в организмах высших животных или мышечных сокращениях) | |
С
6Н
12О
6 2СН
3-СН-СООН

ОН
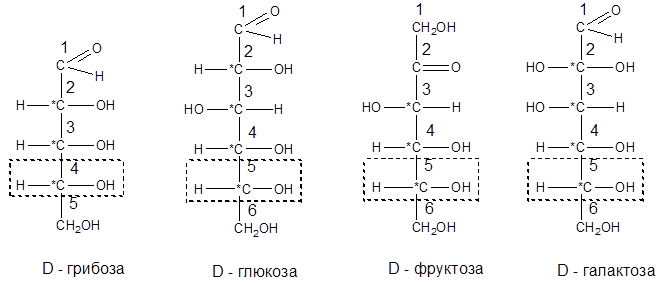



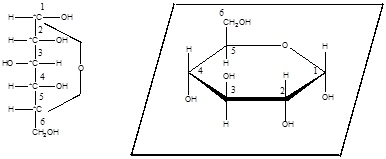

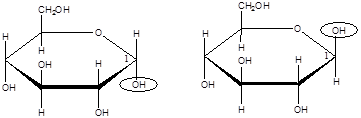
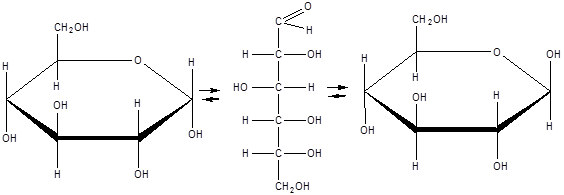
 Важнейшей кетогексозой является D-фруктоза (изомер D-глюкозы). Для циклических форм фруктозы характерны фуранозные структуры. Фуранозный цикл образуется в результате взаимодействия карбонильной (кетонной) группы со спиртовой группой при 5-м углеродном атоме.
Важнейшей кетогексозой является D-фруктоза (изомер D-глюкозы). Для циклических форм фруктозы характерны фуранозные структуры. Фуранозный цикл образуется в результате взаимодействия карбонильной (кетонной) группы со спиртовой группой при 5-м углеродном атоме.
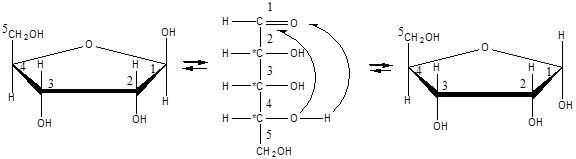
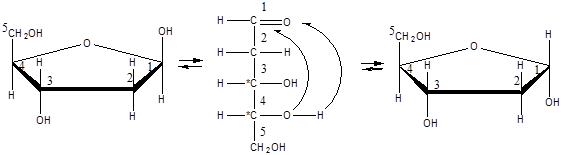
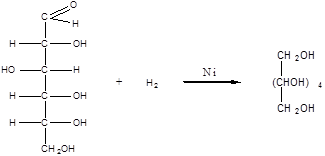

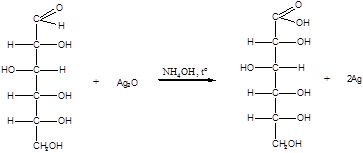
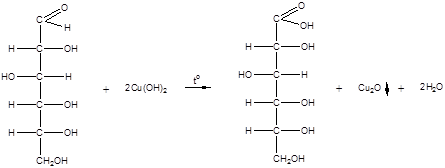
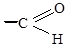 окисляется до карбоксильной группы
окисляется до карбоксильной группы 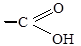 .
.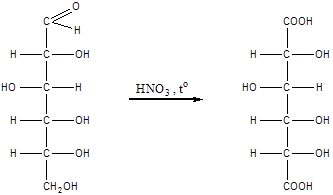
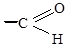 и первичная спиртовая группа – CH2OH окисляется до карбоксильных групп
и первичная спиртовая группа – CH2OH окисляется до карбоксильных групп 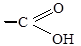 .
.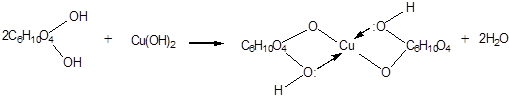
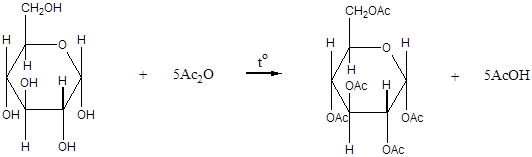
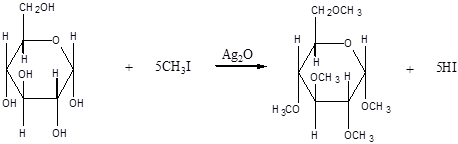

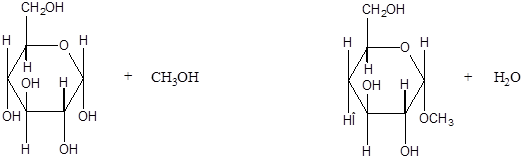






 2015-05-06
2015-05-06 12365
12365

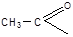 )
)