При анализе влияния различных факторов на скорость неэлементарных реакций (структура реагентов, растворитель и др.) необходимо во всей цепи элементарных реакций, составляющих механизм брутто-реакции, выделять лимитирующую или скорость-определяющую стадию. По своей природе эта стадия протекает энергетически наиболее трудно ипоэтому ее скорость определяет скорость неэлементарного процесса в целом. Выделение в механизме реакций скорость-определяющей стадии имеет принципиальное значение, поскольку все факторы, влияющие на эту стадию, аналогичным образом влияют на скорость реакции в целом.
При анализе влияние различных факторов на скорость-определяющую стадию необходимо использовать метод активированного комплекса (переходного состояния). Согласно теории абсолютных скоростей реакций активированный комплекс рассматривается как молекула, обладающая обычными термодинамическими свойствами. Принято, что реагенты находятся в равновесии с активированным комплексом, представляющим собой высшую точку на диаграмме потенциальный энергией, изображающей переход реагентов в продукты. Координату реакции можно рассматривать как расстояние между любыми двумя атомами в реагирующей системе, между которыми завязывается или рвется химическая связь.
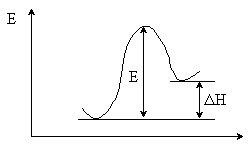
В большинстве случаев успех реакции определяется высотой энергетического барьера (энергией активации Е), который должна преодолеть система на своем пути от реагентов к продуктам реакции. Можно видеть, что энергия активации представляет собой разность между энергией переходного и исходного состояний
Е = Н¹ – Нисх
Из этого следует, что зная, как влияет тот или иной фактор на энергию исходного и переходного состояний можно предсказать изменение величины Е от действия этого фактора, а следовательно, и изменение скорости реакций.
Анализируя подобным образом влияние структурных и других факторов на скорость скорость-определяющей стадии можно полученные выводы распространить на реакцию в целом.
 2015-04-23
2015-04-23 2046
2046








