Аминокислоты в молекуле белка соединены между собой пептидными связями. Эти связи можно расщепить при помощи ферментов и под воздействием концентрированных кислот и щелочей при высокой температуре. При этом происходит гидролиз, т.е. расщепление его на полипептиды, и в конечном итоге, на аминокислоты. При гидролизе белка происходит нарастание количества свободных аминных и карбоксильных групп. По нарастанию количества этих групп можно судить о степени гидролиза белка.
Аминным азотом называют азот свободных аминных групп, содержащихся в аминокислотах, полипептидах и белках.
По приросту аминного азота можно следить за скоростью гидролиза белков, определить конец гидролиза.
Определение аминного азота проводится в процессе хранения, а также при технологической обработке рыбы.
Определение его необходимо также при изучение обмена белков и аминокислот в организме.
Аминокислоты – амфотерные электролиты, поэтому в водных растворах они преимущественно находятся в виде внутренних солей:
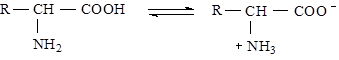
Вследствии этого непосредственное титрометрическое определение аминных и карбоксильных групп в молекулах аминокислот практически невозможно. Поэтому перед титрованием раствор, содержащий аминокислоты, обрабатывают раствором формальдегида, способного связывать свободные аминогруппы с образованием метиленовых производных аминокислот (Шиффовые основания).
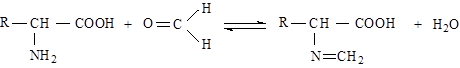
После такой обработки карбоксильные группы можно оттитровать раствором щелочи:
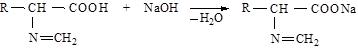
Считают, что количество карбоксильных групп эквивалентно количеству аминных групп, нейтрализованных щелочью.
Ход работы:
Подготовка пробы
Навеску рыбы (фарш) не более 4 г переносят в мерную колбу на 200-250 мл (объем и навеску записать) и наливают дистиллированной воды 1/3 колбы. Тщательно перемешивают содержимое колбы, помещают ее в кипящую водяную баню на 5 минут. После этого колбу с содержимым охлаждают и доводят до метки дистиллированной водой. Для удаления осадка скоагулировавшего белка раствор фильтруют через складчатый фильтр.
Определение аминного азота
Титрование проводят параллельно в 3-х конических колбах емкостью 300 мл.
I колба: Определение кислотности фильтрата
В коническую колбу емкостью 300 мл отмеряют пипеткой 20-25 мл фильтрата (объем пипетки записать), добавляют 0,4 мл индикатора №1 и 1 мл индикатора №2. Титруют 0,2 N раствором NаОН. Конец титрования определяют по изменению синей окраски до зеленой.
II колба: Определение аминного азота
В колбу пипеткой отмеряют 20-25 мл фильтрата (той же пипеткой, что и первую колбу), из бюретки под тягой добавляют 10 мл формалина и 1 мл индикатора №2. Титруют 0.2 N раствором NаОH. Конец титрования определяют по переходу желтой окраски раствора в фиолетовую.
III колба: Определение кислотности формалина
В колбу пипеткой отмеряют 20-25 мл дистиллированной воды (объем воды равен объему взятого выше фильтрата), добавляют 10 мл формалина и 1 мл индикатора №2. Титруют 0,2 N раствором NаОН. Конец титрования определяем так же, как во второй колбе.
Расчет ведут по формуле:
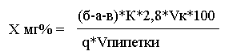
X – результат определения аминного азота в мг %.
q – навеска исследуемого вещества в г.
2.8 – количество мг азота, эквивалентное 1 мл 0.2 N раствора NаОН.
а,б,в – результаты титрования колб №1,2,3.
К – поправочный коэффициент точности приготовленного раствора 0.2N NаОН.
Vк – обьем колбы.
Чтобы сделать вывод об изменении аминного азота в процессе термостатирования рыбы определение аминного азота проводим:
1) В исходной пробе
2) В той же пробе, выдержанной в термостате несколько часов, сутки при Т=37-40°С
 2015-04-30
2015-04-30 1251
1251
