Угольная кислота — слабая двухосновная кислота с химической формулой H2CO3, образуется в малых количествах при растворении углекислого газа в воде, в том числе и углекислого газа из воздуха. Угольная кислота имеет 2 ступени диссоциации: H2CO3=H++HCO3-; т HCO3-=H++CO32-.
В природных водах, кроме так называемой «свободной» углекислоты, находящейся в них в виде растворенного углекислого газа CO2, и недиссоциированных молекул угольной кислоты H2CO3 содержатся бикарбонатные ионы HCO3-, а в некоторых случаях карбонатные ионы CO32-.
Соотношение форм угольной кислоты в воде при 250С и различных значениях pH, %
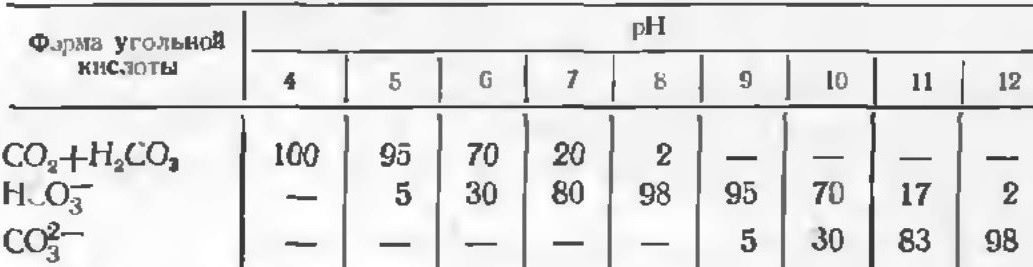
В водных растворах существует кинетическое равновесие между различными формами угольной кислоты: 2HCO3-=CO32-+H2O+CO2.
Из этого уравнения следует, что для поддержания в растворе определенной концентрации HCO3- требуется, чтобы в воде присутствовало соответствующее этой концентрации количество свободной равновесной углекислоты CO2.
Стабильной называется вода, в которой фактическая концентрация СО2 соответствует равновесной концентрации СО2. При равенстве фактической и равновесной концентрации СО2 равновесие никуда не сдвигается и вода будут стабильной.
Агрессивной называется вода с избыточным содержанием CO2 (выше равновесного). Агрессивность воды зависит от содержания CO2, а также от солесодержания воды (чем выше солесодержание, тем вода агрессивней).
Индекс стабильности воды: Разность между экспериментально найденным значением рНфакт и рНравн –индекс стабильности. Ис= рНфакт- рНравн. Если Ис=0-стабильна,если Ис<0-агрессивна, если Ис>0-нестабильна.
 2015-05-14
2015-05-14 2812
2812
