Известкование реализуется при обработке исходной воды в осветлителях суспензией гашеной извести Са(ОН)2, называемой известковым молоком. Основное назначение известкования - снижение щелочности обрабатываемой воды.
Процесс известкования:
1) Вводим известь: CaO+H2O=Ca(OH)2;
2) Связывание свободного углекислого газа: CO2+Ca(OH)2=CaCO3+H2O;
3) Снижение карбонатной жесткости и щелочности:
Ca(HCO3)2+Ca(OH)2=2CaCO3(ос)+2H2O;
Mg(HCO3)2+2Ca(OH)2=Mg(OH)2(ос)+2CaCO3(ос)+2H2O;
Mg(OH)2+H2SiO3=MgSiO3+2H2O – известкование.
4) Обезжелезивание: 4FeSO4+4Ca(OH)2+2H2O+O2=4Fe(OH)3(ос)+4CaSO4.
При известковании избыточную щелочность снизить нельзя, т.к при известковании избыточной щелочности образуется еще более сильная щелочь:
NaHCO3+Ca(OH)2→CaCO3+NaOH+H2O, где NaOH – более сильная щелочь.
В чем причина устойчивости коллоидных систем природной воды?
Природные воды представляют собой сложную многокомпонентную динамическую систему, в состав которой входят: соли (преимущественно в виде ионов, молекул и комплексов), органические вещества (в молекулярных соединениях и в коллоидном состоянии), газы (в виде молекул и гидратированных соединений) и так далее. Во взвешенном состоянии в природных водах содержатся глинистые, песчаные, гипсовые и известковые частицы, в коллоидном состоянии - различные вещества органического происхождения, кремнекислота, в истинно растворенном состоянии - в основном минеральные соли, обогащающие воду ионами.
Между коллоидными частицами одного знака заряда (содержащиеся в природной воде органические примеси, в том числе железосодержащие, и коллоидная кремнекислота заряжены отрицательно) действуют молекулярные силы притяжения (силы Ван-дер-Ваальса) и электростатические силы отталкивания (кулоновское взаимодействие). Таким образом, стабильность (устойчивость) дисперсной фазы и ее коагуляция определяются соотношением между силами притяжения и отталкивания частиц.
Дайте определение селективности адсорбции, которой подчиняется процесс обмена ионов. Приведите ряды селективности для катионов. Покажите примерное расположение слоев катионитового фильтра при катионировании и поясните на этом примере практическое значение рядов селективности?
Селективность ионного обмена (избирательность) – одни ионы по сравнению с другими ионами извлекаются из воды легче и в большем количестве. Ряд селективности для катионов: Ca2+>Mg2+>K+>NH4>Na+.
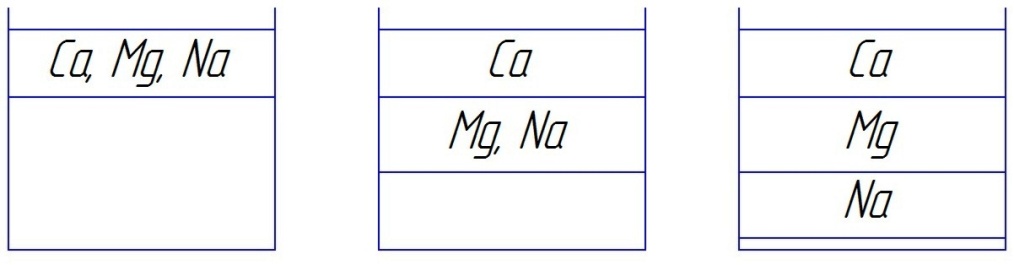
Этот ряд обозначает: 1. Каждый предыдущий элемент этого ряда извлекаются из ионита легче и большем количестве. Самый селективный Ca; 2. Каждый последующий катион ряда, ранее поглощённый ионитом, вытесняется из него всеми предыдущими. (На основе ряда для катионитов, в фильтрате первым окажется Na+, а наиболее селективным является Ca2+):
 2015-05-14
2015-05-14 1213
1213








