Опыт1. Взаимодействие железа, кобальта, никеля с кислотами
Взаимодействие с соляной кислотой
Выполнение опыта: в 3 пробирки налили по 5 капель 2н раствора соляной кислоты, а затем в одну пробирку засыпали немного железных опилок или стружек, в другую – кусочек кобальтовой стружки, в третью – кусочек никелевой стружки. Вторую и третью пробирки слегка нагрели.
Запись данных опыта: во всех реакциях выделяется водород.
а) Раствор серый
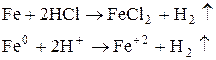
б) Раствор розовый
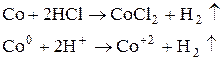
в) Раствор зеленый
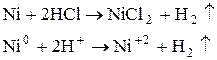
Чтобы убедиться, что в соляной кислоте образуются ионы железа (II), прилили в первую пробирку 1 каплю разбавленного раствора роданида калия.
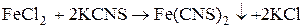
Взаимодействие с серной кислотой
Выполнение опыта: в 3 пробирки внесли по 5 капель 2н раствора серной кислоты, а в четвертую пробирку – 3 капли концентрированной серной кислоты. В первую пробирку поместили кусочек кобальтовой стружки, во вторую - кусочек никелевой стружки, в третью и четвертую – немного железных опилок. Слегка нагрели пробирки. Выделился водород. В третью и четвертую пробирку капнули 1 каплю разбавленного раствора роданида калия.
Запись данных опыта:
а) Раствор розовый
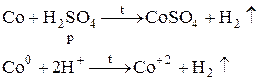
б) Раствор зеленый
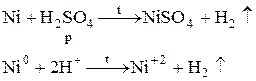
в) Раствор серый
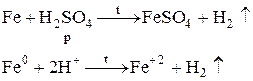
г) взаимодействие Fe с концентрированной H2SO4
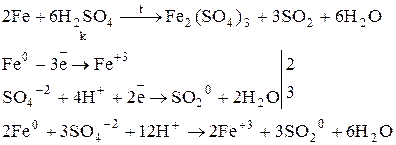
При окислении железа концентрированной серной кислотой образуются ионы Fe+3, тогда как при взаимодействии с разбавленной кислотой – Fe+2. это объясняется тем, что в концентрированной кислоте окислителем является более мощная S+6 по сравнению с H+.
 2015-05-14
2015-05-14 1959
1959