5.1. Характерные реакции на ионы Fe+2
Выполнение опыта: приготовили в пробирке раствор Мора и добавили 1 каплю раствора гексацианоферрата (III) калия (красной кровяной соли K3[Fe(CN)6.
Запись данных опыта:
Качественная реакция на Fe+2 (турнбулева синь)
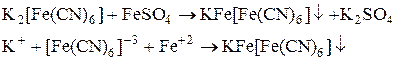 (1)
(1)
Качественная реакция на Fe+3 (берлинская лазурь)
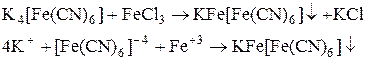 (2)
(2)
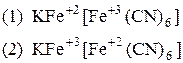
Ответы на вопросы:
1. Процессы, проходящие в доменной печи:
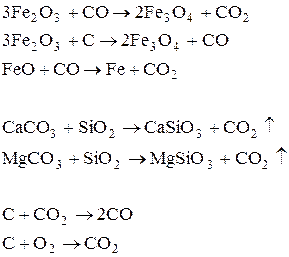
2. Для получения Fe(OH)3 требуется соль железа (II) и щелочь:
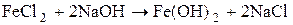 ;
;
для получения FS требуется оба элемента:
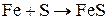
3. Закончить уравнения реакций, в которых соединения 2-х валентного железа проявляют восстановительные свойства:
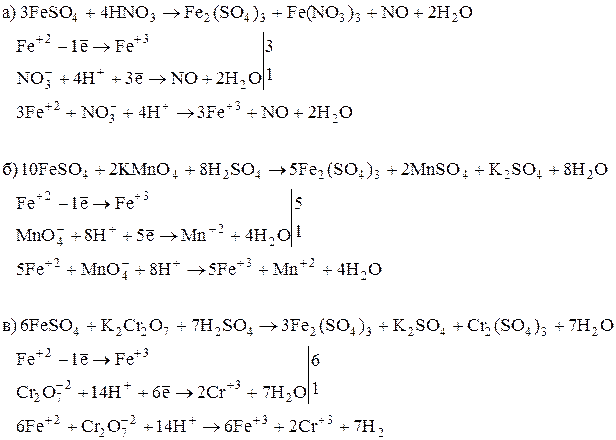
4. Закончить уравнения реакций на ион Fe+3:
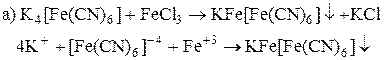
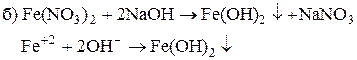
5. Закончить уравнения реакций на ион Fe+2:
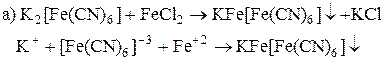
6. Закончить уравнения реакций, в которых 3-х валентное железо является окислителем:
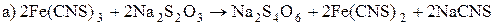
7. Закончить уравнения реакций получения ферратов калия и бария (K2FeO4, BaFeO4):
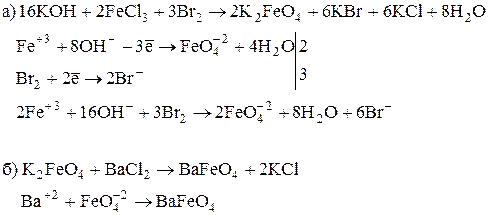
8. Как хлористое железо превратить в хлорное железо и наоборот?
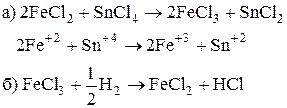
9. Составить уравнения реакций, действия на раствор Co(NO3)2 сначала небольшого количества, а затем избытка NH4OH.
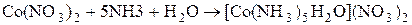
10. Составить уравнения электролиза водного раствора: FeCl3, Co(NO3)2:
| FeCl3 | |
| [K-] | [A+] |
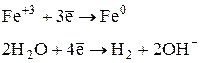 | 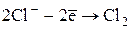 |
| 2FeCl3+2HOH→2Fe0+3Cl0+H20+2OH- |
| Co(NO3)2 | |
| [K-] | [A+] |
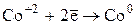 | 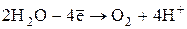 |
Co(NO3)2+HOH→Co0+ 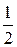 +O20+2HNO3 +O20+2HNO3 |
11. Написать уравнения гидролиза в молекулярно-ионной и сокращенной ионной форме следующих солей: FeCO3, FeCl3:
Гидролиз FeCl3:
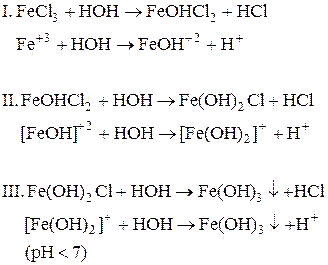
Гидролиз FeCO3:
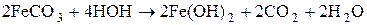
12. Закончите уравнения реакций:
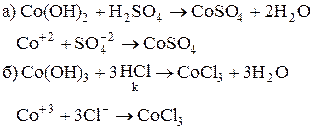
 2015-05-14
2015-05-14 5335
5335