Учебное заведение: Недоступно. Тип материала: Научная статья
I. Физико-химическая – основана на различиях в физико-химических свойствах аминокислот.
1) Гидрофобные аминокислоты (неполярные). Компоненты радикалов содержат обычно углеводородные группы и ароматические кольца. К гидрофобным аминокислотам относятся ала, вал, лей, иле, фен, три, мет.
2) Гидрофильные (полярные) незаряженные аминокислоты. Радикалы таких аминокислот содержат в своем составе полярные группировки (-ОН, -SH, -NH2). Эти группы взаимодействуют с дипольными молекулами воды, которые ориентируются вокруг них. К полярным незаряженным относятся гли, сер, тре, тир, цис, глн, асн.
3) Полярные отрицательно заряженные аминокислоты. К ним относятся аспарагиновая и глутаминовая кислоты. В нейтральной среде асп и глу приобретают отрицательный заряд.
4) Полярные положительно заряженные аминокислоты: аргинин, лизин и гистидин. Имеют дополнительную аминогруппу (или имидазольное кольцо, как гистидин) в радикале. В нейтральной среде лиз, арг и гαис приобретают положительный заряд.
II. Биологическая классификация.
1) Незаменимые аминокислоты не могут синтезироваться в организме человека и должны обязательно поступать с пищей (вал, иле, лей, лиз, мет, тре, три, фен) и еще 2 аминокислоты относятся к частично незаменимым (арг, гис).
2) Заменимые аминокислоты могут синтезироваться в организме человека (глутаминовая кислота, глутамин, пролин, аланин, аспарагиновая кислота, аспарагин, тирозин, цистеин, серин и глицин).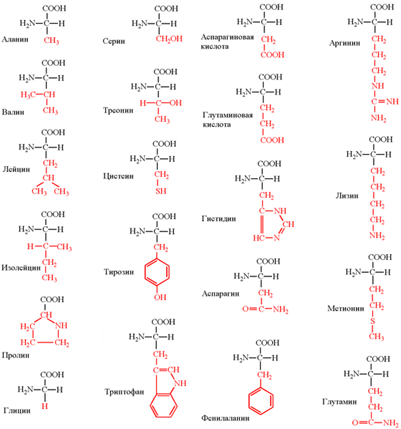
Строение аминокислот. Все аминокислоты являются α-аминокислотами. Аминогруппа общей части всех аминокислот присоединена к α-углеродному атому. Аминокислоты содержат карбоксильную группу –COOH и аминогруппу -NH2. В белке ионогенные группы общей части аминокислот участвуют в образовании пептидной связи, и все свойства белка определяются только свойствами радикалов аминокислот. Аминокислоты амфотерные соединения. Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом.
Физико-химические свойства белков.
Выделение и очистка: электрофоретическое разделение, гель-фильтрация и др. Молекулярная масса белков, амфотерность, растворимость (гидратация, высаливание). Денатурация белков, ее обратимость.
Молекулярная масса. Белки – высокомолекулярные органические азотсодержащие полимеры, построенные из аминокислот. Молекулярная масса белков зависит от количества аминокислот в каждой субъединице.
Буферные свойства. Белки – амфотерные полиэлектролиты, т.е. они сочетают в себе кислые и основные свойства. В зависимости от этого белки могут быть кислыми и основными.
Факторы стабилизации белка в растворе. ГИДРАТНАЯ ОБОЛОЧКА – это слой молекул воды, определенным образом ориентированных на поверхности белковой молекулы. Поверхность большинства белковых молекул заряжена отрицательно, и диполи молекул воды притягиваются к ней своими положительно заряженными полюсами.
Факторы, снижающие растворимость белков. Значение рН, при котором белок становится электронейтральным, называется изоэлектрической точкой (ИЭТ) белка. Для основных белков ИЭТ находится в щелочной среде, для кислых – в кислой среде. Денатурация – это последовательное нарушение четвертичной, третичной, вторичной структур белка, сопровождающееся потерей биологических свойств. Денатурированный белок выпадает в осадок. Осадить белок можно, изменяя рН среды (ИЭТ), либо высаливанием, либо действуя каким-либо фактором денатурации. Физические факторы: 1. Высокие температуры.
Часть белков подвергается денатурации уже при 40-50 2. Ультрафиолетовое облучение 3. Рентгеновское и радиоактивное облучение 4. Ультразвук 5. Механическое воздействие (например, вибрация). Химические факторы: 1. Концентрированные кислоты и щелочи. 2. Соли тяжелых металлов (например, CuSO4). 3. Органические растворители (этиловый спирт, ацетон) 4. Нейтральные соли щелочных и щелочноземельных металлов (NaCl, (NH4)2SO4)
Структурная организация белковых молекул.
Первичная, вторичная, третичная структуры. Связи, участвующие в стабилизации структур. Зависимость биологических свойств белков от вторичной и третичной структуры. Четвертичная структура белков. Зависимость биологической активности белков от четвертичной структуры (изменение конформации протомеров).
Существует четыре уровня пространственной организации белка: первичная, вторичная, третичная и четвертичная структура белковых молекул. Первичная структура белка - последовательность аминокислот в полипептидной цепи (ППЦ). Пептидная связь формируется только за счет альфа-аминогруппы и альфа-карбоксильной группы аминокислот. Вторичная структура - это пространственная организация стержня полипептидной цепи в виде α-спирали или β-складчатой структуры. В α-спирали на 10 витков приходится 36 аминокислотных остатков. Фиксируется α-спираль с помощью водородных связей между NH-группами одного витка спирали и С=О группами соседнего витка.
β-Складчатая структура удерживается также водородными связями между С=О и NH-группами. Третичная структура - особое взаимное расположение в пространстве спиралеобразных и складчатых участков полипептидной цепи. В формировании третичной структуры участвуют прочные дисульфидные связи и все слабые типы связей (ионные, водородные, гидрофобные, Ван-дер-ваальсовые взаимодействия). Четвертичная структура – трехмерная организация в пространстве нескольких полипептидных цепей. Каждая цепь называется субъединицей (или протомером). Поэтому белки, обладающие четвертичной структурой, называют олигомерными белками.
4. Простые и сложные белки, их классификация.
Характер связей простетических групп с белком. Биологические функции белков. Способность к специфическим взаимодействиям с лигандом.
Простые белки построены из остатков аминокислот и при гидролизе распадаются соответственно только на свободные аминокислоты. Сложные белки – это двухкомпонентные белки, которые состоят из какого-либо простого белка и небелкового компонента, называемого простетической группой. При гидролизе сложных белков, помимо свободных аминокислот, освобождается небелковая часть или продукты ее распада. Простые белки в свою очередь делятся на основании некоторых условно выбранных критериев на ряд подгрупп: протамины, гистоны, альбумины, глобулины, проламины, глютелины и др.
Классификация сложных белков:
- фосфопротеины (содержат фосфорную кислоту), хромопротеины (в состав их входят пигменты),
- нуклеопротеины (содержат нуклеиновые кислоты), гликопротеины (содержат углеводы),
- липопротеины (содержат липиды) и металлопротеины (содержат металлы).
Активный центр белковой молекулы. При функционировании белков может происходить их связывание с лигандами – низкомолекулярными веществами. Лиганд присоединяется к определенному участку в белковой молекуле – активному центру. Активный центр формируется на третичном и четвертичном уровнях организации белковой молекулы и образуется благодаря притяжению боковых радикалов определенных аминокислот (между -ОН группами сер формируются водородные связи, ароматические радикалы связаны гидрофобными взаимодействиями, -СООН и –NH2 - ионными связями).
Углеводсодержащие белки: гликопротеины, протеогликаны.
Основные углеводы организма человека: моносахариды, дисахариды, гликоген, гетерополисахариды, их структура и функции.
Углеводсодержащие белки (гликопротеины и протеогликаны). Простетическая группа гликопротеинов может быть представлена моносахаридами (глюкозой, галактозой, маннозой, фруктозой, 6-дезоксигалактозой), их аминами и ацетилированными производными аминосахаров (ацетилглюкоза, ацетилгалактоза. На долю углеводов в молекулах гликопротеинов приходится до 35%. Гликопротеины преимущественно глобулярные белки. Углеводный компонент протеогликанов может быть представлен несколькими цепями гетерополисахаридов.
Биологические функции гликопротеинов:
1. транспортная (белки крови глобулины транспортируют ионы железа, меди, стероидные гормоны);
2. защитная: фибриноген осуществляет свертывание крови; б. иммуноглобулины обеспечивают иммунную защиту;
3. рецепторная (на поверхности клеточной мембраны расположены рецепторы, которые обеспечивают специфическое взаимодействие).
4. ферментативная (холинэстераза, рибонуклеаза);
5. гормональная (гормоны передней доли гипофиза – гонадотропин, тиреотропин).
Биологические функции протеогликанов: гиалуроновая и хондроитинсерная кислоты, кератинсульфат выполняют структурную, связующую, поверхностно-механическую функции.
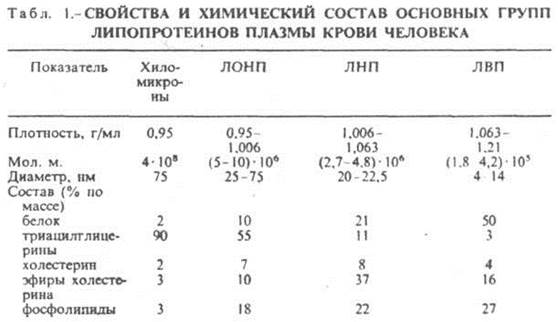
Л ипопротеины тканей человека. Классификация липидов.
Основные представители: триацилглицерины, фосфолипиды, гликолипиды, холестериды. Их структура и функции. Незаменимые жирные кислоты и их производные. Состав, строение и функции липопротеинов крови.
Нуклеопротеины.
Особенности белковой части. История открытия и изучения нуклеиновых кислот. Структура и функции нуклеиновых кислот. Первичная и вторичная структура ДНК и РНК. Виды РНК. Строение хромосом.
Нуклеопротеины - сложные белки, в состав которых входит белок (протамин или гистон), небелковая часть представлена нуклеиновыми кислотами (НК): дезоксирибонуклеиновой кислотой (ДНК) и рибонуклеиновой кислотой (РНК). Протамины и гистоны – белки с резко выраженными основными свойствами, т.к. они содержат более 30% арг и лиз.
Нуклеиновые кислоты (НК) - это длинные полимерные цепи, состоящие из многих тысяч мономерных единиц, которые соединяются между собой 3`,5`- фосфоди-эфирными связями. Мономером НК является мононуклеотид, который состоит из азотистого основания, пентозы и остатка фосфорной кислоты. Азотистые основания бывают пуриновые (А и Г) и пиримидиновые (Ц, У, Т). В качестве пентозы выступает β– Д- рибоза или β –Д- дезоксирибоза. Азотистое основание соединено с пентозой N-гликозидной связью. Пентоза и фосфат связаны друг с другом сложноэфирной связью между –ОН группой, расположенной у С5’-атома пентозы, и фосфатом.
1. ДНК содержит А, Г, Т и Ц, дезоксирибозу и фосфорную кислоту. ДНК находится в ядре клетки и составляет основу сложного белка хроматина.
2. РНК содержит А, Г, У и Ц, рибозу и фосфорную кислоту.
Различают 3 вида РНК:
а) м-РНК (информационная или матричная) – копия участка ДНК, содержит информацию о структуре белка;
б) р-РНК образует скелет рибосомы в цитоплазме, выполняет важную роль при сборке белка на рибосоме в процессе трансляции;
в) т-РНК участвует в активации и транспорте АК к рибосоме, локализована в цитоплазме. НК имеют первичную, вторичную и третичную структуры.
Первичная структура НК одинакова для всех видов – линейная полинуклеотидная цепь, в которой мононуклеотиды связаны 3’, 5’-фосфодиэфирными связями. Каждая полинуклеотидная цепь имеет 3’ и 5’, эти концы заряжены отрицательно.
Вторичная структура ДНК представляет собой двойную спираль. ДНК состоит из 2-х цепей, закрученных в спираль вправо вокруг оси. Виток спирали = 10 нуклеотидов, что составляет в длину 3,4 нм. Обе спирали антипараллельны.
Третичная структура ДНК - это результат дополнительного скручивания в пространстве молекулы ДНК. Это происходит при взаимодействии ДНК с белком. При взаимодействии с октамером гистона двойная спираль накручивается на октамер, т.е. превращается в суперспираль.
Вторичная структура РНК – полинуклеотидная нить, изогнутая в пространстве. Эта изогнутость обусловлена образованием водородных связей между комплементарными азотистыми основаниями. У т-РНК вторичная структура представлена «клеверным листом», в котором различаю комплементарные и некомплементарные участки. Вторичная структура р-РНК – спираль одиночной изогнутой РНК, а третичная – скелет рибосомы. Поступая из ядра в ЦЗ, м-РНК образует со специфическими белками – информомерами комплексы (третичная структура м-РНК) и называются информосомами.
Хромопротеины, их классификация. Флавопротеины, их структура и функции.
Гемопротеины, структура, представители: гемоглобин, миоглобин, каталаза, пероксидаза, цитохромы. Функции гемопротеинов.
Фосфопротеины в качестве простетической группы содержат остаток фосфорной кислоты. Примеры: казеин и казеиноген молока, творога, молочных продуктов, вителлин яичного желтка, овальбумин яичного белка, ихтуллин икры рыб. Фосфопротеинами богаты клетки ЦНС.
Фосфопротеины обладают многообразными функциями:
1. Питательная функция. Фосфопротеины молочных продуктов легко перевариваются, усваиваются и являются источником незаменимых аминокислот и фосфора для синтеза белков тканей ребенка.
2. Фосфорная кислота необходима для полноценного формирования нервной и костной тканей ребенка.
3. Фосфорная кислота участвует в синтезе фосфолипидов, фосфопротеинов, нуклеотидов, нуклеиновых кислот.
4. Фосфорная кислота осуществляет регуляцию активности ферментов путем фосфорилирования при участии ферментов протеинкиназ. Фосфат присоединяется к – ОН группе серина или треонина сложноэфирными связями: Хромопротеины - сложные белки с окрашенной небелковой частью. К ним относятся флавопротеины (желтые) и гемопротеины (красные). Флавопротеины в качестве простетической группы содержат производные витамина В2 – флавины: флавинадениндинуклеотид (ФАД) или флавинмононуклеотид (ФМН). Они являются небелковой частью ферментов дегидрогеназ, катализирующих окислительно-восстановительные реакции.
Гемопротеины в качестве небелковой группы содержат гем – железопорфириновый комплекс.
Гемопротеины подразделяют на два класса:
1. ферменты: каталаза, пероксидаза, цитохромы;
2. неферменты: гемоглобин и миоглобин.
Ферменты каталаза и пероксидаза разрушают перекись водорода, цитохромы являются переносчиками электронов в цепи переноса электронов. Неферменты. Гемоглобин транспортирует кислород (от легким к тканям) и углекислый газ (от тканей к легким); миоглобин – депо кислорода в работающей мышце. Гемоглобин – тетрамер, т.к. состоит из 4-х субъединиц: глобин в этом тетрамере представлен 4-мя полипептидными цепями 2-х разновидностей: 2 α и 2 β цепи. Каждая субъединица связана с гемом. Физиологические типы гемоглобина: 1. HbP – примитивный гемоглобин формируется у зародыша. 2. HbF – фетальный гемоглобин – гемоглобин плода. Замена HbP на HbF происходит к 3-х месячному возрасту человека.
Ферменты, история открытия и изучения ферментов, особенности ферментативного катализа.
Специфичность действия ферментов. Зависимость скорости ферментативных реакций от температуры, рН, концентрации фермента и субстрата.
Ферменты – биологические катализаторы белковой природы, образуемые живой клеткой, действующие с высокой активностью и специфичностью.
Сходство ферментов с небиологическими катализаторами заключается в том, что:
- ферменты катализируют энергетически возможные реакции;
- энергия химической системы остаётся постоянной;
- в ходе катализа направление реакции не изменяется;
- ферменты не расходуются в процессе реакции.
Отличия ферментов от небиологических катализаторов заключаются в том, что:
- скорость ферментативных реакций выше, чем реакций, катализируемых небелковыми катализаторами;
- ферменты обладают высокой специфичностью;
- ферментативная реакция проходит в клетке, т.е. при температуре 37 °С, постоянном атмосферном давлении и физиологическом значении рН;
- скорость ферментативной реакции может регулироваться.
Современная классификация ферментов основана на природе катализируемых ими химических превращений. В основу классификации берется тип реакции, катализируемой ферментом.
Фе рменты разделяют на 6 классов:
1. Оксидоредуктазы - катализируют окислительно-восстановительные реакции
2. Трансферазы – перенос групп
3. Гидролазы – гидролиз
4. Лиазы – негидролитическое расщепление субстрата
5. Изомеразы – изомеризация
6. Лигазы (синтетазы) - синтез с использованием энергии (АТФ)
Номенклатура ферментов.
1. Тривиальное название (пепсин, трипсин).
2. Название фермента может складываться из названия субстрата с прибавлением окончания «аза»
(аргиназа гидролизует аминокислоту аргинин).
3. Добавление окончания «аза» к названию катализируемой реакции (гидролаза катализирует
гидролиз, дегидрогеназа – дегидрирование органической молекулы, т.е. отнятие протонов и электронов от субстрата).
4. Рациональное название – название субстратов и характер катализируемых реакций (АТФ + гексоза гексозо-6-фосфат + АДФ. Фермент: АТФ: D-гексоза-6-фосфотрансфераза).
5. Индексирование ферментов (каждому ферменту присваиваются 4 индекса или порядковых номера): 1.1.1.1 – АДГ, 1.1.1.27 – ЛДГ.
Зависимость скорости ферментативной реакции от рН среды. Для каждого фермента существует значение рН, при котором наблюдается его максимальная активность. Отклонение от оптимального значения рН приводит к понижению ферментативной активности. Влияние рН на активность ферментов связано с ионизацией функциональных групп аминокислотных остатков данного белка, обеспечивающих оптимальную конформацию активного центра фермента. При изменении рН от оптимальных значений происходит изменение ионизации функциональных групп молекулы белка.
Например, при закислении среды происходит протонирование свободных аминогрупп (NH3+), а при защелачивании происходит отщепление протона от карбоксильных групп (СОО-). Это приводит к изменению конформации молекулы фермента и конформации активного центра; следовательно, нарушается присоединение субстрата, кофакторов и коферментов к активному центру. Ферменты, работающие в кислых условиях среды (например, пепсин в желудке или лизосомальные ферменты), эволюционно приобретают конформацию, обеспечивающую работу фермента при кислых значениях рН. Однако большая часть ферментов организма человека имеет оптимум рН, близкий к нейтральному, совпадающий с физиологическим значением рН.
Зависимость скорости ферментативной реакции от температуры среды. Повышение температуры до определённых пределов оказывает влияние на скорость ферментативной реакции, подобно влиянию температуры на любую химическую реакцию. С повышением температуры ускоряется движение молекул, что приводит к повышению вероятности взаимодействия реагирующих веществ. Кроме того, температура может повышать энергию реагирующих молекул, что также приводит к ускорению реакции.
Однако скорость химической реакции, катализируемая ферментами, имеет свой температурный оптимум, превышение которого сопровождается понижением ферментативной активности, возникающим из-за термической денатурации белковой молекулы. Для большинства ферментов человека оптимальна температура 37-38 °С. Специфичность – очень высокая избирательность ферментов по отношению к субстрату. Специфичность фермента объясняется совпадением пространственной конфигурации субстрата и субстратного центра (стерическое совпадение). За специфичность фермента ответственен как активный центр фермента, так и вся его белковая молекула. Активный центр фермента определяет тип реакции, который может осуществить данный фермент. Различают три вида специфичности:
Абсолютная специфичность. Такой специфичностью обладают ферменты, которые действуют только на один субстрат. Например, сахараза гидролизует только сахарозу, лактаза – лактозу, мальтаза – мальтозу, уреаза – мочевину, аргиназа – аргинин и т.д. Относительная специфичность – это способность фермента действовать на группу субстратов с общим типом связи, т.е. относительная специфичность проявляется только по отношению к определенному типу связи в группе субстратов. Пример: липаза расщепляют сложноэфирную связь в жирах животного и растительного происхождения. Амилаза гидролизует α-гликозидную связь в крахмале, декстринах и гликогене. Алкогольдегидрогеназа окисляет спирты (метанол, этанол и др.).
Стереохимическая специфичность – это способность фермента действовать только на один стереоизомер.
Например: 1) α, β-изомерия: α – амилаза слюны и сока поджелудочной железы расщепляет только α-глюкозидные связи в крахмале и не расщепляет β-глюкозидные связи клетчатки. Международной единицей (МЕ) активности ферментов является количество фермента, способного превратить 1 мкмоль субстрата в продукты реакции за 1 мин при 25 °С и оптимуме рН. Катал соответствует количеству катализатора, способного превращать 1 моль субстрата в продукт за 1 сек при 25 °С и оптимуме рН. Удельная активность фермента – число единиц ферментативной активности фермента в расчете на 1 мг белка. Молярная активность – это отношение числа единиц ферментативной активности каталов или МЕ к числу молей фермента.
Строение ферментов. Структура и функции активного центра.
Механизм действия ферментов. Кофакторы ферментов: ионы металлов и коферменты, их участие в работе ферментов. Активаторы ферментов: механизм действия. Ингибиторы ферментативных реакций: конкурентные, неконкурентные, необратимые. Лекарственные препараты – ингибиторы ферментов (примеры).
По строению ферменты могут быть:
1. однокомпонентные (простые белки),
2. двухкомпонентные (сложные белки).
К ферментам - простым белкам – относятся пищеварительные ферменты (пепсин, трипсин). К ферментам – сложным белкам – можно отнести ферменты, катализирующие окислительно - восстановительные реакции. Для каталитической активности двухкомпонентных ферментов необходим дополнительный химический компонент, который называется кофактор, их могут играть как неорганические вещества (ионы железа, магния, цинка, меди и др.), так и органические вещества – коферменты (например, активные формы витаминов).
Для работы ряда ферментов необходимы и кофермент, и ионы металлов (кофактор). Коферменты – низкомолекулярные органические вещества небелковой природы, связанные с белковой частью фермента временно и непрочно. В случае, когда небелковая часть фермента (кофермент) связана с белковой прочно и постоянно, то такую небелковую часть называют простетической группой. Белковая часть сложного белка-фермента называют апоферментом. Вместе апофермент и кофактор образуют холофермент.
В процессе ферментативного катализа, принимает участие не вся белковая молекула, а лишь определенный участок – активный центр фермента. Активный центр ферментов представляет часть молекулы фермента, к которой присоединяется субстрат и от которой зависят каталитические свойства молекулы фермента. В активном центре фермента выделяют «контактный» участок – участок, притягивающий и удерживающий субстрат на ферменте благодаря своим функциональным группам и «каталитический» участок, функциональные группы которого непосредственно участвуют в каталитической реакции. У некоторых ферментов, кроме активного центра, имеется еще «другой» центр – аллостерический.
С аллостерическим центром взаимодействуют различные вещества (эффекторы), чаще всего различные метаболиты. Соединение этих веществ с аллостерическим центром приводит к изменению конформации фермента (третичной и четвертичной структуры). Активный центр в молекуле фермента либо создается, либо он нарушается. В первом случае реакция ускоряется, во втором случае тормозится. Поэтому аллостерический центр называют регуляторным центром фермента. Ферменты, имеющие в своей структуре аллостерический центр, называются регуляторными или аллостерическими. В основу теории механизма действия ферментов положено образование фермент-субстратного комплекса.
Механизм действия фермента:
1. образование фермент-субстратного комплекса, субстрат прикрепляется к активному центру фермента.
2. на второй стадии ферментативного процесса, которая протекает медленно, происходят электронные перестройки в фермент-субстратном комплексе.
Фермент (En) и субстрат (S) начинают сближаться, чтобы вступить в максимальный контакт и образовать единый фермент-субстратный комплекс. Продолжительность второй стадии зависит от энергии активации субстрата или энергетического барьера данной химической реакции. Энергия активации – энергия, необходимая для перевода всех молекул 1 моля S в активированное состояние при данной температуре. Для каждой химической реакции существует свой энергетический барьер. Благодаря образованию фермент-субстратного комплекса снижается энергия активации субстрата, реакция начинает протекать на более низком энергетическом уровне. Поэтому вторая стадия процесса лимитирует скорость всего катализа.
3. на третьей стадии происходит сама химическая реакция с образованием продуктов реакции. Третья стадия процесса непродолжительна. В результате реакции субстрат превращается в продукт реакции; фермент-субстратный комплекс распадается и фермент выходит неизмененным из ферментативной реакции. Таким образом, фермент дает возможность за счет образования фермент-субстратного комплекса проходить химической реакции обходным путем на более низком энергетическом уровне.
Кофактор - небелковое вещество, которое обязательно должно присутствовать в организме в небольших количествах, чтобы соответствующие ферменты смогли выполнить свои функции. В состав кофактора входят коферменты и ионы металлов (например, ионы натрия и калия).
Все ферменты относятся к глобулярным белкам, причем каждый фермент выполняет специфическую функцию, связанную с присущей ему глобулярной структурой. Однако активность многих ферментов зависит от небелковых соединений, называемых кофакторами. Молекулярный комплекс белковой части (апофермента) и кофактора называется холоферментом.
Роль кофактора могут выполнять ионы металлов (Zn2+, Mg2+, Mn2+, Fe2+, Cu2+, K+, Na+) или сложные органические соединения. Органические кофакторы обычно называют коферментами, некоторые из них являются производными витаминов. Тип связи между ферментом и коферментом может быть различным. Иногда они существуют отдельно и связываются друг с другом во время протекания реакции. В других случаях кофактор и фермент связаны постоянно и иногда прочными ковалентными связями. В последнем случае небелковая часть фермента называется простетической группой.
Роль кофактора в основном сводится к следующему:
- изменение третичной структуры белка и создание комплементарности между ферментом и субстратом;
- непосредственное участие в реакции в качестве еще одного субстрата.
Активаторами могут быть:
1) кофакторы, т.к. они важные участники ферментативного процесса. Например, металлы, входящие в состав каталитического центра фермента: амилаза слюны активна в присутствии ионов Са, лактатдегидрогеназа (ЛДГ) – Zn, аргиназа – Mn, пептидаза – Mg и коферменты: витамин С, производные различных витаминов (НАД, НАДФ, ФМН, ФАД, КоАSH и др.). Они обеспечивают связывание активного центра фермента с субстратом.
2) анионы также могут оказывать активирующее влияние на активность фермента, например, анионы
Сl - активируют слюнную амилазу;
3) активаторами могут служить также вещества, создающие оптимальное значение рН среды для проявления ферментативной активности, например, НСl для создания оптимальной среды желудочного содержимого для активации пепсиногена в пепсин;
4) активаторами являются также вещества, переводящие проферменты в активный фермент, например, энтерокиназа кишечного сока активирует превращение трипсиногена в трипсин;
5) активаторами могут быть разнообразные метаболиты, которые связываются с аллостерическим центром фермента и способствуют формированию активного центра фермента.

Ингибиторы - это вещества, которые тормозят активность ферментов. Различают два основных типа ингибирования: необратимое и обратимое. При необратимом ингибировании - ингибитор прочно (необратимо) связывается с активным центром фермента ковалентными связями, изменяет конформацию фермента. Таким образом, могут действовать на ферменты соли тяжелых металлов (ртути, свинца, кадмия и др.). Обратимое ингибирование - это такой тип ингибирования, когда активность ферментов может восстанавливаться. Обратимое ингибирование бывает 2-х типов: конкурентное и неконкурентное. При конкурентном ингибировании обычно субстрат и ингибитор очень похож по химическому строению.
При этом виде ингибирования субстрат (S) и ингибитор (I) одинаково могут связываться с активным центром фермента. Они конкурируют друг с другом за место в активном центре фермента. Классический пример, конкурентного ингибирование – торможение действия сукцинатдегидрогеназы малоновой кислотой. Неконкурентные ингибиторы связываются с аллостерическим центром фермента.
Вследствие этого происходят изменения конформации аллостерического центра, которые приводят к деформации каталитического центра фермента и снижению ферментативной активности. Часто аллостерическими неконкурентными ингибиторами выступают продукты метаболизма. Лекарственные свойства ингибиторов ферментов (Контрикал, Трасилол, Аминокапроновая кислота, Памба). Контрикал (апротинин) применяют для лечения острого панкреатита и обострения хронического панкреатита, острого панкреонекроза, острых кровотечений.
Регуляция действия ферментов. Аллостерический центр, аллостерические ингибиторы и активаторы (примеры). Регуляция активности ферментов путем фосфорилирования и дефосфорилирования (примеры). Виды гормональной регуляции активности ферментов.
Различия ферментов состава органов и тканей.
Органоспецифические ферменты, изоферменты (на примере ЛДГ, МДГ и др.). Изменения активности ферментов при патологии. Энзимопатии, энзимодиагностика и энзимотерапия.
Изоферменты — это различные по аминокислотной последовательности изоформы одного и того же фермента, существующие в одном организме, но, как правило, в разных его клетках, тканях или органах.
Изоферменты, как правило, высоко гомологичны по аминокислотной последовательности. Все изоферменты одного и того же фермента выполняют одну и ту же каталитическую функцию, но могут значительно различаться по степени каталитической активности, по особенностям регуляции или другим свойствам. Примером фермента, имеющего изоферменты, является амилаза — панкреатическая амилаза отличается по аминокислотной последовательности и свойствам от амилазы слюнных желёз, кишечника и других органов. Это послужило основой для разработки и применения более надёжного метода диагностики острого панкреатита путём определения не общей амилазы плазмы крови, а именно панкреатической изоамилазы.
Энзимопатии – заболевания, вызванные нарушением синтеза ферментов:
а) в полном или частичном отсутствии ферментативной активности;
б) в чрезмерном усилении ферментативной активности;
в) в продукции патологических ферментов, которые не встречаются у здорового человека.
Различают наследственные и приобретенные энзимопатии. Наследственные энзимопатии связаны с нарушением в генетическом аппарате клетки, приводящим к отсутствию синтеза определенных ферментов.
К наследственным заболеваниям относятся энзимопатии, связанные с нарушением превращения аминокислот:
1. Фенилкетонурия – наследственное нарушение синтеза фермента фенилаланингидроксилазы, при участии которого происходит превращение фенилаланина в тирозин. При этой патологии происходит увеличение концентрации в крови фенилаланина. При этом заболевании у детей необходимо исключить из рациона фенилаланин.
2. Альбинизм – заболевание, связанное с генетическим дефектом фермента тирозиназы. При потере меланоцитами способности синтезировать этот фермент (окисляет тирозин в ДОФА и ДОФА-хинон) в коже, волосах и сетчатке глаза не образуется меланин.
Приобретенные энзимопатии, т.е. нарушение синтеза ферментов, могут возникать в результате:
1. длительного применения лекарств (антибиотиков, сульфаниламидов);
2. перенесенных инфекционных заболеваний;
3. вследствие авитаминозов;
4. злокачественных опухолей.
Энзимодиагностика определение активности ферментов для диагностики заболеваний. Ферменты плазмы крови делят на 3 группы: секреторные, индикаторные и экскреторные. Индикаторные – клеточные ферменты. При заболеваниях, сопровождающихся повреждением клеточных мембран, эти ферменты в большом количестве появляются в крови, свидетельствуя о патологии в определенных тканях. Например, активность амилазы в крови и моче увеличивается при острых панкреатитах.
Для энзимодиагностики проводят определение изоферментов. При патологических состояниях выход фермента в кровь может усилиться в связи с изменением состояния мембраны клетки. Исследование активности ферментов крови и других биологических жидкостях широко применяется с целью диагностики заболеваний. Например, диастаза мочи и амилаза крови при панкреатитах (повышение активности), понижение активности амилазы – при хроническом панкреатите.
Энзимотерапия – применение ферментов в качестве лекарственных препаратов. Например, смесь ферментативных препаратов пепсина, трипсина, амилазы (панкреатин, фестал) используют при заболеваниях ЖКТ с пониженной секрецией, трипсин и химотрипсин – используются в хирургическойпрактике при гнойных заболеваниях для гидролиза бактериальных белков.
Энзимопатия у детей и важность их биохимической диагностики (на примере нарушения азотистого и углеводного обмена).
Наиболее распространённый вариант энзимопатий, приводящий к развитию гемолитической анемии - недостаточность глюкозо6фосфат дегидрогеназы. Рассмотрим причины энзимопатий у детей. Заболевание широко распространено среди афроамериканцев (630%), меньше - среди татар (3,3%), народностей Дагестана (511,3%); в русской популяции выявляют редко (0,4%). Частный случай недостаточности глюкозо6фосфат дегидрогеназы - фавизм. Гемолиз развивается при употреблении в пищу конских бобов, фасоли, гороха, вдыхании нафталиновой пыли.
Причины энзимопатий у детей Наследование недостаточности глюкозо6фосфат дегидрогеназы (N), в силу чего чаще болеют мужчины. В мире насчитывают около 400 млн носителей этого патологического гена. Заболевание развивается, как правило, после приёма определённых лекарственных средств [производные нитрофурана, хинин, изониазид, фтивазид, аминосалициловая кислота (натрия парааминосалицилат), налидиксовая кислота, сульфаниламиды и др.] или на фоне инфекции.
Энзимопатии у детей – признаки.
Заболевание проявляется бурным развитием гемолиза при употреблении перечисленных выше веществ или инфекциях (особенно при пневмониях, брюшном тифе, гепатите). Недостаточность глкжозо6фосфат дегидрогеназы может быть причиной желтухи новорождённых. В анализе крови выявляют ретикулоцитоз, повышение уровня прямого и непрямого билирубина, ЛДГ, щелочной фосфатазы.
Морфология эритроцитов и эритроцитарные индексы не изменены. Диагноз устанавливают на основании результатов определения активности фермента.
Энзимопатии у детей – лечение.
Вне криза лечение не проводят. При лихорадке применяют физические методы охлаждения. При хроническом гемолизе назначают фолиевую кислоту 1 мт/сут по 3 нед каждые 3 мес. При кризе отменяют все лекарственные средства, проводят инфузионную терапию на фоне дегидратации.
Витамины, классификация витаминов (по растворимость и функциональная). История открытия и изучения витаминов.
Витамины - низкомолекулярные органические соединения различной химической природы и различного строения, синтезируемые главным образом растениями, частично - микроорганизмами.
Для человека витамины - незаменимые пищевые факторы. Витамины участвуют во множестве биохимических реакций, выполняя каталитическую функцию в составе активных центров большого количества разнообразных ферментов либо выступая информационными регуляторными посредниками, выполняя сигнальные функции экзогенных прогормонов и гормонов. По химическому строению и физико-химическим свойствам (в частности, по растворимости) витамины делят на 2 группы.
Водорастворимые:
- Витамин В1 (тиамин);
- Витамин В2 (рибофлавин);
- Витамин РР (никотиновая кислота, никотинамид, витамин В3);
- Пантотеновая кислота (витамин В5);
- Витамин В6 (пиридоксин);
- Биотин (витамин Н);
- Фолиевая кислота (витамин Вс, В9);
- Витамин В12 (кобаламин);
- Витамин С (аскорбиновая кислота);
- Витамин Р (биофлавоноиды).
 2015-04-30
2015-04-30 41482
41482