n - бас квант саны, орбитальдағы электронның энергиясын және орбитальдың көлемін көрсетеді, күрделі атомдарда электрон орналасқан қабаттың реттік нөмірін көрсетеді. n=1; 2; 3; 4; - бүтін сандар. Квант қабаты K, L, M, N, O, P, Q деп белгіленеді.
| l - орбиталь квант саны, электрон бұлтының пішінін сипаттайды l=0, 1, 2, 3... n-1. l- дің бұл мәндеріне s, p, d, f деп белгіленетін орбиталь-дар сәйкес. s - шар тәріздес, p - гантель; d - күрделі гантель; m - магнит квант саны - бұл сан орбиталды квант санына тәуелді, бір пішіндес орбитальдардың жалпы санын және олардың кеңістікте орналасуын көрсетеді. |
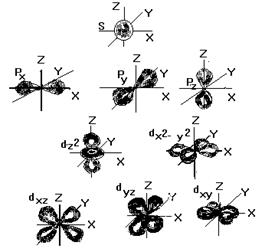
2.1-cурет
m = - l (+l
m - атом орбитальдарының қай жаққа бейімделіп созылуының бағытын білдіреді, сондықтан (+) немесе (-) белгісі болады. Бұл үш квант саны Шредингер теңдеуінен шықты. Ал кейін спектрдегі сызық өте күшті магнит өрісінде екіге жіктелетіні анықталды. БҒл құбылыс электронның төртінші квант саны s- пен сипатталатын жағдайын көрсетті. ms - спин квант саны. Мәні + 1/2 және -1/2; Электронның осінің айналасындағы қозғалысын сипаттайды. Квант сандары квант қабаттарындағы электрондардың санын және ықтималды орындарын сипаттайды.
Төртінші квант қабатында n=4; l=0,1,2,3. Ал магнит квант санының мәндері: 0; (1; (2; (3, демек орбитальдар 4f деп аталады. 4S, 4P, 4d орбитальдарында сәйкесінше 2, 6, 10 электрон, ал 4f орбитальда 14 электрон болады. Сонымен, 4-ші кванттық қабаттағы электрондардың максимал саны 2n2 формуласы бойынша 32-ге тең.
Дәл осылай бесінші, алтыншы, жетінші квант қабаттарындағы электрондардың max саны анықталады. Бірақ жалпы химия деңгейінде 4f деген орбитальдан әрі қарай қарастырылмайды.
Сонымен квант қабаттарындағы электрондар саны 2n2 деген формуламен анықталады.
S- орбитальда электрондардың мүмкін болатын максимал саны 2-ге тең.
Үш Р-орбитальда - 6-ға тең
Бес d - орбитальда - 10-ға тең
11. Квант қабаттарының электрондармен толтырылуы
 2015-05-20
2015-05-20 8775
8775