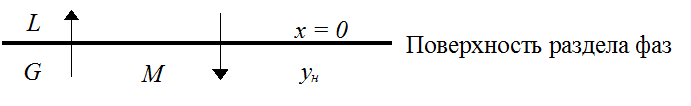
L – первая фаза;
G – вторая фаза;
М – распределяемое вещество;
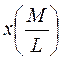 - относительная концентрация вещества М в первой фазе;
- относительная концентрация вещества М в первой фазе;
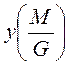 - относительная концентрация вещества М во второй фазе.
- относительная концентрация вещества М во второй фазе.
Если распределяемое вещество М вначале содержится только в фазе G, топри взаимодействии с фазой L начинается перенос (переход) вещества М из фазы G в фазу L, при этом концентрация у уменьшается, а концентрация х увеличивается. С течением времени скорость прямого переноса снижается, а обратного увеличивается; когда скорости прямого и обратного переноса становятся равными, наступает равновесие (концентрации перестают изменяться после достижения равновесия).
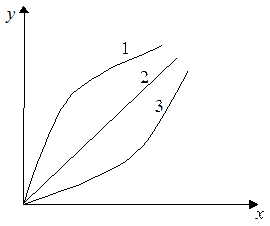 1,2,3 – равновесные линии; x, y – концентрация вещества в фазах, L и G. 1,2,3 – равновесные линии; x, y – концентрация вещества в фазах, L и G. | Данные по равновесию получают экспериментальным путем или рассчитывают для идеальных смесей (например, по закону Рауля, Генри). Эти данные необходимы для расчета массообменного оборудования. Диффузионный процесс идет до достижения равновесия. |
Равновесная кривая обязательно проходит через начало координат. Ее уравнение: 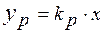 ,
,
где 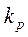 - константа равновесия, если равновесная линия прямая, то
- константа равновесия, если равновесная линия прямая, то 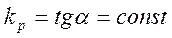 ,
,
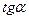 - тангенс угла наклона равновесной линии.
- тангенс угла наклона равновесной линии.
Величина 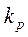 зависит от температуры и давления:
зависит от температуры и давления: 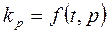 .
.
В жидкости р на 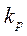 не влияет, т.к. жидкости несжимаемы.
не влияет, т.к. жидкости несжимаемы.
Процесс идет в сторону достижения равновесия.
При расчете иногда кривую равновесия делят на отрезки и заменяют ломаной линией.
 2015-05-12
2015-05-12 765
765







