Рассмотрим наиболее используемые в пирометаллургии двойные и тройные диаграммы.
Система FeO - SiO2. В диаграмме (рисунок 5.1) можно отметить образование устойчивого химического соединения – Fe2SiO4 (2FeO·SiO2) - фаялита - с температурой плавления 1240 °С, и одно неустойчивое соединение со скрытым максимумом FeO·SiO2 – грюнерит с температурой разложения 1160°С. В системе образуется 2 эвтектики с температурами 1220 и 1130 °С. В области SiO2 имеется область расслаивания. Точка плавления FeO 1370 °С. Наиболее легкоплавкая эвтектика (Тпл=1130 °С) образована бисиликатом и моносиликатом оксида железа (Fe2+) и содержит 41,5% SiO2. В части диаграммы, примыкающей к SiО2, в расплавленном состоянии образуются нерастворимые жидкости.
Теперь с точки зрения ионной структуры расплавленных шлаков разберем кристаллизацию в системе FeO-SiO2. Возьмем сплав, соответствующий по составу точке 1. В расплавленном состоянии в шлаке присутствуют ионы Fe2+, O-2, SiO4-4. Выделение в твердую фазу растворенного вещества происходит после достижения произведение растворимости: Lp = (A-) · (K+). Как только температурная прямая пересечёт линию ликвидус, достигается произведение растворимости FeO и начинается его кристаллизация. С понижением температуры Lр уменьшается, поэтому дальнейшая кристаллизация возможна и при понижении концентрации катионов Fe2+ и анионов O-2 в расплаве. Одновременно с обеднением по Fe2+ и O-2 расплав обогащается по SiO4-4. При понижении температуры до значений соответствующих плавлению эвтектики из раствора будут кристаллизоваться одновременно и FeO и Fe2SiO4. При составах сплавов, соответствующих точкам эвтектики и химическому соединению (точки 2 и 3 на графике) кристаллизация будет происходить при постоянной температуре при температуре эвтектики (1220 °С) для эвтектического сплава, и при температуре плавления химического соединения (1240 °С) для расплава соответствующего состава.
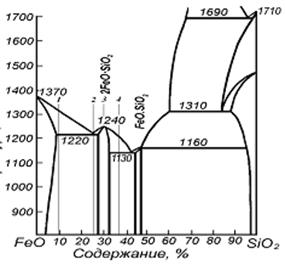 | 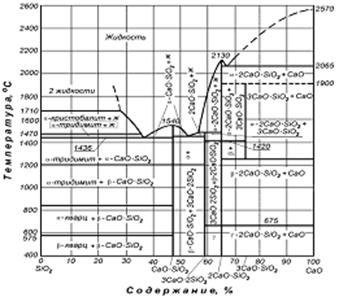 |
| Рисунок 5.1 – Диаграмма состояния системы FeO-SiO2 | Рисунок 5.2 – Диаграмма состояния системы CaO-SiО2 |
В практике цветной металлургии требуются температуры плавления шлаков 1050-1100°С. Основные шлаковые компоненты имеют высокие температуры плавления: ТплFeO = 1370 °C; ТплSiO2 = 1710 °C; ТплCaO = 2570 °C; ТплMgO = 2800 °C; ТплAl2O3 = 2052 °C. Однако уже в двойных сплавах образуется несколько эвтектик. В системе FeO - SiO2 эвтектики плавятся при 1130-1220 °С.
Диаграмма состояния системы CaO – SiO2. Температура плавления SiOa и СаО равна соответственно 1710 и 2570 °С. В этой системе (рисунок 5.2) образуются два прочных химических соединения: CaO-SiО2 — бисиликат (Тпл=1540 °С) и 2CaO-SiО2 — моносиликат оксида кальция (Тпл=2130 °С). Образуется два неустойчивых химических соединения; 3CaO·2SiO2 и 3CaO·SiO2. Одноиз них разлагается при температуре 1470 °С с образованием моносиликата и жидкой фазы, а другое соединение устойчиво в области температур 1250—1900 °С.
По характеру максимума кривой ликвидуса (по сингулярным точкам) можно судить о степени прочности (степени диссоциации) того или иного химического соединения при расплавлении. Сравнивая положение линий ликвидус около химических соединений CaO·SiО2 и 2СаО·SiO2, можно прийти к выводу, что моносиликат прочнее бисиликата.
Температуры плавления эвтектик, которые образуются между соседними химическими соединениями в этой системе, равны 2065, 1470 и 1436 °С.
Горизонтальные линии, примыкающие к СаО, относятся к температурам превращения в твердом состоянии и отображают температуры полиморфных превращений химических соединений в твёрдом состоянии. Например, линия при температуре 575 °С относится к полиморфному переходу β-кварца в α-кварц, а линия при 870 °С – к переходу α-кварца в тридимит.
Диаграммы состояния систем CaO – Al2O3 и SiO2 - Al2O3. В системе CaO – Al2O3 (рисунок 5.3) температура плавления сплава может достигать 1395-1400 °С при температуре плавления оксидов 2570 и 2070 °С, а в системе SiO2 - Al2O3 (рисунок 5.4) – 1545 °С.
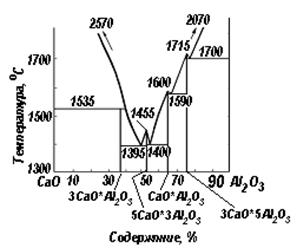 | 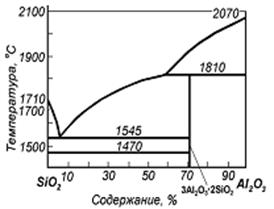 |
| Рисунок 5.3 – Диаграмма состояния системы CaO – Al2O3 | Рисунок 5.4 – Диаграмма состояния системы SiO2 – Al2O3 |
Диаграммы состояния систем PbO – SiO2 и SiO2 – ZnO. Большое значение для понимания и прогнозирования процессов окислительного и агломерирующего обжига свинцовых и цинковых концентратов имеет поведение оксидов свинца, цинка и кремния (рисунок 5.5 и 5.6).
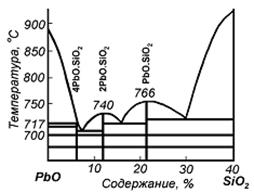 | 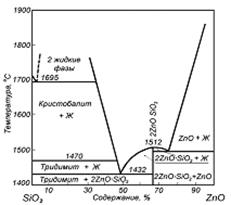 |
| Рисунок 5.5 – Диаграмма состояния системы PbO-SiO2 | Рисунок 5.6 – Диаграмма состояния системы ZnO-SiO2 |
Диаграммы состояния системы CaO-SiO2-Al2O3. Более полные сведения о свойствах шлаков можно получить на основании анализа тройных диаграмм плавкости. Тройные диаграммы позволяют:
· Определять температуру плавления и затвердевания тройного сплава заданного состава, учитывая при этом момент начала кристаллизации и состав выпадающей твердой фазы, момент окончания затвердевания расплава и состав тройной эвтектики.
· Подбирать состав тройного сплава, отвечающий заданной температуре плавления (и вязкости при наличии на диаграммах кривых постоянной вязкости при постоянной температуре) в данной области диаграммы.
· Составлять диаграммы псевдобинарных систем путем проведения вертикальных разрезов и нанесение на них линий пересечения секущей плоскости с поверхностью ликвидуса тройной системы.
· Определить графически процентное содержание двух тройных сплавов в их смеси, необходимое для получения другого тройного сплава заданного состава, пользуясь правилом рычага.
Можно решать и обратные задачи.
Условно делят шлаки на шлаки чёрной и цветной металлургии. К первым относятся шлаки, свойства которых в основном определяются взаимодействиями в системе CaO-SiO2-Al2O3 (рисунок 5.7). Ко второй - систему CaO-SiO2–FeO.
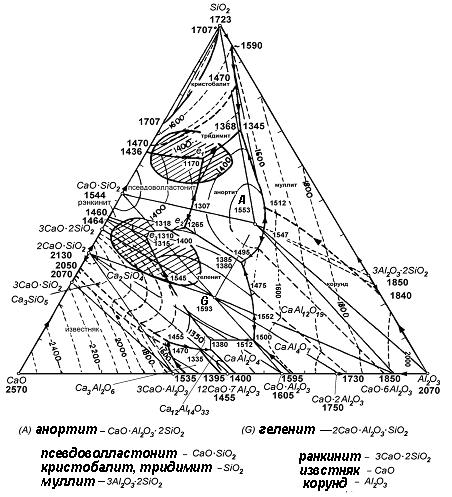 |
| Рисунок 5.7 – Диаграмма состояния системы CaO-SiO2-Al2O3 |
Тройная система CaO-SiO2-Al2O3 в настоящее время является одной из наиболее изученных. На диаграмме отмечены двойные и тройные химические соединения, образующиеся в системе. В этой тройной системе образуется 2 тройных химических соединения: CaO∙Al2O3∙2SiO2 - анортит и 2CaO∙Al2O3∙SiO2 - геленит. Если соединение устойчивое – на диаграмме показана температура его плавления. Неустойчивые соединения – без обозначения температур их разложения. На диаграмме изображены линии двойных эвтектик, точки тройных эвтектик, а также ряд изотерм – геометрических мест точек составов шлаков, имеющих одинаковую температуру плавления.Между отдельными химическими соединениями образуется целый ряд тройных эвтектик со сравнительно низкими температурами плавления (1170, 1265, 1310 º С).
Диаграмма состояния системы CaO - SiO2 – FeO. Диаграмма FeO–SiO2–CaO до сих пор не полностью изучена. Это связано с тем, что в шлаках железо может присутствовать как в двухковалентной, так и в трехвалентной форме.
На диаграмме (рисунок 5.8) приведены изотермы плавкости.
В системе образуется эвтектика с температурой плавления 1030 ºС, состоящей из 25% CaO∙SiO2 и 75% FeO∙SiO2. В системе имеется целая область составов, имеющих температуру плавления 1150 ºС и ниже. Это позволяет в широких пределах варьировать составом шлаков. Часто при расчете шлака не учитывают амфотерный оксид Al2O3, а просто следят за его предельным содержанием. В такой же роли выступает и ZnO.
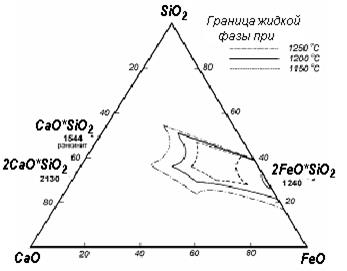 |
| Рисунок 5.8 - Диаграмма состояния системы CaO - SiO2 – FeO |
 2015-05-12
2015-05-12 10097
10097
