Все, что мы с вами рассматривали о кристаллизации двойных сплавов, справедливо и для шлаковых систем. Для различных шлаков различны интервалы замерзания, поэтому трудно определить температуру замерзания.
Возьмем шлак, содержащий различные оксиды SiO2, CaO, FeO, MgO и т.д. Будем бесконечно медленно охлаждать жидкотекучий шлак. С понижением температуры подвижность катионов и анионов падает. Простые анионы вновь соединяются в огромные комплексные анионы, а катионы собираются около кремнезема, образуя по мере понижения температуры недиссоциированные молекулы. С дальнейшим понижением температуры проходят процесс агрегации молекул во все более крупные аморфные комплексы.
При дальнейшем охлаждении образуются первичные кристаллы, выделяется тепло кристаллизации.
Кристаллизация шлака начинается с того соединения, для которого в первую очередь будет достигнуто произведение растворимости - Lp.
В первую очередь из шлака будет кристаллизоваться MgSiO3. Однако, полное выделение магния в кристаллическую структуру, согласно закону действия масс, невозможно. Любое вещество обладает определенной растворимостью в жидкости, обязательно будет сохраняться равновесие:
Mg2SiO4тв = Mg2SiO4ж = 2Mg+2 + SiO4-4
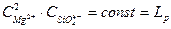 - произведение растворимости при постоянной температуре.
- произведение растворимости при постоянной температуре.
Произведение растворимости зависит от температуры. С понижением температуры Lp понижается, но никогда не равно 0. при понижении температуры будет понижаться концентрация кристаллизующегося катиона (в нашем случае Mg2+), а концентрация катиона Ca2+ (для примера) изменяться не будет. В конечном счете мы достигаем LpCa2SiO4, и силикат кальция будет выделятся в твердую фазу.
Ca2SiO4тв = Ca2SiO4ж = 2Ca2+ + SiO4-4
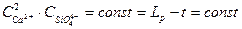
Начиная с этой точки происходи кристаллизация одновременно двух соединений Ca2SiO4 и Mg2SiO4.
По мере вывода из раствора катионов Ca2+ и Mg2+ раствор обогащается Al2O3, FeO, Cr2O3 и прочими присутствующими в шлаке оксидами. В конечном счете, начинает происходить выпадение соединений типа CaO ∙ MgO, Al2O3 ∙ SiO2, CaO∙FeO∙ Al2O3.
Более низкими значениями произведений растворимости обладают наиболее тугоплавкие оксиды. Поэтому, все рассуждения о порядке кристаллизации можно вести с точки зрения температур плавления.
Однако могут наблюдаться и отклонения от того порядка выделения соединений.
Имеем Mg2SiO4 и Ca2SiO4 Lp Ca2SiO4 > Lp Mg2SiO4
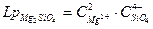
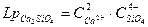
Ca2SiO4 будет кристаллизоваться в первую очередь, в случае если будет для него в первую очередь достигнуто Lp, а это может быть в случае, если в шлаке большая концентрация катионов Ca2+, гораздо больше концентрация Mg2+.
Для затвердевших шлаков характерны несколько видов структур, в зависимости от скорости охлаждения.
1. Стекловидные шлаки - кристаллизация не произошла и шлаки застыли в беспорядочной форме. Если быстро происходит охлаждение шлаков, то в связи с быстро увеличивающейся вязкостью шлака застывающая масса не успевает сориентироваться из-за малой диффузионной способности. Стекловидным можно получить любой шлак. Кислые шлаки дают большие массы в форме стекла.
2. Форфоровидные.
3. Камневидные.
4. Аморфные.
Потери металлов в шлаке. Величина потерь металла в шлаке зависит от состава и температуры шлака, характера процессов плавления шихты и разделения жидких фаз. Существуют три вида потерь металла в шлаках:
1. Химические потери. Шлаковая фаза содержит в растворе оксиды извлекаемого металла.
2. Физические потери. Шлак содержит в себе растворенные металлы или сульфиды (при плавках на штейн).
3. Механические потери. Шлаковая фаза может механически увлекать с собой не отделившиеся капельки другой, ценной фазы (металла или штейна) и выносит их с собой из плавильного агрегата в отвал.
Химические потери возникают в результате не завершённости основных реакций. При восстановительной плавке это: MeO + C = Me + CO (CO2) и MeO + Me1 = Me1O + Me; при плавке на штейн: MeO + FeS' (CaS) = MeS + FeO (CaO).
Значительное содержание оксида извлекаемого металла в шлаке свидетельствует о серьезных нарушениях технологии и условий плавки: недостатке восстановителя или сульфидизатора; очень быстром проведении процесса, когда время протекания основных реакций сокращено.
К химическим потерям приводит окисление металла шлаком: (Me1O)шл+[Me]=(MeO)шл+[Me1]
Физические потери возникают в результате растворимости сульфидов и металлов в шлаке, и их величина зависит от состава шлака и всегда повышается с повышением температуры шлака. При охлаждении и затвердевании шлака эти сульфиды выпадают в форме самостоятельной сульфидной фазы, диспергированной в массе шлака. Снижение потерь от растворения в шлаке сульфидов достигается работой на кислые и маложелезистые шлаки, при возможно более низкой температуре.
Механические потери, т.е. потери вследствие незавершенности процесса отстаивания более тяжелой ценной фазы от шлака, зависит от соотношения плотностей разделяемых фаз, вязкости шлаковой фазы и продолжительности процесса отстаивания. Механические потери редко наблюдаются при плавках на металл, т.к. большое различие в плотностях, что не препятствует ликвации. При плавках на штейн механические потери – основной вид потерь.
 2015-05-12
2015-05-12 1617
1617








