РАСЧЕТЫ ПРИ ПРИГОТОВЛЕНИИ РАСТВОРОВ И
ОПРЕДЕЛЕНИИ РЕЗУЛЬТАТОВ ТИТРИМЕТРИЧЕСКОГО
АНАЛИЗА
Методические указания и варианты контрольных заданий
к самостоятельной работе студентов по дисциплине
«Аналитическая химия» для студентов ХТФ направления
550800– «Химическая технология и биотехнология»
Томск 2007
 |
УДК 543
Дубова Н.М. Аналитическая химия. Расчеты при приготовлении растворов и определении результатов титриметрического анализа.Методические указания и варианты контрольных заданий к самостоятельной работе студентов ХТФ направления 550800. – Томск: Изд-во ТПУ, 2007. – 24 с.
Составитель доц., к.х.н. H.M.Дубова
Рецензент
доц., к.х.н. кафедры ФАХ Е.И.Короткова
Методические указания рассмотрены и рекомендованы к изданию методическим семинаром кафедры физической и аналитической химии № 1 от 1 сентября 2007г.
Зав. кафедрой ФАХ_____________ _ _____ А. А. Бакибаев
Одобрено учебно-методической комиссией ХТФ
Председатель учебно-методической комиссии
Н.В.Ушева
 | |||||||
 | |||||||
 | |||||||
 |
РАСЧЕТЫ ПРИ ПРИГОТОВЛЕНИИ РАСТВОРОВ И
ОПРЕДЕЛЕНИИ РЕЗУЛЬТАТОВ АНАЛИЗА
Если вещество удовлетворяет требованиям, предъявляемым к стандартным или исходным веществам, то из него можно приготовить рабочий раствор с точно известной концентрацией путем растворения точной навески вещества (m) в мерной колбе (V).
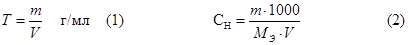
В случае, когда вещество не удовлетворяет требованиям, предъявляемым к стандартным веществам, готовят рабочий раствор приблизительной концентрации, а точную концентрацию устанавливают по стандартному веществу, используя метод пипетирования или метод отдельных навесок (формулы 3;5)
a) метод пипетирования
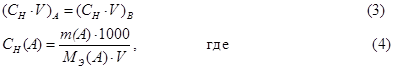
СН(А), СН(В) – молярные концентрации эквивалентов стандартного (А) и рабочего (В) растворов;
V(A), V(B) – объемы стандартного и рабочего растворов при титровании;
m(A) – навеска стандартного вещества (А);
Мэ(А) – молярная масса эквивалента вещества (А)
b) 
метод отдельных навесок
При приготовлении растворов (например, кислот и оснований) используется разбавление.
Пример 1.
Сколько миллилитров конц. H2SO4 (ρ=1,49 г/см3), содержащей 60% H2SO4, нужно взять для приготовления 500 мл 0,1 н. раствора?
Решение:
1. Вычислим молярную концентрацию эквивалента концентрированной H2SO4:
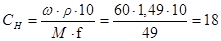 н
н
2. Если раствор разбавлять, то его объем и концентрация будут изменяться, но общее количество эквивалентов растворенного вещества останется постоянным. Поэтому при разбавлении, как и при титровании, справедливо равенство: 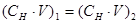 . Применяя его к рассматриваемому случаю, получим:
. Применяя его к рассматриваемому случаю, получим: 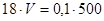 , откуда Vконц (H2SO4)=3 мл.
, откуда Vконц (H2SO4)=3 мл.
Пример 2.
Рассчитать, какой объем 3 н H2SO4 следует прибавить к 1 л 0,6 н H2SO4, чтобы получить 1,5 н раствор?
Решение:
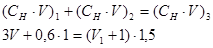
Решив полученное уравнение, получим V =600 мл.
 2015-05-13
2015-05-13 1240
1240







