Гидролиз солей – реакция взаимодействия солей приводящая к нарушению равновесия электролитической диссоциации воды и изменению рН раствора.
Физический смысл – в результате гидролиза образуются слабо диссоциированные частицы (ионы или молекулы), поэтому гидролизу подвергаются катионы слабых оснований и анионы слабых кислот.
Не подвергаются гидролизу соли, образованные сильным основанием и сильной кислотой и нерастворимые соли. Процесс гидролиза обратимый.
Если в состав соли входит только один слабый ион (катион или анион), то гидролиз идет ступенчато, где количество ступеней соответствует численно заряду слабого иона.
1. Гидролиз по аниону, соль образована сильным основанием и слабой кислотой, продуктом гидролиза будет кислая соль и сильное основание.
CO32− + HOH⇆HCO3− + OH− pH > 7
Na2CO3 + НОН⇆NaHCO3 + NaOH
2. Гидролиз по катиону, соль образована сильной кислотой и слабым основанием, продуктом гидролиза будет основная соль и сильная кислота.
2Fe+3 + 2НОН⇆FeOH2+ + 2H+ рН<7
Fe2(SO4)3 + 2НОН⇆2FeOHSO4 + H2SO4
3. Гидролиз по катиону и аниону, соль образована слабым основанием и слабой кислотой, гидролиз идет по разному. Чем больше К дис, тем сильнее соль подвергается гидролизу.
1) если соль растворима, гидролиз идет ступенчато по 1-й ступени:
NH4+ + CN− + НОН⇆NH4ОН + НCN рН>7
NH4CN + НОН⇆NH4ОН + НCN
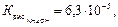
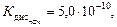 т.е. основание диссоциирует сильнее, чем кислота, раствор насыщается частично ионами ОН−, среда слабощелочная.
т.е. основание диссоциирует сильнее, чем кислота, раствор насыщается частично ионами ОН−, среда слабощелочная.
NH4+ + NO2− + НОН⇆NH4ОН + НNO2 рН<7
NH4NO2 + НОН⇆NH4ОН + НNO2
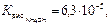
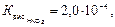 т.е. кислота диссоциирует сильнее, чем основание, раствор насыщается частично ионами Н+, среда слабокислая.
т.е. кислота диссоциирует сильнее, чем основание, раствор насыщается частично ионами Н+, среда слабокислая.
NH4+ + CH3COO− + НОН⇆NH4ОН + CH3COOН рН» 7
NH4CH3COO + НОН⇆NH4ОН + CH3COOН
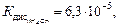
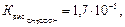 среда близка к нейтральной, т.к. соль образована слабой кислотой и слабым основанием одинаковой силы.
среда близка к нейтральной, т.к. соль образована слабой кислотой и слабым основанием одинаковой силы.
2) если соль разлагается водой, гидролиз идет до конца:
AI2S3 + 6НОН⇆2AI(OH)3¯ + 3H2S
 2015-05-13
2015-05-13 1300
1300
