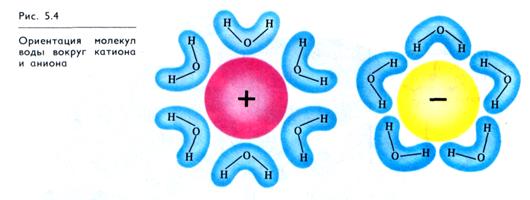
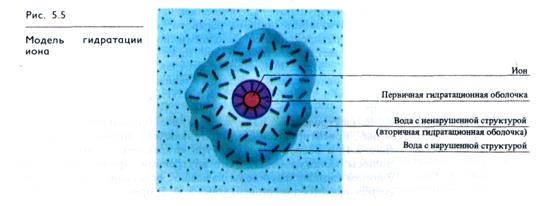
В состоянии первичной гидратации молекулы воды имеют сниженную подвижность и находятся в обменном равновесии с ближайшими молекулами. А молекулы вторичной гидратной оболочки, сохраняя подвижность, под поляризующим влиянием иона стремятся к некоторой упорядоченности, что нарушает исходную структуру воды. С наружной стороны этого слоя вода сохраняет неизменную структуру.
Воду, связанную с ионами, называют также осмотически связанной. Она является важной составляющей осмотического давления в клетках растений.
По мере повышения концентрации раствора (до 1,5 — 2 моль/л) вторичные гидратные оболочки ионов перекрываются и вода с собственной структурой перестает существовать: наблюдается переход от структуры чистой воды к структуре кристаллогидрата. Чем больше ионов в растворе, тем больше нарушена структура воды и, следовательно, тем меньше энергии необходимо для разрушения оставшихся водородных свя зей и повышения температуры раствора. На рис. 5.6 представлена зависимость теплоемкости водного раствора от концентрации растворенного электролита (КВг). При повышении концентрации КВг теплоемкость воды снижается из-за дезорганизации системы водородных связей в структуре воды. Эти данные позволяют понять природу высокой теплоемкости воды и характер влияния на эту теплоемкость растворенных в воде веществ.
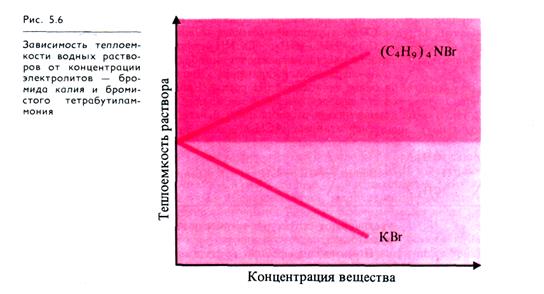
Влияние гидрофобных радикалов на структуру воды. При растворении в воде вещества с большим гидрофобным радикалом, например тетрабутиламмонийбромида (С4H9)4NBr, и с увеличением его концентрации в растворе теплоемкость раствора повышается (рис. 5.6). Это объясняется тем, что неполярные молекулы увеличивают степень структурной организации воды. Вокруг них образуются кристаллогидраты с пентагональными ячейками. Например, (С4H9)4NBr образует, кристаллогидрат, масса которого на 90% состоит из кристаллической воды. Вода в этом кристалле имеет высокую теплоемкость: кристалл плавится не при 0°С, как лед, а при 30 °С. Возникновение кристаллогидратов можно наблюдать в производственных условиях в газопроводах. Описаны случаи закупорки льдом труб газопровода при 20°С (образование кристаллогидрата около молекул метана), а также замерзания зерна и повреждения посевов от появления льда в тканях при 4,5°С (образование кристаллогидратов около неполярных радикалов макромолекул белков).
Растворы белков. В белках гидратация обусловлена взаимодействием молекул воды с гидрофильными (ионными и электронейтральными) и гидрофобными (неполярными) группами и ее иммобилизацией в замкнутых пространствах внутри макромолекул при их конформанионных перестройках.
При гидратации ионной (взаимодействие с — NH+3,
— COO--группами) и электронейтральной (с —СООН, —ОН,
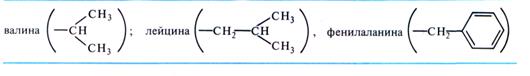
— СО, -NH, -NH2, -СОNН2-группами) молекулы воды электростатически связываются и образуется мономолекулярный слой первичной гидратации. Число ионизированных групп в белке зависит от рН среды. Наименее гидратирован белок в его изоэлектрической точке, при которой отмечается также самая низкая растворимость белков. Гидрофобные группы, например аланина (—СН3), увеличивают структурированность воды в этих участках молекулы белка.
 Помимо гидрофобных групп в молекулах белков, на структурированность воды влияет гидрофобная липидная фаза мембран.
Помимо гидрофобных групп в молекулах белков, на структурированность воды влияет гидрофобная липидная фаза мембран.
Иммобилизованная вода, оказавшаяся замкнутой внутри макромолекул, может участвовать в образовании слоя первичной гидратации, а остальная ее часть сохраняет свойства обычной воды, но с ограниченной подвижностью.
Растворимость белков в воде варьирует в широких пределах. Определенной зависимости между гидратацией и растворимостью белков не наблюдается. Например, сухой коллаген способен связать гораздо больше воды, чем сухой сывороточный альбумин. Однако коллаген нерастворим в воде, а альбумин растворяется в ней легко. На возможность гидратации белков за счет пептидных связей указывает тот факт, что искусственный полипептид нейлон, не содержащий боковых ио-ногенных цепей и гидрофильных групп, способен связывать воду.
Таким образом, макромолекулы оказывают разнообразное влияние на окружающую воду. В зависимости от физико-химических свойств (наличие полярных, неполярных, ионизированных групп), конформационного состояния и внешних условий (рН, ионный состав) может наблюдаться большее или меньшее связывание воды и образование стабильной льдопо-добной структуры.
Содержание воды в растительных тканях представляет собой исключительно изменчивую и динамическую величину. Оно сильно различается у разных видов, в различных частях растений, претерпевая сезонные и суточные изменения в одних и тех же тканях. Изменения обусловливаются возрастом ткани, доступностью почвенной влаги и соотношением поглощения воды и транспирации.
В клетках и тканях различают две формы воды — свободную и связанную. Связанная вода подразделяется на: а) связанную осмотически (гидратирует растворенные вещества — ионы, молекулы); б) коллоидно связанную, которая включает интрамицеллярную воду, находящуюся внутри коллоидной системы (в том числе и иммобилизированную воду), и интермицелляр-ную воду (находится на поверхности коллоидов и между ними); в) капиллярно связанную (находится в клеточных стенках и сосудах проводящей системы).
Свободная вода обладает достаточной подвижностью. Если внести тяжелую воду (H182O) в среду, омывающую корни растений, то через 1 — 10 мин процент тяжелой воды будет одинаков как во внешней среде, так и во внутренних тканях корня. Таким образом, проницаемость плазмалеммы клеток корней для воды достаточно высока. В молодых корнях пшеницы около 3/4 всей внутриклеточной воды содержится в вакуолях, 1/4 в оболочках клеток и только 1/20 в цитоплазме. Но в клетках меристем, имеющих лишь малочисленные мелкие вакуоли и гонкие клеточные оболочки, основная масса воды заключена в цитоплазме.
Вода удерживается в клетках за счет осмоса и набухания биоколлоидов. Даже при содержании влаги ниже критического уровня большие количества воды удерживаются частицами гидратированных коллоидов, а также связываются гидра-тированными ионами и молекулами. Доля всей внутриклеточной воды, находящейся в связанном состоянии, очень изменчива и зависит от вида, местоположения и части растения, от общего содержания воды в растительной ткани.
Клеточные стенки обладают значительной гигроскопичностью и удерживают воду в основном в силу высокой гидрофильности их пектиновых и целлюлозных компонентов. Они содержат две фракции воды: подвижную и малоподвижную. Вода, находящаяся в микрокапиллярных пространствах, и та, которая удерживается водородными связями на микрофибриллах целлюлозы, считается малоподвижной, тогда как значительные количества воды в крупных капиллярных пространствах между микрофибриллами целлюлозы легко перемещаются. Содержание влаги в клеточных стенках тургесцентных клеток превышает 50% (например, в колеоптилях овса). Передвижение воды вне проводящих пучков происходит главным образом по клеточным стенкам, причем массовый ток воды по ним можно вызвать с помощью приложенного извне гидростатического давления.
По сравнению с клеточными стенками цитоплазма содержит больше воды: ее содержание может достигать 95 % от массы цитоплазмы. Основной вид гидрофильных коллоидов в цитоплазме — белки. Внутри белковых структур заключено значительное количество воды. На расстояниях до 1 мкм от поверхности белка эта вода прочно связана и в гидрофобных зонах имеет структуру, близкую к структуре льда. Цитоплазма содержит также сахара, соли, липиды и другие соединения, которые оказывают влияние на состояние содержащейся в ней воды.
Пластиды, митохондрии и ядра отделены от цитоплазмы собственными мембранами. Их объем изменяется под действием осмотических сил. Содержание воды в хлоропластах обычно меньше, чем в цитоплазме (около 50 %), что связано с присутствием в них большого количества липидов и липофильных веществ, которые могут составлять до 40 % сухой массы хлоропластов. То же самое относится к митохондриям.
 Первое место по концентрации воды в клетке (около 98 %) занимает вакуоль. Вакуолярный сок содержит сахара, органические кислоты и их соли, неорганические катионы (К+ и др.) и анионы (С1-), ферменты, белки и другие азотистые соединения, слизи, таннины, пигменты. Соли, сахара и органические кислоты находятся в растворе, тогда как белки, таннины и слизи составляют гидрофильную коллоидную фракцию вакуолей. Вакуолярный сок можно рассматривать в основном как истинный раствор, удерживающий воду осмотически из-за избирательной проницаемости тонопласта.
Первое место по концентрации воды в клетке (около 98 %) занимает вакуоль. Вакуолярный сок содержит сахара, органические кислоты и их соли, неорганические катионы (К+ и др.) и анионы (С1-), ферменты, белки и другие азотистые соединения, слизи, таннины, пигменты. Соли, сахара и органические кислоты находятся в растворе, тогда как белки, таннины и слизи составляют гидрофильную коллоидную фракцию вакуолей. Вакуолярный сок можно рассматривать в основном как истинный раствор, удерживающий воду осмотически из-за избирательной проницаемости тонопласта.
Поглощение воды из внешней среды — обязательное условие существования любого живого организма. Вода может поступать в клетки растений благодаря набуханию биоколлоидов, увеличению степени их гидратации. Такое поступление воды характерно для сухих семян, помещенных в воду. Однако главным способом поступления воды в живые клетки является ее осмотическое поглощение.
Осмос и его законы. Осмосом называется прохождение рас- творителя в раствор, отделенный от него полупроницаемой мембраной (т. е. пропускающей растворитель, но не молекулы растворенных веществ).
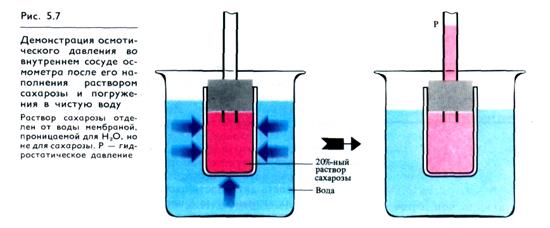
Природу осмоса стали изучать прежде всего биологи. Первый осмометр был сконструирован в 1826 г. французским физиологом Г. Дютроше. Принципэтого осмометра заключался в следующем. Пузырь из полупроницаемой пленки (пергамент, животный пузырь) с помещенной в него стеклянной трубочкой заполнялся раствором сахара или другого органического вещества. После погружения пузыря в чистую воду наблюдался подъем уровня жидкости в трубке. Однако применявшиеся Дютроше пленки не были абсолютно полупроницаемыми и медленно проникавший сахар мешал количественному измерению осмотического давления.
Более совершенная конструкция осмометра была предложена В. Пфеффером. Свой осмометр он назвал «искусственной клеткой». Основой ее служил пористый фарфоровый сосуд. Во внутреннюю полость сосуда наливался раствор желтой кровяной соли K4[Fe(CN)6], и сосуд помещался в раствор CuSO4. При взаимодействии этих веществ в порах фарфорового сосуда образовывалась гелеобразная масса железистосинеродистой меди Cu2[Fe(CN)6], служившая полупроницаемой мембраной. Таким образом одновременно достигались достаточная прочность и полупроницаемость сосуда.
Поступление воды в такого рода осмотическую ячейку (рис. 5.7) приводит к увеличению объема жидкости и поднятию ее уровня в манометрической трубке до тех пор, пока гидростатическое давление Р столба жидкости не повысится настолько, чтобы воспрепятствовать дальнейшему увеличению объема раствора. В достигнутом состоянии равновесия полупроницаемая мембрана в единицу времени пропускает одинаковые количества воды в обоих направлениях. Гидростатическое давление в этом случае соответствует потенциальному осмотическому давлению π*.
Вант-Гофф, использовав в качестве осмотической ячейки «искусственную клетку» и другие модели, показал, что осмотические законы соответствуют газовым законам Бойля — Мариотта. Для расчета потенциального давления он предложил формулу:
π*=i•с•RT, ]
где с — концентрация раствора в молях, Т — абсолютная температура, R — газовая постоянная, i — изотонический коэффициент, равный 1 +α (n— 1), где α — степень электролитической диссоциации, п — число ионов, на которые распадается молекула электролита.
 Таким образом, для разбавленных растворов осмотическое давление при постоянной температуре определяется концентрацией частиц (молекул, ионов) растворенного вещества (числом их в единице объема раствора). Потенциальное осмотическое давление выражается в Паскалях и отражает максимально возможное давление, которое имеет раствор данной концентрации, или максимальную способность раствора в ячейке поглощать воду.
Таким образом, для разбавленных растворов осмотическое давление при постоянной температуре определяется концентрацией частиц (молекул, ионов) растворенного вещества (числом их в единице объема раствора). Потенциальное осмотическое давление выражается в Паскалях и отражает максимально возможное давление, которое имеет раствор данной концентрации, или максимальную способность раствора в ячейке поглощать воду.
В настоящее время, рассматривая осмотические явления, пользуются также понятиями, характеризующими термодинамические особенности системы. Энергетический уровень молекул данного вещества, который выражается в скорости их диффузии, называют химическим потенциалом этого вещества (Ψ). Химический потенциал чистой воды называют водным потенциалом (Ψн2о). Он характеризует способность воды диффундировать, испаряться или поглощаться и выражается в Паскалях. Наивысшая величина водного потенциала — у химически чистой воды. Эта величина условно принята за нуль. Поэтому водный потенциал любого раствора и биологических жидкостей имеет отрицательное значение. Водный потенциал включает компоненту, определяемую присутствием растворенного вещества, называемую осмотическим потенциалом (Ψπ)
и потенциал, связанный с гидростатическим давлением (ΨР).
Если раствор сахарозы в ячейке из полупроницаемого материала (целлофана, коллоидной пленки), пропускающего только воду, погрузить в чистую воду (см. рис. 5.7), то молекулы воды будут перемещаться из чистой воды в раствор сахарозы, где концентрация (активность) воды меньше, т. е. от высокого водного потенциала к более низкому. Поскольку растворенные вещества снижают активность воды в растворе, из ячейки воды выходит меньше, чем входит. Это и приводит к увеличению объема раствора сахарозы и подъему жидкости в трубке осмометра. Для оценки величины осмотического давления нужно измерить давление, которое необходимо приложить к раствору, чтобы преодолеть активность частиц чистого растворителя по сравнению с их активностью в растворе и тем самым уравнять скорость движения молекул воды в двух направлениях. Осмотический потенциал (Ψπ) (раствора в условиях этого равновесия равен по величине потенциалу гидростатического давления Ψр, но противоположен ему по знаку. Ψπ всегда имеет отрицательное значение.
 Растительная клетка окружена клеточной стенкой, которая обладает определенной эластичностью и может растягиваться. Вакуоль содержит большое количество осмотически активных веществ — Сахаров, органических кислот, солей. При изучении осмотических явлений в растительных клетках обычно рассматривается упрощенная модель, в которой полупроницаемой мембраной считается система, состоящая из плазмалеммы и тонопласта одновременно. Поскольку мембрана избирательно проницаема и водалроходит через нее значительно легче, чем вещества, растворенные в клеточном соке и цитоплазме, при помещении клетки в воду последняя по законам осмоса будет поступать внутрь клетки.
Растительная клетка окружена клеточной стенкой, которая обладает определенной эластичностью и может растягиваться. Вакуоль содержит большое количество осмотически активных веществ — Сахаров, органических кислот, солей. При изучении осмотических явлений в растительных клетках обычно рассматривается упрощенная модель, в которой полупроницаемой мембраной считается система, состоящая из плазмалеммы и тонопласта одновременно. Поскольку мембрана избирательно проницаема и водалроходит через нее значительно легче, чем вещества, растворенные в клеточном соке и цитоплазме, при помещении клетки в воду последняя по законам осмоса будет поступать внутрь клетки.
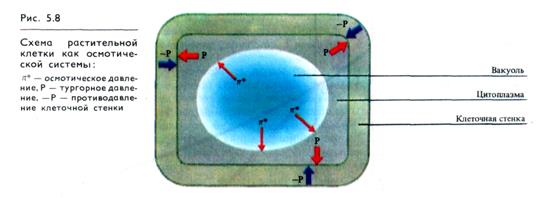
Силу, с которой вода входит в клетку, называют сосущей силой S. Она тождественна водному потенциалу клетки (ΨН2o)-Величина сосущей силы определяется осмотическим давлением клеточного сока (π*) и тургорным (гидростатическим) давлением в клетке (Р), которое равно противодавлению клеточной стенки, возникающему при ее эластическом растяжении (рис. 5.8):
S = π * - Р.
При замене этих обозначений соответствующими термодинамическими величинами уравнение приобретает следующий вид:
ΨН2o=- Ψπ- Ψр
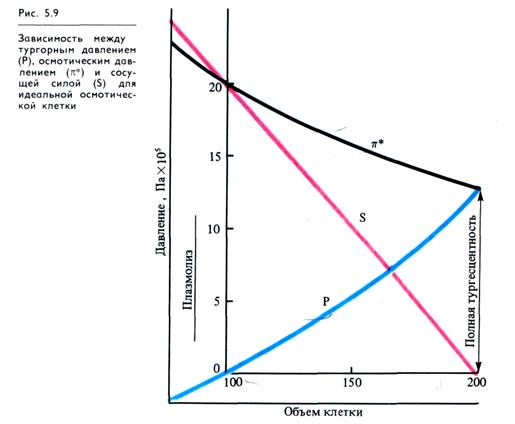
В условиях разной оводненности соотношения между всеми компонентами этого уравнения меняются (рис. 5.9). Когда клетка полностью насыщена водой (полностью тургесцентна), ее сосущая сила равна нулю, а тургорное давление равно потенциальному осмотическому: S = 0; P = π* (рис. 5.9, правая сторона). Состояние полного тургора наблюдается в клетках при достаточной влажности почвы и воздуха. Если подача воды к клетке уменьшается (при усилении ветра, при недостатке влаги в почве и т. д.), то вначале возникает водный дефицит в клеточных стенках, водный потенциал которых становится ниже, чем в вакуолях, и вода начинает перемещаться в клеточные стенки.
Отток воды из вакуоли снижает тургорное давление в клетках и, следовательно, увеличивает их сосущую силу. При длительном недостатке влаги большинство клеток теряет тургор и растение подвядает. В этих условиях Р = 0; S= π* (рис. 5.9, левая cторона).
Явление потери тургора клетками можно наблюдать экспериментально, помещая кусочки тканей в гипертонический раствор. В этом случае отток воды из клеток приводит к уменьшению объема протопластов и их отделению от клеточных стенок (происходит плазмолиз). Пространство между стенкой и сократившимся протопластом заполняет наружный раствор. Клетку в таком состоянии называют плазмолизированной. При помещении этой клетки в чистую воду значения S, π* и Р изменяются так, как представлено на рис. 5.9 слева направо.
В условиях водного дефицита в молодых тканях резкое усиление потери воды, например при суховее, может приводить к тому, что тургорное давление в клетках становится отрицательной величиной и протопласты, сокращаясь в объеме, не отделяются от клеточных стенок, а тянут их вслед за собой. Клетки и ткани сжимаются. Это явление называется циторризом.
Помимо осмотического фактора, поглощение цитоплазмой воды может быть связано с гидратацией белков и других биоколлоидов. При учете воды, поглощаемой клетками в результате процессов гидратации, в уравнение водного потенциала наряду с другими компонентами вводится и потенциал набухания Ψτ
Величина осмотического потенциала неоднозначна у разных видов растений и в разных частях одного и того же растения.
Осмотическая концентрация вакуолярного сока для клеток корней составляет 0,3—1,2 МПа, а для клеток надземных органов—1,0-2,6 МПа. Это обусловливает существование вертикального градиента осмотической концентрации и сосущей силы от корней к листьям. Очень высоко осмотическое давление в клетках галофитов, растущих в условиях засоления: оно достигает 15 МПа.
 Водные растения, как правило, не испытывают недостатка в воде. Вышедшие на сушу растения приспособились к наземному образу жизни благодаря приобретению способности создавать внутри своего тела непрерывный восходящий ток воды. Этот ток начинается на поглощающей воду поверхности корней, пронизывает все растение и заканчивается на испаряющих поверхностях наземных органов, главным образом листьев, причем испарение воды листьями должно быть компенсировано поглощением воды корнями. Таким образом, водообмен у растений складывается из трех этапов: 1) поглощения воды корнями, 2) передвижения ее по сосудам, 3) транспирации, т. е. испарения воды листьями. Каждый из этих этапов в свою очередь состоит из нескольких взаимосвязанных процессов.
Водные растения, как правило, не испытывают недостатка в воде. Вышедшие на сушу растения приспособились к наземному образу жизни благодаря приобретению способности создавать внутри своего тела непрерывный восходящий ток воды. Этот ток начинается на поглощающей воду поверхности корней, пронизывает все растение и заканчивается на испаряющих поверхностях наземных органов, главным образом листьев, причем испарение воды листьями должно быть компенсировано поглощением воды корнями. Таким образом, водообмен у растений складывается из трех этапов: 1) поглощения воды корнями, 2) передвижения ее по сосудам, 3) транспирации, т. е. испарения воды листьями. Каждый из этих этапов в свою очередь состоит из нескольких взаимосвязанных процессов.
Хотя небольшие количества воды могут поглощаться и надземными частями растений, практически вся вода и минеральные соли поступают в организм высших растений через корневую систему из почвы.
Состояние воды в почве. Почва — многофазное тело, состоящее из четырех главных компонентов: твердых минеральных частиц, органического вещества (гумуса), почвенного раствора и почвенного воздуха. Минеральные частицы и гумус образуют почвенную структуру, а вода и воздух заполняют полости этой структуры.
Способность почвы удерживать воду зависит от ее состава и свойств. Относительно крупные кристаллы силикатов (песок) связывают воду в значительной степени. Разнообразные глинистые минералы (алюмосиликаты) и гетерогенные гумусовые вещества, будучи коллоидами, могут удерживать значительные количества гидратационной воды. Такая вода условно называется связанной. Вода, содержащаяся в капиллярах почвы, может условно считаться свободной. Определенное количество воды входит в состав минеральных компонентов почвы. Эта вода химически связана и практически недоступна для растений.
В пределах значений влажности, важных с биологической точки зрения, главную роль играют два механизма удержания воды в почве: 1) за счет сил, действующих на разделе фаз жидкость — воздух, при этом поверхностное натяжение уравновешивает силы, способствующие удалению воды; 2) благодаря силам, действующим на поверхностях раздела жидкой и твердой фаз.
Существуют различные термины, применяемые для обозначения доступности почвенной влаги. При поступлении воды в сухую почву она вначале впитывается очень быстро. Затем скорость просачивания воды в нижние горизонты становится все медленнее. Когда скорость нисходящего движения воды оказывается резко сниженной, влажность почвы достигает уровня, называемого полевой влагоемкостью. Если понятие «полевая влагоемкость» широко применяется для характеристики максимальных размеров запаса почвенной влаги, который может быть использован для роста растений, то влажность устойчивого завядания служит показателем минимальных размеров такого запаса. Под влажностью устойчивого завядания понимают такую влажность почвы, при которой растения остаются увядшими до тех пор, пока в почву не подается вода. Влажность почвы, при которой наступает завядание различных растений, варьирует незначительно. Влажность устойчивого завядания представляет собой нижнюю границу того интервала влажности почвы, в котором возможен рост растений.
Под доступной для растений почвенной влагой понимается то количество воды, которое накапливается в почве от уровня влажности устойчивого завядания до полевой влагоемкости. В среднем легкодоступная для растений влага удерживается в почве силой до 0,5 МПа, среднедоступная — до 1,0—1,2 МПа, а труднодоступная — до 2,5 — 3,0 МПа. Определение доступной почвенной влаги имеет большое практическое значение для выяснения сельскохозяйственной ценности почв, поскольку известно, что в умеренной зоне за вегетационный период растения испаряют больше воды, чем ее выпадает за это время в виде атмосферных осадков. При этом растения используют накопленную с весны доступную почвенную влагу. Вода в почьве передвигается олагодаря разности водных потенциалов между различными частями системы (от более высокого к более низкому потенциалу). По мере иссушения почвы скорость движения воды в ней значительно замедляется.
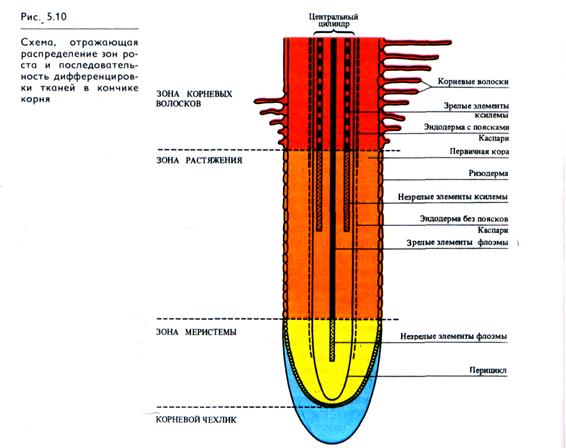
Строение корня. Все особенности морфологии и анатомии корня связаны с необходимостью поглощать воду и минеральные вещества из почвы. В первичном строении корня различают несколько тканей: корневой чехлик, апикальную меристему, ризодерму, первичную кору, эндодерму, перицикл и проводящие ткани, сосредоточенные в центральном цилиндре, или стеле (рис. 5.10). Растущая часть корня обычно не превышает 1 см в длину и состоит из меристемы (1,5 — 2 мм от кончика) и зоны растяжения (2 — 7 мм).
На самом кончике корня находится корневой чехлик, клетки наружных слоев которого секретируют полисахаридную слизь и слущиваются при перемещении корня в почве. Клетки центральной части чехлика (статоциты) содержат много амилопластов, заполненных крахмалом (статолиты) и участвующих в восприятии корнем направления действия силы тяжести. Основными функциями корневого чехлика являются: а) предохранение растущей зоны, в первую очередь апикальной меристемы, от повреждения при соприкосновении с почвой; б) облегчение продвижения кончика корня в почве; в) восприятие геотропического стимула, обеспечивающее правильную ориентацию корней в пространстве.
Апикальные клетки меристемы корня (1—2% от общего числа клеток в меристеме) отличаются от остальных значительно более редкими делениями, более медленным синтезом ДНК, РНК и белков, меньшим числом плазмодесм с соседними клетками. Они получили название покоящегося центра. При повреждении апикальной меристемы корня из-за неблагоприятных условий (засуха, механические повреждения и т. д.) фонд ее клеток восстанавливается за счет деления клеток покоящегося центра.
За время жизни в меристеме корня каждая клетка делится 6 — 7 раз. Количество клеток увеличивается вдоль оси корня, в результате чего образуются продольные ряды клеток. Уже в меристеме ткани корня дифференцируются (рис. 5.10): формируется перицикл, прослеживается эндодерма, клеточные стенки которой еще лишены субериновых поясков Каспари, начинается образование элементов флоэмы.
Прекратившие деление клетки корня переходят к растяжению также в направлении оси корня. Это приводит к пространственному разграничению делящихся клеток меристемы и клеток, растущих растяжением. В зоне растяжения заканчивается дифференцировка флоэмы и формируются элементы протоксилемы — клетки, содержащие цитоплазму с органоидами. В клеточных стенках обнаруживаются кольчатые и спиральные утолщения, не мешающие росту клеток растяжением.
Дифференцировка тканей корня заканчивается в зоне корневых волосков, где завершается образование основных тканей корня: ризодермы, первичной коры, эндодермы и системы тканей центрального цилиндра.
Ризодерма — это чаще всего однослойная ткань, покрывающая корень снаружи. У одних видов растений каждая клетка ризодермы обладает потенциальной способностью формировать корневой волосок; у других она состоит из двух типов клеток: трихобластов, образующих корневые волоски, и атри-хобластов, не способных к их образованию. Основная функция ризодермы — поглощение воды и минеральных веществ, для чего важна площадь контакта корня с почвой. Эта проблема решается как на организменном (растение развивает разветвленную корневую систему), так и на клеточном уровне (образование корневых волосков), что увеличивает поглощающую поверхность корня. С возрастом у одних видов растений ризодерма заменяется вторичными покровными тканями — экзодермой и перидермой (пробковой тканью). У других она сохраняется длительное время, но меняет структуру, суберинизи-руется и кутинизируется, что ограничивает ее способность к поглощению.
У травянистых растений кора корня обычно представляет собой несколько слоев живых паренхимных клеток, расположенных между экзодермой (или ризодермой) и эндодермой. Между клетками имеются крупные межклетники, обеспечивающие хорошую аэрацию корня. У сельскохозяйственных культур кора может составлять 80 — 90",, от объема корня.
Эндодерма — это внутренний слой клеток коры, граничащий с центральным цилиндром. Поперечные и радиальные клеточные стенки ее содержат непроницаемый для воды слой су-берина и лигнина, называемый в каждой клетке пояском Кае-пари. Этот слой преграждает транспорт воды и солей по апопласту и вещества проходят через клетки эндодермы по симпласту, который является частью единой системы симпласта корня.
К центральному цилиндру или стеле, относится комплекс тканей, ограниченных снаружи эндодермой. Он содержит перицикл и две системы проводящих элементов: ксилему и флоэму. Клетки перицикла представляют собой одно- или реже многослойную обкладку стели и располагаются непосредственно под эндодермой. Его клетки могут выполнять регуляторную функцию на пути транспорта веществ как из наружных слоев в ксилему, так и из флоэмы в кору. Кроме того, клетки перицикла выполняют функции образовательной ткани, способной продуцировать боковые корни, а у большинства двудольных, корни которых способны к вторичному росту, клетки перицикла формируют камбий и лучевую паренхиму.
В отличие от послойного расположения остальных тканей корня группы элементов ксилемы и флоэмы в центральном цилиндре чередуются по окружности. Окончательная дифференциация сосудов ксилемы в корне происходит одновременно с появлением поясков Каспари на стенках клеток эндодермы.
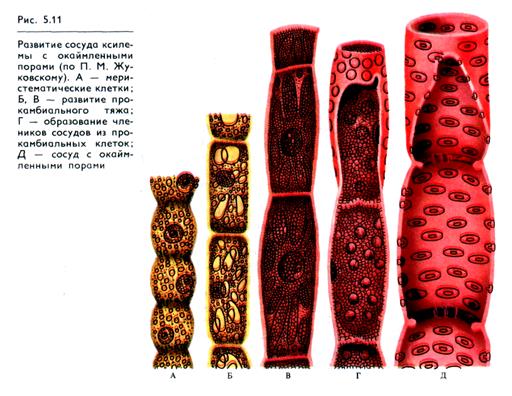
В зоне корневых волосков ксилема представлена метаксилемой с проводящими клетками, лишенными живого содержимого. Вторичные стенки клеток сосудов имеют сплошной тип утолщения. У голосеменных функцию проведения выполняют трахеиды — длинные (1 мм—12 см) остроконечные клетки, сообщающиеся через окаймленные поры в косых стенках. У покрытосеменных также есть трахеиды, но преобладают сосуды, представляющие собой полые трубки из клеточных стенок, расположенных одна под другой вертикальными рядами. Поперечные стенки между клетками вначале перфорированы, но постепенно разрушаются. Средняя длина сосудов около 10 см (у дуба — длина до 2 м, ширина — до 0,3 — 0,5 мм). Сосуды ксилемы сообщаются между собой через поры — углубления во вторичных клеточных стенках (рис. 5.11). Первичные клеточные стенки двух смежных клеток представляют собой непрерывную фазу, которую вода и растворенные вещества преодолевают путем диффузии. Поры сосудов и трахеид формируются одновременно в двух смежных клетках. Сосуды ксилемы контактируют с паренхимными клетками центрального цилиндра, которые активно транспортируют ионы в проводящие элементы ксилемы (см. рис. 8.1). Контакт осуществляется через полуокаймленные поры во вторичной клеточной стенке со стороны сосуда и поры со стороны паренхимной клетки. Между этими клетками нет плазмодесм.
 Вода и растворенные вещества из паренхимных клеток диффундируют в полость сосуда через первичную клеточную стенку. Для некоторых паренхимных клеток сосудистого пучка характерны выросты (лабиринты) стенок, выстланные плазмалеммой, что значительно увеличивает ее площадь. Эти клетки активно участвуют в транспорте веществ в сосуды и обратно и называются передаточными (переходными). Они могут граничить одновременно с сосудами ксилемы и ситовидными трубками флоэмы. Транспортные системы флоэмы обеспечивают перенос органических и некоторых минеральных веществ из надземной части растения в корни (см. рис. 8.1).
Вода и растворенные вещества из паренхимных клеток диффундируют в полость сосуда через первичную клеточную стенку. Для некоторых паренхимных клеток сосудистого пучка характерны выросты (лабиринты) стенок, выстланные плазмалеммой, что значительно увеличивает ее площадь. Эти клетки активно участвуют в транспорте веществ в сосуды и обратно и называются передаточными (переходными). Они могут граничить одновременно с сосудами ксилемы и ситовидными трубками флоэмы. Транспортные системы флоэмы обеспечивают перенос органических и некоторых минеральных веществ из надземной части растения в корни (см. рис. 8.1).
 2015-05-26
2015-05-26 3796
3796
