| Группа организмов | Температура, °С | ||
| минимальная | оптимальная | максимальная | |
| Психрофильные Мезофильные Термофильные | -4 3...10 18...30 | 6...10 20...35 50...60 | 45...50 60...75 |
При отрицательной температуре почвы большинство бактерий переходит в состояние анабиоза — скрытой жизни, когда жизнедеятельность организма максимально затормаживается. При температуре ниже 0°С некоторая активность физиологических процессов проявляется только у психрофилов. Из последних следует назвать облигатных психрофилов, обитающих в условиях Арктики и высоких гор, а также некоторые дрожжи, получившие широкое распространение в холодных вечно мерзлотных почвах тундры. Очень устойчивы к низкой температуре споры грибов и особенно бактерий, выдерживающие охлаждение до -190 и даже до -253 °С.
Термофилы активно растут и размножаются в местах разложения больших масс органического вещества — навозе, компостах, нижних слоях подстилки. Наиболее устойчивые из этой группы микроорганизмов выдерживают температуру до 80 и даже 90 °С. Вместе с тем они очень чувствительны к недостатку воды в почве. По этой причине их мало в южных почвах, которые часто испытывают засуху.
Повышение температуры выше максимума приводит к резкому нарушению метаболизма микроорганизмов и ультраструктуры их клеток. Белки цитоплазмы коагулируют, мембраны разрушаются, что ведет к смерти клеток.
IV. Жизнедеятельность микроорганизмов в сильной степени зависит от реакции среды, в частности почвенного раствора. Для различных физиологических групп микробов оптимальные пределы рН не совпадают. Так, например, грибы предпочитают более кислую реакцию (рН 3 — 6), бактерии — нейтральную или щелочную с оптимумом рН 7 — 8. Лишь уксуснокислые и серные бактерии и некоторые другие лучше развиваются в условиях сильнокислой среды.
Азотобактер в условиях кислых почв при недостатке кальция не встречается. Аммонифицирующие бактерии хорошо развиваются при рН, равной 6,5 — 8,0, денитрифицирующие — 7,0 — 8,7. Клубеньковые бактерии по-разному относятся к рН почвы в зависимости от хозяина. Например, люпиновые предпочитают более кислую среду, чем люцерновые.
Бактерии, выносящие сильнокислую среду, называют ацидофилами. Облигатные (экстремальные) ацидофилы, например бактерии из рода Thiobacillus, могут выдерживать рН среды равное 1.
Изменение рН в ту или другую сторону от оптимальных значений ведет к изменению заряда цитоплазматической мембраны микробной клетки, а это, в свою очередь, меняет скорость поступления ионов в клетку, активность ферментов. В особо экстремальных случаях эти изменения заряда могут привести к коагуляции биоколлоидов (белков и других жизненно важных соединений). Поверхность коллоидов резко уменьшается, что снижает процессы дыхания, синтез веществ и другие стороны метаболизма.
VII. Свет нужен лишь микроскопическим водорослям, цианобактериям, пурпурным и зеленым бактериям, которые на свету осуществляют фотосинтез. Для большинства же микроорганизмов свет не только не необходим для их жизнедеятельности, но является отрицательным фактором. Особенно неблагоприятны ультрафиолетовые лучи, которые действуют разрушительно на нуклеиновые кислоты. На этом основана обработка фруктовых соков ультрафиолетовыми лучами.
Основная масса различных физиологических групп микроорганизмов уже на рассеянном свету прекращает размножаться, а прямой свет оказывает бактерицидное действие. Характерно, что споры грибов и бактерий оказываются так же чувствительны к свету, как и вегетативные тела, а иногда даже менее стойки к нему. На этом основано использование света для борьбы с нежелательной патогенной микрофлорой. Так, при строительстве санаториев, больниц отводят наиболее освещаемые места, а сами здания строятся с большими окнами, пропускающими много света.
VIII. На количественный и качественный состав, а также на активность микроорганизмов почвы могут оказывать влияние радиоактивные вещества. Содержание их в различных почвах обычно невелико: от 3 до 9∙10-4 % (торий), от 9 до 58∙10-5 % (уран) и от 2 до 9∙10-11 % (радий). Доказано стимулирующее воздействие небольших доз проникающей радиации на активность и рост микроорганизмов. Азотобактер под влиянием малых доз радиации усиливал процесс азотфиксации, у клубеньковых бактерий повышалась способность проникать в ткани корней бобовых растений. Искусственно повышенный фон радиации может вызывать мутагенный эффект, приводить к повреждениям структур, а очень высокий — вызывать летальный исход. Растения и микроорганизмы в естественных условиях способны аккумулировать в десятки и сотни раз больше радиоактивных веществ, чем их содержится в окружающем субстрате.
Зная отношение микробов к факторам внешней среды, можно так регулировать их жизнедеятельность, в частности в почве, чтобы направить процессы в нужную сторону, создать наиболее благоприятные условия для минерального питания растений. Это, в свою очередь, будет способствовать увеличению биологической продуктивности и урожайности растений.
Чувствительность микроорганизмов к неблагоприятным факторам используется в быту. Для более длительного сохранения пищевых продуктов их подвергают кипячению, высушиванию, засолке (20 — 30% раствор поваренной соли), используют высокое содержание сахара при приготовлении варенья (60 — 70), сильнокислую среду (маринование, квашение овощей, мочение фруктов и т. д.), антисептирование при копчении мясных и рыбных продуктов через образование смол иальдегидов, замораживание и др. В сельском хозяйстве кислая среда используется при силосовании кормов.
РАСПРОСТРАНЕНИЕ МИКРООРГАНИЗМОВ В ПРИРОДЕ
Микроорганизмы распространены повсюду, но основным местом их обитания является почва.
I. Распределение микроорганизмов в почве зависит от конкретных физико-географических условий, типа почвообразовательного процесса, гидрологического режима и ряда других факторов.
Минимальное количество бактерий и других микроорганизмов отмечено в почвах северных районов (подзолы), а максимальное — в южных районах (черноземы, сероземы) под травянистой растительностью (табл. 5.2). Это увеличение общего числа микроорганизмов с продвижением к югу связано с миром бактерий, тогда как численность грибов уменьшается.
Наиболее заселена верхняя часть профиля почвы. С продвижением вниз численность микроорганизмов убывает с разной степенью резкости в зависимости от типа и свойств почвы. Распределение представителей микромира здесь находится в тесной зависимости от запаса органического вещества. Так, например, в верхнем A1 горизонте дерново-подзолистой лесной почвы общее число микроорганизмов доходит до 2,7 млрд в 1 г, а в нижнем подзолистом А2 —0,3 млрд, т. е. почти на целый порядок меньше. Однако в период засухи наиболее насыщенными могут оказаться более глубокие горизонты почвы, сохранившие воду.
В течение года численность микромира почвы сильно изменяется. Массовые вспышки численности могут сменяться резким снижением. Меняется и соотношение различных групп микроорганизмов почвы по ходу вегетации.
Максимальное количество представителей микроскопических существ в одном и том же генетическом горизонте отмечено около живых корней растений (в ризосфере), а также на поверхности органических остатков. В лесной подстилке развивается очень много микроскопических грибов.
Основная масса микроорганизмов почвы (80 — 90 %) находится на поверхности или внутри почвенных частиц, где им легче использовать субстратный материал, к которому они прикреплены. Адсорбция бактерий на поверхности почвенных частиц способствует их закреплению в определенных слоях почвы и сохранению гомеостаза микробных ассоциаций. Это, в свою очередь, ведет к сбалансированному для каждой разновидности почвы круговороту веществ. С развитием того или иного почвообразовательного процесса, вызванного естественными или искусственными причинами, идет и изменение состава микрофлоры, и ее распределение по профилю почвы.
Частички почвы заселены микроорганизмами очень своеобразно: на поверхности развивается аэробная часть микромира, а внутри — анаэробная. Сплошной чехол из аэробных бактерий на поверхности почвенной частички создает своеобразный фильтр, который поглощает кислород вследствие дыхания аэробов, и воздух внутри частички оказывается лишенным кислорода. Именно поэтому внутри почвенных частичек развиваются облигатные анаэробы, например бактерии из рода Clostridium.
Характерно распределение бактерий в типично лесных почвах. Так, по данным Н.Л. Благовидова, в условиях Северо-западной таежной зоны маломощных подзолов в еловых лесах кисличного типа численность бактерий оказалась в 4 раза выше, чем в торфяно-перегнойных иловатых почвах болотного ряда почвообразования. Прослеживается тесная связь количества бактерий с продуктивностью лесов: наиболее высокий среднегодичный прирост древесины характерен для кисличников, а наименьший — для сфагнозников травяных с постоянным избытком влаги.
Из грибов в почве наряду с родами Penicillium и Aspergillus заметное место занимают Fusarium и Trichoderma, а в почве тундры и степей еще и Dematium. С продвижением на юг заметно увеличивается число грибов из рода Aspergillus, а количество грибов из рода Penicillium даже несколько снижается (табл. 5.3). При окультуривании почвы количество бактерий увеличивается примерно вдвое, а число грибов уменьшается.
Цианобактерии широко распространены во всех почвах, особенно в степных каштановых, в пустынях на голых скалах и даже на поверхности льда и снега в высоких горах. Встречаются они и в воде морей, озер, водохранилищ, прудов и других водоемов, а также в воде горячих источников при температуре до 70 °С.
Достаточно широкое распространение в почве, особенно в ее самых верхних генетических горизонтах, получают микроскопические водоросли (50... 100 тыс. клеток на 1 г почвы).
По месту обитания различают наземные, водно-наземные, собственно почвенные и сверлящие водоросли. Первые разрастаются на поверхности почвы в виде налета, коробочек, вызывая «цветение» почвы. Вторые живут в воде постоянно влажных почв, и лишь третьи обитают непосредственно в толще почвы. Сверлящие водоросли, поселяясь на камнях, проделывают в них ходы и в этих ходах живут, растут и размножаются.
Распределение водорослей по профилю почвы сходно с распределением бактерий: с глубиной резко сокращается число видов и их масса (рис. 5.6.).
Максимальная глубина почвы, на которой обнаруживаются водоросли, не превышает 1,5 м. Общее число видов водорослей в лесной почве (25 — 65) ниже, чем в почве травянистых фитоценозов, где это число может достигать 100 и более.
В подзолистых почвах таежной зоны преобладают зеленые водоросли, в дерновых почвах — диатомовые. Диатомовые водоросли широко также представлены в почве верховых болот, на каменистых залежах и в некоторых других местах.
В глубоких слоях почвы, куда не проникает свет, облигатно автотрофные водоросли погибают, а факультативные переходят на гетеротрофный сапрофитный тип питания.
В грубогумусных разной степени оподзоленности почвах лесов таежной зоны основную роль в круговороте веществ играют грибы, количество которых здесь варьирует от 250 до 900 тыс. шт. в 1 г сухой почвы, затем уже бактерии, хотя количество последних в этих почвах доходит до 2 — 4 млрд в 1 г почвы. И тех и других представителей микробного мира привлекает здесь, прежде всего обилие органических остатков (корнепад, листопад) и воды. Меньше всего встречается в почвах таежных лесов актиномицетов, которые не выносят кислой среды.
Простейшие животные встречаются во всех почвах. Их число доходит до нескольких тысяч и даже сотен тысяч клеток в 1 г сухой почвы. Наибольшее значение для них имеют наличие воды в порах почвы, и количество пищи, главным образом масса бактерий, водорослей и дрожжей.
II. В воде рек, озер, морей и других водоемов микроорганизмов значительно меньше в связи с большим проникновением в воду света и меньшим содержанием органических и минеральных веществ. Вода рек может содержать разное количество микробов в зависимости от того, как далеко река расположена от населенных мест и защищена от сброса различных сточных и промышленных вод, — от нескольких сотен и тысяч до миллионов в 1 мл. В озерах количество микроорганизмов колеблется от нескольких тысяч до 10 млн в 1 мл воды. Очень много различных групп микроорганизмов в верхних слоях ила прудов, водохранилищ, рек и озер — до нескольких миллиардов клеток в 1 г ила.
II. Обилие света и отсутствие питательных веществ в воздухе предопределяют очень слабое развитие в нем микроскопических существ. Лишь в пыльном воздухе помещений с множеством людей (вокзалы, кинотеатры и т. д.) санитарно-гигиенические условия резко ухудшаются из-за обилия микробов. Замечено довольно резкое увеличение числа бактерий и других микроорганизмов в школьных классах после уроков, в студенческих аудиториях после лекций и занятий. В воздухе городов количество микроорганизмов в несколько сотен раз больше, чем в загородном парке или в лесу. Там деревья и в целом все растения очищают воздух от пыли и, выделяя особые вещества — фитонциды, убивают бактерии. Известно, что фитонциды дуба излечивают от дизентерии, а сосны — убивают туберкулезную палочку Коха. Допустимая санитарная норма содержания микроорганизмов в воздухе не более 11 тыс. в 1 м3.
УЧАСТИЕ МИКРООРГАНИЗМОВ В БИОЛОГИЧЕСКОМ КРУГОВОРОТЕ УГЛЕРОДА
Главная роль в конструктивном обмене микроорганизмов принадлежит углероду. В природе практически нет ни одного углеродеодержащего соединения, на которое не воздействовали бы микроорганизмы. По отношению к углероду все организмы делятся на автотрофные, способные синтезировать органические соединения из СО2внешней среды, и гетеротрофные, источником углеродного питания которых является готовое органическое вещество.
1. Гетеротрофы делятся на паразитов и сапрофитов.
— Паразиты живут за счет органических веществ других организмов, а сапрофиты питаются мертвым органическим материалом. Среди паразитов различают такие, которые способны развиваться только внутри клеток хозяина (облигатные паразиты, например, хламидии, лишенные собственной системы фосфорилирования), и такие, которые способны вести сапрофитный образ жизни (факультативные паразиты). Последних значительно больше, чем первых.
— Сапрофиты составляют основную массу почвенных микроорганизмов. Они перерабатывают огромные массы органических веществ мертвых остатков растений и животных и содержащихся в продуктах жизнедеятельности почвенных организмов, а также в органических удобрениях.
2. Автотрофы, в свою очередь, делятся на фотоавтотрофов (водоросли, цианобактерии, пурпурные и зеленые бактерии) и хемоавтотрофов (нитрифицирующие, водородные, бесцветные серные и железобактерии).
— Из фотоавтотрофов водоросли и цианобактерии осуществляют процесс фотосинтеза с выделением О2, подобно высшим растениям. Они имеют обе фотосистемы (ФС-1 и ФС-2). У пурпурных бактерий содержится бактериохлорофилл, активная форма которого представлена пигментом П870 а у зеленых серобактерий — П840 У пурпурных и зеленых бактерий функционирует только ФС-1, и фотосинтез происходит без выделения кислорода. Отличается эта группа и донорами протонов и электронов. Так, у зеленых и пурпурных серных бактерий таким донором является сероводород:
свет
СО2 + 2H2S → (СН2О)n + 2S + Н2О
пигменты
У пурпурных несерных бактерий в качестве доноров протонов и электронов служит молекулярный водород или водород спиртов и некоторых других органических соединений:
свет
СО2 + 2Н2 → (СН2О)n + Н2О.
пигменты
— Хемоавтотрофные бактерии получают энергию для синтеза органических веществ за счет окисления различных неорганических соединений: аммиака, водорода, сероводорода, серы, закисного железа и других. Процесс синтеза органических веществ из внешней углекислоты за счет энергии окисления неорганических соединений, как указывалось выше, носит название хемосинтеза.
Большинство микроорганизмов, как и высшие растения, используют в качестве источника энергии окисление органических веществ в процессе дыхания.
Для анаэробных микроорганизмов важнейшим источником энергии является сбраживание органических веществ. Различают следующие типы брожений:
—спиртовое;
—молочнокислое;
—маслянокислое;
—пропионовокислое и др.
I. Возбудителями спиртового брожения служат главным образом дрожжевые грибы. Пировиноградная кислота с помощью фермента пируватдекарбоксилазы расщепляется до уксусного альдегида и СО2:
СН3-СО-СООН → СН3-СНО + СО2.
Образующийся ацетальдегид при участии НАД-зависимой алкогольдегидрогеназы восстанавливается до этилового спирта.
Общее уравнение спиртового брожения можно записать так:
С6Н12О6 + 2АДФ + 2Н3РО4 → 2СН3СН2ОН + 2СО2 + 2АТФ.
В анаэробных условиях дрожжи осуществляют спиртовое брожение. При доступе кислорода они прекращают ход спиртового брожения и начинают активно размножаться почкованием. Поэтому в анаэробных условиях получают спирт, а в аэробных — коммерческие дрожжи. Из Сахаров легче всего сбраживается глюкоза, фруктоза, сахароза и мальтоза. Плохо поддаются этому процессу манноза и галактоза.
Кроме дрожжей спиртовое брожение могут вызывать некоторые бактерии, в частности Zymomonas mobilis, Sarcina ventriculi и др.
II. Возбудителями молочнокислого брожения являются бактерии из родов Streptococcus, Lactobacillus, Pediococcus и некоторых других. Все они грамположительны, не образуют спор, не способны к передвижению иявляются факультативными анаэробами. Они вызывают типичное гомоферментативное молочнокислое брожение, конечный продукт которого — молочная кислота. Другая группа молочнокислых бактерий (род Leuconostoc, некоторые виды рода Lactobacillus) в процессе гетероферментативного молочнокислого брожения продуцирует наряду с молочной ряд других веществ: уксусную кислоту, этиловый спирт и другие продукты.
При гомоферментативном молочнокислом брожении пировиноградная кислота восстанавливается с участием НАДН2 и дает молочную кислоту:
СН3-СО-СООН + НАД-Н2 → СН3-СНОН-СООН + НАД
Молочнокислое брожение используется для получения кисломолочных продуктов, при квашении овощей и силосовании кормов.
Гетероферментативное молочнокислое брожение осуществляется по окислительному пентозофосфатному пути, один из продуктов которого — ФГА превращается в ПВК, а второй — ацетилфосфат дает уксусную кислоту или этиловый спирт и СО2. Факультативно анаэробная кишечная палочка, обитающая в кишечнике животных, в анаэробных условиях сбраживает субстрат до молочной, уксусной, янтарной и муравьиной кислот, этилового спирта и молекулярного водорода.
III. Процесс сбраживания углеводов до масляной кислоты носит название маслянокислого брожения:
С6Н12О6 →СН3-СН2-СН2-СООН + 2СО2 + 2Н2 + энергия.
Возбудителями маслянокислого брожения являются бактерии из рода Clostridium. В результате окислительного декарбоксилирования ПВК образуется ацетил-КоА, который частично превращается в ацетилфосфат, а затем в уксусную кислоту. На этом этапе образуется молекула АТФ. Путь, непосредственно ведущий к синтезу масляной кислоты, начинается с конденсации двух молекул ацетил-КоА и через ряд восстановительных реакций в конечном итоге приводит к образованию масляной кислоты.
Для биологического круговорота веществ в лесу особенно важными являются две разновидности маслянокислого брожения:
— сбраживание пектиновых веществ, содержащихся в срединных пластинках клеточных стенок растений;
— анаэробное разложение целлюлозы — основного компонента оболочек растительных клеток.
Пектины состоят из довольно большого количества остатков D-галактуроновой кислоты и различных сахаров: галактозы, ксилозы и арабинозы. Разложение пектиновых веществ начинается с их гидролиза, а собственно маслянокислому брожению подвергаются только сахара — продукты гидролиза. При этом из галактозы образуются масляная кислота, углекислота и водород, а из арабинозы и ксилозы, относящихся к группе пентоз, — масляная кислота, углекислота и вода:
С5Н10О5 → СН3-СН2-СН2-СООН + СО2 + Н2О + энергия.
В анаэробных условиях, в частности в заболоченных лесных почвах, происходит медленное гидролитическое расщепление целлюлозы до глюкозы, которая затем сбраживается бактериями из рода Clostridium до масляной кислоты и ряда других продуктов.
В природе наряду с анаэробным сбраживанием существуют и аэробные процессы разложения пектиновых веществ и целлюлозы, осуществляемые микроорганизмами различных систематических групп: миксобактериями, актиномицетами и грибами. В кислых лесных почвах основную роль в разложении пектиновых веществ играют грибы, в особенности мукоровые, а клетчатки — микромицеты Trichoderma, Penicillium, Aspergillus и др. Целлюлоза в почвах степных и луговых формаций разлагается в основном бактериями.
В лесных почвах в больших количествах наряду с целлюлозой находится и лигнин. Это очень медленно гидролизуемый компонент растительного спада. Находящиеся в его составе ароматические углеводороды трудно поддаются разложению. Лигнин разлагается грибами и небольшим числом бактерий, в основном из рода Pseudomonas. Из разрушающих лигнин грибов следует, прежде всего, назвать базидиальные. После частичного разрушения лигнина базидиальными грибами в работу включаются микромицеты Fusarium, Trichoderma, Rhizoctonia, Penicillium, Aspergillus и др. На самых последних стадиях разрушения лигнина участвуют и некоторые грамотрицательные бактерии. Обычно процессы гидролиза лигнина и целлюлозы в почве идут параллельно и могут вызываться одними и теми же микроорганизмами и высшими грибами.
Гидролиз лигнина сопровождается синтезом веществ, являющихся составными элементами гумуса почвы. Ароматические спирты, продукты микробиологического распада лигнина, конденсируются с аминокислотами почвы и пептидами, образуя первичные продукты гумусовых веществ. В процессе гумификации растительных остатков, в том числе содержащих лигнин, дубильные вещества, белки, смолы, воски и некоторые другие, происходит постепенное окисление гидроксильных групп до карбоксильных. Образующиеся высокомолекулярные вещества, способные осаждаться кальцием, получили название гумусовых кислот, а более дисперсная часть гумуса — фульвокислот.
Наряду с синтезом происходит и распад гумуса почвы. Продукты распада служат основой минерального питания растений. В этом процессе участвуют бактерии из родов Pseudomonas, Seliberia, Agrobacterium, а также актиномицеты и грибы. Поэтому обогащение почвы гумусом — это результат положительного баланса между образованием и разрушением гумусовых веществ.
В составе растительного опада и трупных останков животных трудно гидролизуемыми органическими веществами являются и жиры. Они разлагаются в почве аэробными бактериями из рода Pseudomonas, актиномицетами, а также анаэробными бактериями, в особенности представителями рода Clostridium.
Возбудителями пропионового брожения являются грамположительные, не образующие спор, бактерии из рода Propionibacterium. Конечный продукт брожения — пропионовая кислота. Основной начальный этап процесса данного брожения — гликолиз. Вместе с тем у данной группы бактерий обнаруживается и окислительный пентозо-фосфатный путь, цикл Кребса ит. д. У некоторых видов проявляется эффект Пастера. К среде эти микроорганизмы малотребовательны. Они проявляют свою активность после деятельности молочнокислых бактерий, сбраживая молочную кислоту до пропионовой (СНз-СН2-СООН) и уксусной. Важно отметить, что в начале процесса ПВК не восстанавливается, как в других видах брожений, а карбоксилируется с образованием щавелевоуксусной кислоты, дальнейшее превращение которой происходит в цикле Кребса. Процесс карбоксилирования ПВК получил название гетеротрофной или темновой фиксации СО2. В небольших масштабах эта гетеротрофная фиксация СО2 наблюдается почти у всех живых организмов, в том числе у животных.
Рассмотрим схему биологического круговорота углерода (рис. 5.7.).
Автотрофы — высшие зеленые растения, водоросли, цианобактерии, фотосинтезирующие и хемосинтезирующие бактерии — фиксируют углерод СО2, включая его в органические соединения. Животные, поедая растения, концентрируют углерод в органическом веществе своего тела. Дыхание аэробных организмов и многие виды брожений сопровождаются выделением углекислоты. Опад растений и трупные останки животных и микроорганизмов разлагаются и пополняют атмосферу СО2. Образующаяся углекислота опять используется в процессах фото- и хемосинтеза. Цикл биологического круговорота углерода повторяется снова. В этом круговороте прослеживается тесная связь жизнедеятельности растений, животных и микроорганизмов.
УЧАСТИЕ МИКРООРГАНИЗМОВ В БИОЛОГИЧЕСКОМ КРУГОВОРОТЕ АЗОТА
Наряду с участием в биологическом круговороте углерода микроорганизмы выполняют очень важную роль в преобразовании азотистых веществ. Это значение микробов трудно переоценить, ибо недостаток в почве важнейшего для растений элемента азота — обычное явление. Азотное питание в сельском и лесном хозяйстве представляет собой проблему номер один.
Азот, как и углерод, является основным компонентом наиболее существенных для жизни растений органических веществ. После отмирания растений, микроорганизмов, животных органическое вещество их опа-да и трупных остатков разлагается почвенными микробами до самых простых минеральных форм азота, так нужных растениям. Это происходит с помощью большой группы микроорганизмов — аммонификаторов, а процесс по конечному продукту (аммонию) получил название аммонификации.
I. В аммонификацию включаются белки, мочевина, хитин, нуклеиновые кислоты — вещества, имеющие большой запас азота. Все они активно атакуются аммонифицирующими микроорганизмами с образованием аммиака. Разлагая то или иное азотсодержащее органическое вещество, возбудители рассматриваемого процесса за счет этого питаются, размножаются, черпают необходимое количество энергии для своей жизнедеятельности.
Обычно микробы при этом используют незначительную долю высвобождающегося азота на поддержание собственного метаболизма. Большая часть подвижного и хорошо доступного корням азота остается в почве, что благоприятно сказывается на азотном питании растений и на их урожайности. Одновременно при разложении органических веществ почвенными микроорганизмами высвобождаются ионы ортофосфорной кислоты, а также сера в форме H2S; последний окисляется серными бактериями до сульфатов.
Возбудителями аммонификации белков являются, с одной стороны, аэробы — спорообразующие палочки Bacillus mycoides, В. megaterium, В. subtilis (сенная палочка), многие актиномицеты и грибы, а с другой — анаэробные палочки из рода клостридиум (С. putrificum, С. sporogenes, С. botulinum, С. tetani). Два последних вида очень вредны для человека: первый вызывает пищевое отравление вплоть до летальных последствий, а второй — возбудитель столбняка. Все названные аммонификаторы, или гнилостные микроорганизмы, вырабатывают и выделяют большое количество протеолитических ферментов — протеаз, осуществляющих гидролиз белков. Процесс распадается на два этапа:
l.Ha первом этапе с помощью протеаз сложные белки разлагаются до простых белков, а те, в свою очередь, до аминокислот. Образующиеся аминокислоты частично усваиваются микробами, из них они строят белки своего тела. В этом случае схема реакций дезаминирования аминокислот выглядит так:
R-CHNH2-COOH + О2 → R-COOH + CO2 + NH3
2. Большая часть аминокислот на втором этапе подвергается дезаминированию, в процессе которого от них отщепляется аминогруппа NH2 и образуются свободный аммиак и органические кислоты. Различают дезаминирование, идущее с участием и без участия кислорода. Процесс осуществляется с помощью НАД-зависимой дегидрогеназы:
R-CHNH2-COOH + НАД + Н2О → R-CO-COOH + НАДН2+ NH3.
Конечные продукты аммонификации белков частично используются бактериями: аммиак — в конструктивном обмене в качестве источника азота, а органические кислоты — в энергетическом метаболизме.
Благоприятными внешними условиями для аммонификации белков являются температура в пределах 20 —30°С, достаточное количество воды, нейтральная или щелочная среда (рН 7 и выше).
Мочевина является продуктом жизнедеятельности многих грибов и животных. В чистом виде она труднодоступна корням растений. Аммонификаторы разлагают ее до аммиака, предоставляя растению удобную форму азотного питания. К уробактериям, осуществляющим аммонификацию мочевины, относятся Micrococcus urea, Sporosarcina urea, Bacillus pasteurii и др. Они вырабатывают специальный фермент уреазу и, выделяя его в среду, осуществляют рассматриваемый процесс. Аммонификация мочевины состоит из двух этапов:
1) сначала происходит гидролитическое дезаминирование мочевины с образованием углекислого аммония:
CO(NH2)2 + Н2О → (NH4)2CO3;
2) затем углекислый аммоний как вещество очень нестойкое распадается на аммиак, углекислоту и воду:
(NH4)2 СО3 → 2 NH3 + СО2 + Н2О.
Образующийся аммиак частично участвует в конструктивном обмене уробактерий, а в остальном пополняет запасы доступного для растений азота в почве.
Очень сложным и трудно разлагаемым в почве азотсодержащим веществом является хитин. Он входит в состав клеточных стенок грибов, наружного скелета ракообразных и насекомых. В химическом отношении является аналогом целлюлозы, лишь одна гидроксильная группа глюкозы заменяется группой СН3-CO-NH-. Элементарное звено молекулы этого азотсодержащего полисахарида представлено ацетилглюкозамином.
Возбудителями процесса аммонификации хитина являются бактерии из родов Bacillus, Pseudomonas, Achromobacter, а также плесневые грибы, главным образом из рода Aspergillus, и актиномицеты:
1)на первом этапе с помощью эктоферментов микроорганизмы расщепляют хитин на его элементарные звенья — молекулы ацетилглюкозамина;
2) ацетилглюкозамин уже на втором этапе распадается на глюкозу, уксусную кислоту и аммиак. Здесь, так же как и в предыдущих случаях, образующийся аммиак используется аммонификаторами и пополняет запасы азота в почве.
Наиболее активным возбудителем аммонификации нуклеиновых кислот является Bacillus megaterium:
1) с участием синтезируемых бактериями внеклеточных ферментов (рибонуклеаза и дезоксирибонуклеаза) производится гидролиз ДНК и РНК до нуклеотидов;
2) затем нуклеотиды распадаются до азотистых оснований, сахара и фосфорной кислоты;
3) азотистые основания усваиваются бактериями и внутри их клеток разлагаются до аммония, углекислоты, муравьиной, уксусной и молочной кислот. Образующийся аммоний используется в качестве источника азотного питания бактерий.
Процессам аммонификации подвергаются также гуминовые кислоты, мочевая кислота и некоторые другие вещества почвы. Образующийся в процессе аммонификации перечисленных азотсодержащих соединений аммиак соединяется в почве с анионами и образует аммонийные соли — углекислые, сернокислые и др. После отмирания аммонифицирующих бактерий азот их органических соединений под действием живых аммонификаторов также пополняет почву аммонием.
II. Другим важным в биологическом круговороте азота процессом является нитрификация — окисление образующегося при аммонификации аммиака до азотистой и азотной кислоты. Осуществляют этот процесс бактерии из группы хемоавтотрофов.
Протекает процесс нитрификации в 2 этапа:
1. Аммиак окисляется до азотистой кислоты:
2NH3 + 3O2 → 2HNO2 + 2H2O + энергия.
Этот этап осуществляют мелкие палочковидные бактерии со жгутиками из рода Nitrosomonas, а также представители родов Nitrosococcus и Nitrosospira.
2. Азотистая кислота окисляется до азотной кислоты:
2HNO2 +О2 → 2HNO3 + энергия.
Окисление происходит благодаря деятельности бактерий из родов Nitrobacter и Nitrococcus.
Высвобождающаяся при окислении аммиака и нитратов энергия идет на хемосинтез — образование из СО2 органического вещества, а также на некоторые другие процессы жизнедеятельности.
Азотная кислота, взаимодействуя с различными солями и щелочами почвы, образует нитраты — второй прекрасный источник азотного питания растений. Кроме того, азотная кислота переводит нерастворимые фосфорные соединения почвы в легкодоступные для растений формы.
Нитрификации мы обязаны образованием залежей селитры. Такие залежи возникли в Средней Азии, на Памире, в Индии, Чили, в ряде районов Африки и других местах. Наиболее богатые месторождения селитры приурочены к жаркому сухому климату и высоким горам. Особенно благоприятные условия нитрификаторы находят для себя на склонах гор.
Дождевые воды или воды вечных снегов и льдов смывают нитраты к подножию, вода здесь быстро испаряется, а нитраты накапливаются в виде больших залежей.
Нитрификация может происходить только при хорошей аэрации и нейтральной или слабощелочной реакции почвы. Достаточно активно процесс нитрификации протекает в черноземных и некоторых других почвах. В большинстве лесных почв нитрификация отсутствует или проявляется весьма слабо.
III. Противоположным нитрификации процессом является денитрификация, при которой происходит восстановление нитратов до молекулярного азота. Промежуточными веществами являются нитриты (NO2-), окись азота (NO) и закись азота (N2O).
Возбудителями денитрификации являются факультативно анаэробные бактерии из родов Pseudomonas, Micrococcus, в частности М. denitrificanas, и др. Процесс осуществляется ими с помощью соответствующих ферментов — редуктаз.
Общее уравнение процесса денитрификации выглядит так:
С6Н12О6 + 4NO3-→ 6СО2 + 6Н2О + 2N2 + энергия.
Денитрификация происходит в условиях плотных и затопленных почв с плохой аэрацией и является весьма вредным процессом, так как образующийся молекулярный азот уходит в атмосферу и не используется растениями. В практике лесного и сельского хозяйства нельзя допускать уплотнения пахотных или лесокультурных почв, а затапливаемые почвы следует осушать. В природных лесах необходимо проводить мероприятия по регулированию наплыва городского населения с тем, чтобы не уплотнять почву до предельных величин. При хорошей аэрации денитрификация прекращается, так как возбудители этого процесса переходят от анаэробного нитратного дыхания к обычному аэробному дыханию, используя в качестве акцептора электронов молекулярный кислород.
Особо важное место в биологическом круговороте веществ в природе занимает фиксация микроорганизмами атмосферного газообразного азота. Главное значение азотфиксации сводится к вовлечению инертного молекулярного азота атмосферы в биологический круговорот, к обогащению им почвы как среды обитания растений.
Микроорганизмы, способные фиксировать молекулярный азот, называются азотфиксирующими или азотфиксаторами. Среди них различают две большие группы: свободно живущие в почве азотфиксаторы и симбионты, осуществляющие этот процесс в симбиозе с растениями. К первой группе относятся Clostridium pasteurianum и некоторые другие представители рода Clostridium, Azotobacter, Beijerinckia, многие фото-трофные бактерии и цианобактерии.
Clostridium pasteurianum — анаэробная палочка-, в момент спорообразования принимающая вид веретена. Это возбудитель маслянокислого брожения. Энергия, высвобождающаяся в процессе брожения, используется этим микроорганизмом на фиксацию молекулярного азота и перевод его в состав органических веществ своего тела; на 1 г сбраживаемого сахара связывается 2 — 3 мг азота. Clostridium — строгий анаэроб, кислород является для него ядом. Вместе с тем эта бактерия широко распространена во многих почвах, в том числе хорошо дренированных, с наличием больших количеств кислорода. Объяснение заключается в том, что данный вид поселяется внутри почвенных частичек, тогда как аэробные микроорганизмы — на их поверхности. Последние, поглощая кислород, как бы фильтруют проходящий внутрь почвенного комочка воздух, лишая его кислорода.
Аэробный азотфиксатор Azotobacter chroococcum в молодых культурах представлен подвижными палочками, затем жгутики утрачиваются, клетки становятся шаровидными, обычно соединенными по 2 — 3 и окруженными слизистой капсулой. Энергию для азотфик-сации азотобактер черпает за счет обычного дыхательного распада окисляемых веществ, что определяет и эффективность процесса: на 1 г расходуемого сахара фиксируется до 20 мг азота. Чистые культуры азотобактера широко используются в качестве бактериального удобрения под названием азотобактерин.
Клубеньковые бактерии способны фиксировать азот атмосферы только в симбиозе с растениями. Бактерии, живущие в клубеньках на корнях бобовых, относятся к роду Rhizobium. Название вида клубеньковых бактерий происходит от названия вида растений, с которыми бактерии сожительствуют. Например, если на клевере, то это будет R. trifolii, на белой акации — R. robinii и т. д.
Клубеньковые бактерии живут в почве, но к фиксации азота в таком состоянии не способны. Этот процесс они могут осуществлять лишь находясь в тесном симбиотическом сожительстве, так как для азотфиксации нужна энергия, поставляемая растением-хозяином. Известно более 1300 видов бобовых растений, в корнях которых функционирует процесс азотфиксации с помощью клубеньковых бактерий. Последние представляют собой грамположительные палочки длиной всего лишь около 3 мкм. Бактерии заражают растение сразу же после прорастания семян бобовых растений, когда корень проростка проникает в почву.
Корневые волоски бобовых растений при соприкосновении с клубеньковыми бактериями выделяют особые вещества — лектины белковой природы, а бактерии — полисахариды. Под влиянием этих веществ между корневым волоском и бактериями происходит тесное взаимодействие. Корневой волосок изгибается, принимает форму ручки зонтика и начинает выделять полигалактуроназу. Этот фермент разрушает стенку своей клетки и открывает путь бактериям внутрь. Это начало пути инфекции. Бактерии в корневом волоске активно делятся, образуют инфекционную нить. Попадая в клетки коры корня, бактерии размножаются и изменяют форму: из палочек превращаются в клетки колбовидной формы — бактероиды. В дальнейшем под воздействием гормонов происходит активное деление корня с образованием клубенька.
Клубенек постепенно из белого превращается в розовый благодаря образованию леггемоглобина — белка очень сходного с гемоглобином крови животных. В этот момент устанавливается тесная функциональная связь бактериального комплекса с корнем растения, а весь комплекс представляет теперь собой азот-фиксирующую единицу.
Клубеньковые бактерии не только обеспечивают азотом себя, но и до 75 % зафиксированного ими азота отдают растению-хозяину. За один вегетационный период бобовые растения фиксируют от 100 до 400 кг азота на 1 га поля. В связи с этим урожаи зерновых, посеянных вслед за бобовыми растениями, удваиваются.
В симбиоз с азотфиксирующими микроорганизмами вступают не только бобовые, но и представители некоторых других семейств. Из древесных небобовых растений на корнях образуют клубеньки лох, облепиха, ольха. У них клубеньки формируют актиномицеты, относящиеся к роду Frankia. Они также способны фиксировать азот атмосферы. У некоторых древесных растений тропиков клубеньки образуются на листьях.
Механизм азотфиксации очень сложен. Наиболее трудным для азотфиксаторов является процесс разрыва первой из трех связей в молекуле азота N = = N. На это идет большое количество энергии, а именно 941 кДж/моль.
Связывание молекулярного азота осуществляется с помощью нитрогеназы — ферментного комплекса, способного активировать N2, а затем восстанавливать его. В состав нитрогеназы входят два белка: 1) азоферредоксин, содержащий железо; 2) молибдоферредоксин, содержащий два атома молибдена и 30 атомов железа (рис. 5.9.). Биосинтез ферментного комплекса нитрогеназы осуществляется с участием особой плаз-миды, внехромосомной ДНК. Прежде чем начинается процесс фиксации, азот активируется молибденом нитрогеназы. Железо нитрогеназы используется в качестве переносчика электронов.
Источником водорода и электронов для восстановления азота у большинства азотфиксаторов служит пировиноградная кислота. Электроны попарно передаются сначала на азоферредоксин, затем — на молибден молибдоферредоксина и, наконец, на азот. В качестве промежуточных продуктов аэотфиксации образуются диимид (NH = NH) и гидразин (H2N — NH2). Вместе с тем они могут быть и тесно связанными с ферментным комплексом — нитрогеназой. Реакции идут в следующей последовательности:
+2H +2H +2H
N=N → HN=NH → HN-NH2 → 2NH3
азот диимид гидразин аммиак
На каждую из этих реакций расходуется 4 молекулы АТФ, а всего на фиксацию молекулы N2 — 12 АТФ. Источником АТФ является окислительное или фотосинтетическое фосфорилирование.
Данный механизм азотфиксации характерен как для свободно живущих азотфиксирующих бактерий, так и для симбионтов. Образующийся NH3 служит затем основным компонентом для синтеза аминокислот, образованию которых способствует наличие в теле азотфиксаторов большого набора органических кислот.
У клубеньковых бактерий леггемоглобин принимает участие в переносе кислорода для дыхания бактероида. Энергия для восстановления азота до аммиака поступает за счет макроэргов АТФ, образующегося в митохондриях клеток корня хозяина.
Биологический круговорот азота в природе, в котором принимают участие растения, микроорганизмы и животные, складывается из следующих процессов:
1) растения усваивают соли аммония и нитраты, включая азот этих солей в свои органические вещества; они же усваивают часть азота, связанного клубеньковыми бактериями;
2) животные, поедая растения, переводят азот в состав своих органических веществ;
3) после отмирания растений, животных и микроорганизмов трупные останки их разлагаются аммонификаторами с образованием минерального азота — аммония; часть NH3 окисляется до нитратов в процессе нитрификации, вследствие чего происходит накопление в почве нитратов;
4) определенная часть нитратов, обычно в неблагоприятных условиях аэрации, в процессе денитрификации восстанавливается до молекулярного азота N2, который улетучивается в атмосферу; почва обедняется азотом;
5) свободноживущие и симбиотические азотфиксирующие микроорганизмы связывают молекулярный азот, вовлекая его в биологический круговорот.
ТИПЫ БИОЛОГИЧЕСКИХ СВЯЗЕЙ В МИРЕ ПОЧВЕННЫХ МИКРООРГАНИЗМОВ. ВЗАИМООТНОШЕНИЯ МЕЖДУ МИКРООРГАНИЗМАМИ И ВЫСШИМИ РАСТЕНИЯМИ
Микроорганизмы почвы находятся в тесной взаимосвязи между собой и другими представителями живого, с самой почвой и почвообразующей породой. Биогеоценозы представляют собой сложные комплексы разных царств природы — растений, животных, грибов, прокариот и абиотической среды:

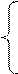 Биотип (местообитание — факторы неживой природы)
Биотип (местообитание — факторы неживой природы)
Биогеоценоз Биоценоз Фитоценоз
(сообщество) Зооценоз
Микробный ценоз
Биоценоз состоит из популяций, т.е. из особей отдельных видов растений, животных, грибов, бактерий. Основные типы взаимных связей между организмами в биоценозе сводятся к трофическим (пищевым) и метаболическим связям (выделение продуктов обмена, физиологически активных веществ и т. д.). В том и другом случае различают множество разнообразных связей.
По способности использовать в качестве пищи различные субстраты почвенные микроорганизмы были разделены С.Н. Виноградским на следующие четыре типа:
— зимогенные, которые способны питаться свежим органическим веществом;
— автохтонные, которые, обладая более мощным ферментативным аппаратом, способны разлагать сложные перегнойные вещества почвы;
— олиготрофные, довольствующиеся бедным субстратом; они способствуют завершению процессов минерализации органических веществ;
— автотрофные, использующие минеральные вещества почвы.
Заселяя один и тот же субстрат, микроорганизмы разных видов вступают между собой в сложные взаимоотношения. Поэтому различают ассоциации микроорганизмов с положительным и отрицательным балансом в борьбе за пищу или метаболиты:
1. Взаимоотношения с положительным балансом проявляется в виде симбиоза и метабиоза.
—Ярким примером симбиотических взаимных отношений являются лишайники: гриб добывает из окружающей среды воду и зольные вещества, а также минеральный азот, а водоросль поставляет грибу продукты фотосинтеза (ассимиляты). В очень тесных симбиотических отношениях находятся дрожжи и молочнокислые бактерии. Молочная кислота, как конечный продукт молочнокислого брожения, служит источником углеродного питания для дрожжей и благоприятной для них кислой среды. Устраняя избыток молочной кислоты и обогащая субстрат витаминами, дрожжи, в свою очередь, благоприятно воздействуют на развитие бактерий. Азотное питание бактерий в дальнейшем оптимизируется за счет использования аминокислот, появляющихся после отмирания грибов.
— Метабиоз может выступать в различных формах. Это уже не тесное сожительство двух видов микроорганизмов. В одном случае какой-то из партнеров оказывает положительное влияние на другой. Например, такая форма метаболизма существует между аммонификаторами и двумя группами нитрифицирующих бактерий: аммиак, образующийся в процессе аммонификации, окисляется бактериями из рода Nitrosomona до нитрита, который, в свою очередь, окисляется дальше нитратными бактериями до нитрата. Метабиоз может быть и двусторонне полезным (прокооперация). Такие отношения складываются между азотобактером и целлюлозоразрушающими бактериями: азотобактер непосредственно не может использовать целлюлозу, но хорошо усваивает продукты ее гидролиза целлюлозоразрушающими бактериями — глюкозу и органические кислоты; в свою очередь, азотобактер снабжает эти бактерии азотом. Поэтому и сам процесс разложения целлюлозы идет лучше в комплексе с азотобактером.
2. Отрицательные воздействия одних микроорганизмов на другие выступают в виде конкуренции, хищничества, паразитизма и антагонизма.
—При конкуренции за пищу побеждает тот вид микроорганизмов, который быстрее растет. Это часто наблюдается на начальных этапах разложения органического опада, например, в группе сахаролитических грибов.
—Ярким примером хищничества является пожирание простейшими животными бактерий, водорослей и дрожжей или «поедание» хитридиевыми грибами почвенных водорослей.
—Под паразитизмом понимается полная, реже частичная зависимость одного микроорганизма (паразита) от другого (хозяина). Типичным паразитом в почве является Bdellovibrio. Этот мелкий вибрион внедряется в клетки более крупных бактерий и в них интенсивно размножается за счет живого органического вещества этих бактерий. В клетках последних возникает до 50 штук вибрионов, что приводит к гибели хозяина.
—Явление подавления одним видом микроорганизма другого носит название антагонизма. Это подавление может проявляться путем образования токсических веществ неспецифического действия — таких, как сероводород, метан, перекиси, органические кислоты, и специфических антибиотиков. Отличительной особенностью антибиотиков является то, что они действуют на организмы избирательно и в очень низких концентрациях. Так, антибиотик пенициллин, продукт грибов из рода Penicillium, отрицательно действует на грамположительные бактерии и не влияет на грамотрицательные. Действие антибиотиков связано с тем, что одни из них нарушают синтез клеточной стенки (пенициллин), другие — белков (левомицетин), третьи —нуклеиновых кислот (актиномицин) и т. д. Активными продуцентами антибиотиков являются актиномицеты, что, очевидно, способствует их выживанию в жесткой конкуренции за субстрат с быстрорастущими микроорганизмами, ибо они сами растут очень медленно. Особую группу микробов-антагонистов составляют миколитические бактерии, способные за счет своих экзоферментов растворять мицелий микроскопических грибов. Наиболее ярким представителем миколитичес-ких бактерий является Pseudomonas fluorescens. Этот микроорганизм защищает растения от заражения патогенными грибами.
Очень важным является установление своеобразных связей микроорганизмов с высшими растениями в биогеоценозах. Взаимное влияние растений и микроорганизмов может наблюдаться при непосредственном поселении последних на корнях растений. К этой группе относятся, в частности, грамотрицательные бактерии, не способные образовывать споры. Эти эпифитные микроорганизмы питаются сахарами, аминокислотами и некоторыми другими веществами, в небольших количествах выделяемых растениями. К корням растений эти эпифиты прикрепляются с помощью слизи, которую они вырабатывают.
Во взаимоотношениях высших растений и микроорганизмов можно выделить и ряд других особенностей. Используя корневые выделения и опад корней, микроорганизмы в больших количествах поселяются в ризосфере — зоне, расположенной в непосредственной близости к корням. Ризосфера содержит в десятки и сотни раз больше микроорганизмов, чем почва в расчете на 1 г. Качественный состав микробов здесь также богаче вследствие разнообразия корневых выделений и растительных остатков. Ризосферные микроорганизмы оказывают существенное влияние на жизнедеятельность растений через создание особых условий вокруг корня, минерализацию органических остатков, растворение труднодоступных растению минеральных веществ почвы, фиксацию молекулярного азота, нитрификацию и т. д. Все это приводит к обогащению почвы доступными формами элементов почвенного питания растений. Положительно влияют на рост и развитие растений и выделяемые микроорганизмами физиологически активные вещества (ауксины, витамины, антибиотики и др.). Вместе с тем в ризосфере могут наблюдаться и негативные для растений явления. Так, здесь может протекать процесс денитрификации с потерей одного из важнейших элементов питания растений — азота, замедление роста растений и развития полезных микроорганизмов вследствие выделения веществ, тормозящих рост. При недостатке в почве необходимых элементов питания в доступной форме их усвоение микроорганизмами также может привести к ухудшению роста и развития растений, а следовательно, к снижению их урожайности. Некоторые микроорганизмы, проникая внутрь растения, ведут паразитический образ жизни, ослабляют растения. Особенно многочисленны грибные заболевания (микозы) растений. Бактериальные заболевания растений (бактериозы) встречаются реже.
Количество микроорганизмов в ризосфере не остается постоянным в течение вегетационного периода. К осени, например, здесь резко увеличивается количество целлюлозоразрушающих микробов при снижении большинства других групп. В целом ризосферный эффект, т.е. увеличение количества микроорганизмов в ризосфере по сравнению с почвой без корней наиболее сильно проявляется в условиях бедных песчаных почв. Специфичность же микробиологического состава ризосферы обычно выражена слабее.
Следующим ярким примером взаимных связей микроорганизмов и растений является настоящий симбиоз — мутуализм (клубеньковые бактерии, микориза).
С помощью ряда агротехнических и лесохозяйственных мероприятий можно регулировать численность и качественный состав микроорганизмов почвы, а с ними и взаимоотношения между растениями и микробами. Среди практических мероприятий можно назвать соответствующее чередование культур, агротехнику выращивания их, внесение органических, минеральных и бактериальных удобрений, известкование кислых и гипсование засоленных почв. Мощным средством воздействия на микробный ценоз почвы, а через него и на растения, является гидротехническая мелиорация сельскохозяйственных и лесных земель (ирригация, дренаж).
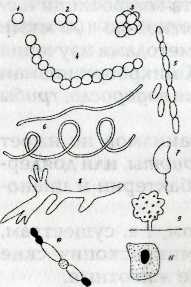
Рис. 5.1. Морфологические формы клеток прокариот: 1 — кокк; 2 — диплококк; 3 — сарцина; 4 — стрептококк; 5 — палочковидные бактерии (одиночные клетки и цепочка клеток); б — спириллы; 7 — вибрион; 8 — актиномицет;9 — плодовое тело миксобактерии;10 — нитчатая цианобактерия, образующая споры (акинеты) и гетероцисты; 11 — бактерия с капсулой (по М.В. Гусеву и Л.А. Минеевой)
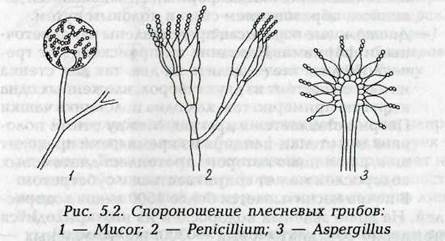
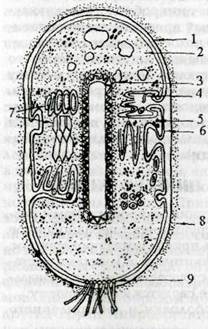
Рис. 5.3. Ультрамикроскопическое строение бактериальной клетки: 1 — стенка клетки; 2 — цитоплазма; 3 — ядерный аппарат;4 — мезосома; 5 — рибосома; 6 — цитоплазматическая мембрана; 7 — включения; 8 — капсула; 9 — жгутики
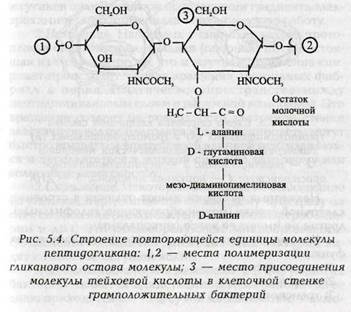
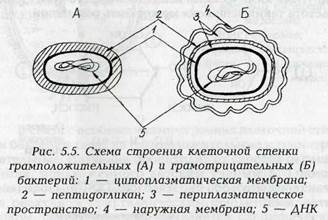
Таблица 5.2.
 2015-05-26
2015-05-26 3120
3120
