Эти изменения гемодинамики возможны при всех формах печёночно-клеточной недостаточности, но особенно — при декомпенсированном циррозе [35]. Они проявляются гиперемией конечностей, скачущим пульсом и капиллярной пульсацией. Периферический кровоток увеличивается, в основном за счёт кожного кровотока [24]. Усиливается приток артериальной крови в нижние конечности [6]. Увеличивается кровоток по воротной вене. Почечный кровоток, особенно перфузия коркового вещества, уменьшается. Увеличивается сердечный выброс [13, 29], что проявляется тахикардией, выраженным сердечным толчком, а во многих случаях и систолическим шумом (рис. 6-1 и 6-2). Эти изменения в системе кровообращения только в очень редких случаях приводят к сердечной недостаточности.
Артериальное давление низкое; в терминальной фазе это усугубляет нарушение функции почек. Нарушение кровотока в печени способствует развитию печёночной недостаточности, а снижение церебрального кровотока усугубляет нарушение психического статуса |10]. Такая артериальная гипотензия опасна для жизни, однако попытки повысить объём циркулирующей крови гемотрансфузиями или лекарственными препаратами (например, допамином) приводят только к кратковременному улучшению (см. рис. 9-13).
Периферическое сосудистое сопротивление уменьшается, как и артериовенозная разница по кислороду. При циррозе общее потребление кислорода организмом и оксигенация тканей снижаются [28]. Это связано с гипердинамическим типом кровообращения и с артериовенозным шунтированием. Таким образом, состояние повышенной вазодилатации при печёночной недостаточности может способствовать общей гипоксии тканей.
Тонус мышц сосудов понижается; доказательством этому служит сниженная вазоконстрикция при умственных нагрузках, при пробе Вальсальвы и при переходе из горизонтального положения тела в вертикальное |23, 24]. Поражение вегетативных нервов прогностически неблагоприятно [7]. Под влиянием сосудорасширяющих веществ, по-видимому, происходит раскрытие большого количества существующих, но неактивных в норме артериовенозных анастомозов. Эффективный объём артериальной крови падает, поскольку дилатация артериол приводит к увеличению артериального сосудистого объёма. В результате этого активируются симпатическая и ренин-ангиотензиновая системы и происходит задержка натрия и воды с развитием асцита (см. главу 9). Показано, что гиперкинетический тип кровообращения во внутренних органах связан с портальной гипертензией (см. главу 10).
Вазодилататоры, принимающие участие в изменениях гемодинамики, точно не установлены. Вероятно, их несколько. Какова бы ни была их природа, они зависят от поражённых гепатоцитов: либо синтезируются в них, либо недостаточно инактивируются, либо минуют их через внутри- или вне-печёночные портосистемные шунты. Вероятно, вазодилататоры образуются в кишечнике. При циррозе повышенная проницаемость слизистой оболочки кишечника и портосистемное шунтирование позволяют эндотоксину и цитокинам проникать в системное русло, что, возможно, и обусловливает наблюдаемые изменения [21, 22].
Оксид азота (NO), оказывающий мощное сосудорасширяющее действие (рис. 6-3), может служить причиной гипердинамического кровообращения и, следовательно, развития асцита, гепаторенального синдрома (см. главу 9) и портальной гипертензии (см. главу 10) [38j. NO синтезируется в эндотелии из L-аргинина; его действие связано с инактивацией гуанилатциклазы. Активностью NO-синтетазы можно управлять; эту реакцию подавляют аналоги
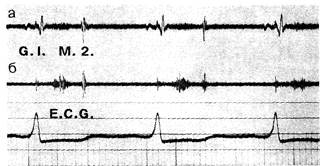
Рис. 6-1. ФКГ на верхушке (а) и на основании (б) сердца при циррозе печени. Выявляются систолический шум изгнания (М) и предсердный шум — пресистолический ритм галопа (G) [23].
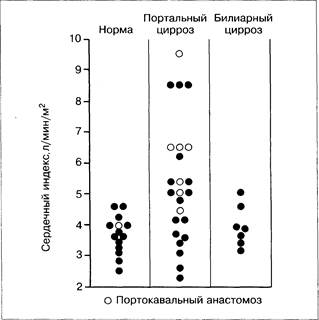
Рис. 6-2. Сердечный выброс при циррозе печени во многих случаях повышен, но при билиарном циррозе остается нормальным. В норме сердечный индекс составляет в среднем 3,68±0,60 л/мин/м3, при циррозе печени — в среднем 5,36±1,98л/мин/м2 f29].
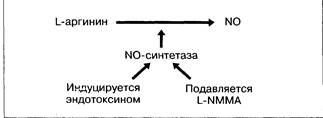
Рис. 6-3. Оксид азота (NO) — основной вазодилататор. Он образуется из L-аргинина с помощью фермента NО-синтетазы. Она может быть индуцирована эндотоксином и подавлена L-NMMA.
L-аргинина, например NG-монометил-L-аргинин (L-NMMA). Показано, что применение этих веществ устраняет многие сосудорасширяющие эффекты NO. У крыс с портальной гипертензией они уменьшали проявления гипердинамического кровообращения [19]. При циррозе печени у этих животных чувствительность к прессорному действию ингибиторов NO повышена; их введение повышает давление в воротной вене [30]. NO-синтетазу можно индуцировать стимуляцией бактериальным эндотоксином или цитокинами [26].
На кровообращение в воротной вене различные гастроинтестинальные пептиды, например вазоактивный интестинальный полипептид, субстанция Р и пептид, связанный с геном кальцитонина CGRP (II) [2], оказывают небольшое влияние. Глюкагон оказывает сосудорасширяющее действие и усиливает кровоток по непарной вене у больных циррозом, но мало влияет на сердечный индекс или на гемодинамику; таким образом, он почти не оказывает воздействия на системное сосудистое сопротивление [20]. Маловероятно, чтобы он был единственным вазодилататором, вызывающим описанные изменения.
Простагландины (El, E2 и Е12) обладают сосудорасширяющими свойствами; показано, что при хронических заболеваниях печени в воротную вену выделяются простаноиды [40]. Возможно, они частично обусловливают вазодилатацию.
При циррозе реактивность артерий на эндогенные вазоконстрикторы снижена [27].
После трансплантации печени давление в воротной вене нормализуется, однако сохранение портосистемного коллатерального кровообращения не позволяет снижаться сердечному индексу и кровообращению во внутренних органах [9, 11].
Печёночно-лёгочный синдром [18]
Почти в трети случаев декомпенсированного цирроза насыщение артериальной крови кислородом уменьшено; у некоторых больных отмечается цианоз [32] (табл. 6-1, рис. 6-4). Вероятно, причиной этого является внутрилегочное шунтирование крови через микроскопические артериовенозные фистулы [12, 34]. Исследование лёгочной артерии методом инъекционных препаратов при циррозе печени выявляет значительное расширение её тонких периферических ветвей как в лёгочной ткани, так и в плевре, где в некоторых случаях наблюдаются сосудистые звёздочки (рис. 6-5) [3]. Изредка артериовенозные шунты в лёгких удаётся выявить при ангиопульмонографии (рис. 6-6). При катетеризации сердца больного циррозом печени с цианозом, выявлено шунтирование справа налево; при физической нагрузке насыщение артериальной
Таблица 6-1. Изменения в лёгких, осложняющие хроническое печёночно-клеточное заболевание
| Гипоксия | Высокое стояние диафрагмы |
| Внутрилегочное шунтирование крови | Базальный ателектаз |
| Нарушение вентиляционно-перфузионного соотношения | Первичная лёгочная гипертензия Портопульмональное шунтирование |
| Снижение уровня фактора переноса | Пятнистость лёгочного рисунка при рентгенографии |
| Плевральный выпот |
крови кислородом уменьшалось с 91 до 68%. Доказать наличие таких шунтов можно при аутопсии, заполняя сосудистое русло лёгких желатином с контрастным веществом [3].
Расширение сосудов лёгких и артериовенозное шунтирование можно выявить при эхокардиографии с контрастированием [16]. При сканировании лёгких с 99mТc, связанным с альбумином, или при ангиопульмонографии выявляется губчатое строение сосудов базальных отделов лёгких, соответствующее участкам инфильтрации на рентгенограммах.
Снижение диффузионной способности развивается при отсутствии рестриктивных нарушений вентиляции [37]. Вероятно, оно обусловлено расширением мелких кровеносных сосудов лёгких, осложняющим как далеко зашедший цирроз, так и фульминантную печёночную недостаточность [3, 36, 42]. Во всех случаях выявляется снижение уровня фактора переноса, вероятно, связанное с утолщением стенок мелких вен и капилляров слоем коллагена [36].
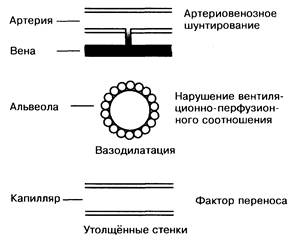
Рис. 6-4. Изменения в лёгких при печёночно-клеточной недостаточности.
Расширение сосудов лёгких сочетается с низким сопротивлением в них, которое не изменяется при гипоксии или нагрузке [1]. Это также ведёт к нарушению вентиляционно-перфузионного соотношения в лёгких [33|. Даже при сохранении вазоконстрикторной реакции лёгких на гипоксию давление в лёгочной артерии на фоне гипоксии и повышения уровня диоксида углерода оказывается сниженным. Показано образование портопульмональных анастомозов, но маловероятно, чтобы они влияли на уменьшение насыщения крови кислородом, поскольку в воротной вене содержание кислорода высокое. Кроме того, кровоток по ним, вероятно, незначителен.
Наконец, снижению функции лёгких при циррозе печени могут способствовать высокое стояние диафрагмы (вследствие гепатомегалии или значительного асцита), плевральный выпот или хронические заболевания лёгких на фоне злостного курения и алкоголизма.
Симптом «барабанных палочек» выявляется часто, но он не всегда связан с цианозом и увеличением сердечного индекса. Обычно развиваются затруднение дыхания при вставании (платипноэ) и снижение оксигенации в положении стоя (ортодеоксия)|15|.
Наиболее выраженный цианоз и симптом «барабанных палочек» наблюдаются при хроническом активном гепатите и длительно существующем циррозе. При улучшении функции печени уменьшаются как цианоз, так и тени узлов в лёгочной ткани на рентгенограммах грудной клетки.
Механизм этих изменений остаётся неясным. Вероятно, их вызывает вещество, расширяющее сосуды лёгких, но связано ли это с нарушением синтеза или с нарушением метаболизма в поражённой печени, неизвестно |14].
Связь с трансплантацией печени
При подготовке к трансплантации печени следует обязательно провести исследование лёгких [14]. Необходимо выполнить рентгенографию грудной клетки. Следует определить РаО2, в положении больного стоя и лёжа, чтобы выявить ортодеоксию, которая указывает на вазодилатацию в лёгких. Её подтверждают с помощью контрастной эхокардиографии |15|. Кроме того, вазодилатацию в лёгких можно подтвердить при сканировании с 99m'Тc, связанным с альбумином [15|.
После трансплантации печени внутрилегочное шунтирование, особенно диффузная прекапиллярная вазодилатация, уменьшается (рис. 6-7) [39]. У детей внутрилегочное шунтирование подвергается обратному развитию в течение нескольких недель после операции 117). При крупных внутрилегочных
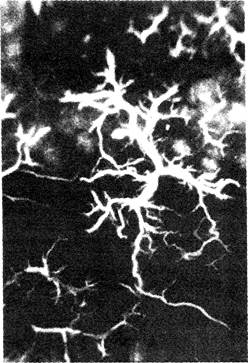
Рис. 6-5. Цирроз печени. На макропрепарате плевры видно расширение сосудов, напоминающее сосудистые звездочки |3|.
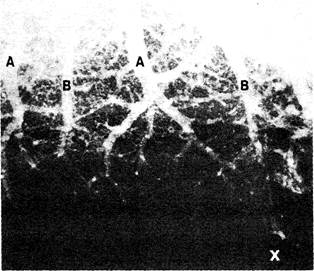
Рис. 6-6. Артериограмма больного циррозом печени (срез на уровне базальных отделов левого лёгкого). Артерии (А) и вены (В) чередуются, видны артериовенозный шунт (X) и образующая его крупная артериальная ветвь. Для контрастирования использована бариевая взвесь [3|.
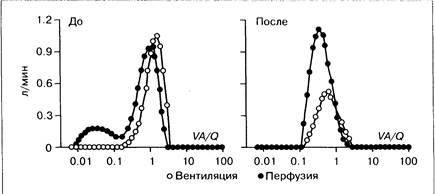
Рис. 6-7. Метод элиминации инертных газов выявляет прекращение внутрилегочного шунтирования и нормализацию вентиляционно-перфузионного соотношения после трансплантации печени [5|.
артериовенозных шунтах обратное развитие наблюдается не всегда и может потребоваться эмболизация спиралью, которую следует выполнить до трансплантации [31].
 2015-06-10
2015-06-10 4849
4849








