Под скоростью химической реакции понимают изменение концентрации
одного из реагирующих веществ в единицу времени. Рассмотрим в общем виде
скорость реакции, протекающей по уравнению:
A + B → C + D.
По мере расхода вещества А скорость реакции уменьшается. Отсюда следует, что
скорость реакции может быть определена лишь для некоторого промежутка времени.
Так как, концентрация вещества А в момент времени t1 измеряется
величиной с1, а в момент времени t2 – величиной с2
, то за время Δt= t2 - t1 концентрация изменится на
Δс= с2 - с1:
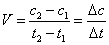
Обычно скорость измеряется в моль/л·с.
Поскольку скорость все время изменяется, то в химической кинетике рассматривают
только истинную скорость, т.е. скорость в данный момент времени. При
рассмотрении скорости необходимо различать реакции, протекающие в гомогенной и
гетерогенной системе. Гомогенной системой называется система,
состоящая из одной фазы. Гетерогенная система состоит из
нескольких фаз. Фазой называется часть системы, отделенная от
|
|
|
других ее частей поверхностью раздела, при переходе через которую свойства
изменяются скачком. Если реакция идет в гомогенной системе, то она идет во всем
объеме этой системы. Если реакция протекает в гетерогенной системе, то она
может идти только на поверхность раздела. В связи с этим скорость определяется
различно. Скорость гомогенной реакции определяется количеством вещества,
вступающего в реакцию или образующегося при реакции в единицу времени в единице
объема:
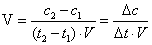
Скорость гетерогенной реакции определяется количеством вещества, вступившего
в реакцию или образовавшегося в результате реакции за единицу времени на
единице поверхности фазы:
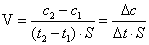
Скорость химической реакции зависит от природы реагирующих веществ и условий
протекания реакции, важнейшими из которых являются концентрация, температура
и присутствие катализатора. Чтобы осуществить химическое взаимодействие,
необходимо, чтобы вещества А и В столкнулись. Чем больше столкновений, тем
быстрее идет реакция. Число столкновений тем выше, чем больше концентрация.
Следовательно, скорость химической реакции пропорциональна произведению
концентраций реагирующих веществ. Для реакции A +B = C + D этот закон
выразится уравнением:
V = k∙c[A]∙c[D].
Этот закон химической кинетики назван законом «Действующих масс». Константа
скорости k зависит от природы реагирующих веществ и температуры, но не зависит
от концентрации! Зависимость скорости реакции от температуры отражается
правилом Вант-Гоффа: при повышении температуры на каждые 10 градусов
скорость большинства химических реакций увеличивается в 2-4 раза:
|
|
|
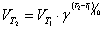
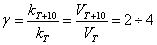
Правило Вант-Гоффа является приближенным и применимо лишь для ориентировочной
оценки влияния температуры на скорость реакции. Изменение скорости под
действием температуры связано с тем, что неактивные молекулы превращаются в
активные, обладающие энергией для осуществления данной реакции. Эта энергия
называется энергией активации.
Другой способ регулирования скорости – применение катализаторов.
Катализаторы – вещества, которые ускоряют химическую реакцию путем
многократного участия в промежуточном химическом взаимодействии с реагентами,
но после каждого цикла восстанавливающие свой химический состав. Различают
положительные катализаторы, которые ускоряют реакцию, и отрицательные
катализаторы (ингибиторы), замедляющие ее. Ускоряющее действие катализаторов
заключается в уменьшении энергии активации. Различают два вида катализа:
гетерогенный (1) – катализатор и реагирующие вещества находятся в разных фазах,
и гомогенный (2) – катализатор и вещества находятся в одной фазе:
1. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2. 2NO + O2 → 2NO2
2NO2 + 2SO2 → 2SO2 + 2NO.
 2015-07-14
2015-07-14 629
629








