Al2O3 - белый порошок или бесцветные кристаллы, очень тугоплавкий (2072 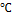 ), по твердости сравним с алмазом. Применяют термоустойчивую керамику (тигли, кирпичи…), искуственно полученные кристаллы корунда используют для производства шлифовальной бумаги (наждак), для изготовления деталей точных приборов (весы, часы). По химическим свойствам это амфотерный оксид.
), по твердости сравним с алмазом. Применяют термоустойчивую керамику (тигли, кирпичи…), искуственно полученные кристаллы корунда используют для производства шлифовальной бумаги (наждак), для изготовления деталей точных приборов (весы, часы). По химическим свойствам это амфотерный оксид.
Al2O3+ HCl → AlCl3 + H2O
Al2O3 + NaOH + H2O → Na[Al(OH)4] – в растворах
Al2O3 + NaOH → NaAlO2 + H2O – при сплавлении
Al(OH)3 - белое твердое вещество, нерастворимое в воде. Свежеполученный он выглядит как студень белого цвета. Получают его из солей:
AlCl3+ NaOH →Al(OH)3↓+ NaCl
Гидроксид алюминия имеет амфотерные свойства:
Al(OH)3+ HCl → AlCl3 + H2O
Al(OH)3+ NaOH + H2O → Na[Al(OH)4]
Эту последнюю реакцию используют как качественную, т.е. при действии щелочи на раствор, содержащий ионы алюминия выпадает белый студенистый осадок, который растворяется в избытке щелочи.
Соли алюминия в растворах подвергаются гидролизу, т.е. разлагаются водой. Особенно если это соли слабых кислот. Используют: хлорид алюминия – как катализаторов в органическом синтезе; сульфат алюминия – для очистки воды при производстве бумаги; алюминиевые квасцы (КAl(SO4)2∙ 12H2O) – для дубления кожи, как протрава при крашении х/б тканей; для производства красителей (ультрамарин).
 2015-08-12
2015-08-12 1809
1809







