États classiques de la matière
(suite)
État solide
À l'échelle macroscopique, un solide:
possède un volume propre (il est très difficilement compressible; son volume ne dépend quasiment que de la température par effet de dilatation thermique, généralement faible);
possède une forme propre (mais il peut se déformer sous l'effet de contraintes, en fonction de son élasticité et de sa ductilité).
À l'état solide, les particules (atomes, molécules ou ions) sont liées les unes aux autres par des liaisons chimiques qui fixent leurs positions relatives.
État liquide
À l'échelle macroscopique,:
un liquide possède un volume propre;
il ne possède pas de forme propre: il prend la forme du récipient qui le contient;
la surface libre d'un liquide au repos est plane et horizontale (dans un champ de pesanteur uniforme)
À l'état liquide, les particules sont faiblement liées: contrairement à l'état liquide, elles peuvent se déplacer spontanément les unes par rapport aux autres (déformabilité) mais, contrairement à l'état gazeux, elles ne sont pas indépendantes (incompressibilité). On peut également dire que leur énergie thermique est suffisante pour leur permettre de se déplacer mais pas de s'échapper...
L'état liquide est un état fluide, c'est-à-dire parfaitement déformable.
État gazeux
À l'échelle macroscopique,:
un gaz ne possède ni forme propre, ni volume propre;
il tend à occuper tout le volume disponible.
À l’état gazeux, les particules sont très faiblement liées, quasiment indépendantes (on les considère indépendantes dans le modèle des gaz parfaits, qui décrit bien le comportement des gaz basse pression).
Comme l'état liquide, l'état gazeux est un état fluide.
Un corps à l'état gazeux n'est constitué que d'atomes et de molécules. Un gaz ionisé est appelé plasma.
Changements d'état de la matière
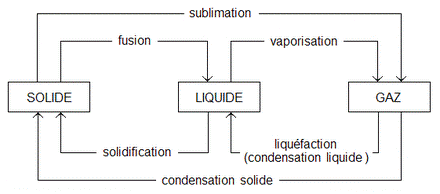
Principaux changements d'état de la matière
Le passage d'un état de la matière à un autre est appelé changement d'état. Ce changement se fait sous l'effet d'une modification du volume, de la température et/ou de la pression.
 2015-10-14
2015-10-14 313
313








