I. Алюминий.
Порошкообразный алюминий легко взаимодействует с неметаллами:
4Al + 3O2 = 2Al2O3
2Al + N2 = 2AlN
4Al + 3C  Al4C3
Al4C3
2Al + 3Br2 = 2AlBr3
2Al + 3Cl2 = 2AlCl3
2Al + 3I2 = 2AlI3
2Al + 3S = Al2S3
Очищенный от оксидной пленки алюминий способен взаимодействовать с водой:
2Al + 6H2O = 2Al(OH)3 + 3H2
Алюминий восстанавливает металлы из их оксидов (алюмотермия)
2Al + Cr2O3 = Al2O3 + 2Cr
8Al + 3Fe3O4 = 4Al2O3 + 9Fe
Как активный металл алюминий реагирует с растворами кислот с выделением водорода:
2Al + 6HCl = 2AlCl3 + 3H2
2Al + 3H2SO4(разб.) = Al2(SO4)3 + 3H2
Концентрированные серная и азотная кислоты на холоду пассивируют алюминий, однако, при сильном нагревании они растворяют алюминий.
2Al + 6H2SO4 (конц.)  Al2(SO4)3 + 3SO2 + 6H2O
Al2(SO4)3 + 3SO2 + 6H2O
Al + 6HNO3(конц..)  Al(NO3)3 + 3NO2 + 3H2O
Al(NO3)3 + 3NO2 + 3H2O
10Al + 36HNO3(разб.) = 10Al(NO3)3 + 3N2 + 48H2O
8Al + 30HNO3(разб.) = 8Al(NO3)3 + 3N2O + 15H2O
8Al + 30HNO3(оч. разб.) = 8Al(NO3)3 + 3NH4NO3 + 9H2O
При нагревании с концентрированными растворами щелочей алюминий образует комплексные соли.
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
2Al + 6NaOH  2Na3AlO3 + 3H2 (сплавление)
2Na3AlO3 + 3H2 (сплавление)
2Al + 3Na2O2  2NaAlO2 + 2Na2O
2NaAlO2 + 2Na2O
8Al + 3KNO3 + 5KOH + 18H2O = 8K[Al(OH)4] + 3NH3
10Al + 6KMnO4 + 24H2SO4 = 5Al2(SO4)3 + 6MnSO4 + 3K2SO4 + 24H2O
2Al + NaNO2 + NaOH + 5H2O = 2Na[Al(OH)4] + NH3
Al + 3KMnO4 + 4KOH = 3K2MnO4 + K[Al(OH)4]
4Al + K2Cr2O7  2Cr + 2KAlO2 + Al2O3
2Cr + 2KAlO2 + Al2O3
II. Cоединения алюминия.
1) Оксид.
Оксид алюминия – типичный представитель амфотерных оксидов. Он взаимодействует и с кислотами, и с щелочами, с кислотными и основными оксидами:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
При сплавлении оксида алюминия с щелочами образуется метаалюминат.
Al2O3 + 2NaOH  2NaAlO2 + H2O
2NaAlO2 + H2O
Al2O3 + 2KOH  2KAlO2 + H2O
2KAlO2 + H2O
Al2O3 + 3N2O5 = 2Al(NO3)3
Al2O3 + K2O  2KAlO2
2KAlO2
В соответствующие соли оксид алюминия можно перевести с помощью солей, кислотные или основные свойства которых выражены в меньшей степени:
Al2O3 + 6KHSO4 = Al2(SO4)3 + 3K2SO4 + 3H2O
Al2O3 + Na2CO3  2NaAlO2 + CO2
2NaAlO2 + CO2
Al2O3 + 3CaH2  3CaO + 2Al + 3H2
3CaO + 2Al + 3H2
2Al2O3  4Al + 3O2 (получение алюминия)
4Al + 3O2 (получение алюминия)
на катоде на аноде
2) Гидроксид алюминия.
Al2(SO4)3 + 6(NH3 ∙ H2O) = 2Al(OH)3↓ + 3(NH4)2SO4 (получение)
AlCl3 + 3(NH3 ∙ H2O) = Al(OH)3 + 3NH4Cl
Гидроксид алюминия проявляет амфотерные свойства:
Al(OH)3 + NaOH = Na[Al(OH)4]
Al(OH)3 + NaOH  NaAlO2 + 2H2O
NaAlO2 + 2H2O
Al(OH)3 + 3HCl = AlCl3 + 3H2O
2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O
Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O
Al(OH)3 + 3HBr = AlBr3 + 3H2O
Гидроксид алюминия термически неустойчив:
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
3) Соли.
Na[Al(OH)4] + CO2 = Al(OH)3↓ + NaHCO3
K[Al(OH)4] + CO2 = Al(OH)3 + KHCO3
Na[Al(OH)4] + SO2 = Al(OH)3↓ + NaHSO3
K[Al(OH)4] + SO2 = Al(OH)3 + KHSO3
Na[Al(OH)4] + 4HCl(избыток) = NaCl + AlCl3 + 4H2O
Na[Al(OH)4] + НCl(недостаток) = Al(OH)3↓ + NaCl + H2O
Na[Al(OH)4] + HNO3(недостаток) = Al(OH)3↓ + NaNO3 + H2O
2Na[Al(OH)4] + Cl2 = 2Al(OH)3↓ + NaCl + NaClO
AlCl3 + 3Na[Al(OH)4] = 4Al(OH)3↓ + 3NaCl
Na[Al(OH)4]  NaAlO2 + 2H2O↑
NaAlO2 + 2H2O↑
K[Al(OH)4]  KAlO2 + 2H2O
KAlO2 + 2H2O
AlBr3 + 3AgNO3 = 3AgBr↓ + Al(NO3)3
2Al(NO3)3 + 3K2S = 6KNO3 + Al2S3
AlCl3 + 3AgNO3 = 3AgCl↓ + Al(NO3)3
2AlCl3 + 3Ag2SO4 = Al2(SO4)3 + 6AgCl↓
Al2(SO4)3 + 3BaCl2 = 3BaSO4↓ + 2AlCl3
2AlCl3  2Al + 3Cl2
2Al + 3Cl2
на катоде на аноде
4Al(NO3)3  2Al2O3 + 12NO2 + 3O2
2Al2O3 + 12NO2 + 3O2
2Al2(SO4)3  2Al2O3 + 6SO2 + 3O2
2Al2O3 + 6SO2 + 3O2
2(AlCl3 ∙ 6H2O)  Al2O3 + 6HCl + 9H2O
Al2O3 + 6HCl + 9H2O
Al2(SO4)3 + 6NaHSO3 = 2Al(OH)3 + 6SO2 + 3Na2SO4
Al(NO3)3 + 4KOH(избыток) = K[Al(OH)4] + 3KNO3
Al(NO3)3 + 3(NH3 ∙ H2O) = Al(OH)3↓ + 3NH4Cl
AlCl3 + 3(NH3 ∙ H2O) = Al(OH)3 + 3NH4Cl
Al2(SO4)3 + 6(NH3 ∙ H2O) = 2Al(OH)3↓ + 3(NH4)2SO4
Al2(SO4)3 + 6NaOH (недостаток) = 2Al(OH)3↓ + 3Na2SO4
Al2(SO4)3 + 8NaOH(избыток) = 2Na[Al(OH)4] + 3Na2SO4
AlCl3 + 3NaOH(недостаток) = Al(OH)3↓ + 3NaCl
Al(NO3)3 + 4KOH  KAlO2 + 3KNO3 + 2H2O
KAlO2 + 3KNO3 + 2H2O
KAlO2 + 4HCl = KCl + AlCl3 + 2H2O
NaAlO2 + 4HCl = AlCl3 + NaCl + 2H2O
NaAlO2 + 4HNO3 = Al(NO3)3 + NaNO3 + 2H2O
2NaAlO2 + 4H2SO4 = Al2(SO4)3 + Na2SO4 + 4H2O
KAlO2 + H2O = K[Al(OH)4]
NaAlO2 + 2H2O = Na[Al(OH)4]
При смешивании растворов происходит гидролиз и по катиону слабого основания, и по аниону слабой кислоты:
2AlBr3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + CO2↑ + 6NaBr
2Al(NO3)3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 6NaNO3 + 3CO2↑
2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 6NaCl + 3CO2↑
Al2(SO4)3 + 3K2CO3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 3K2SO4
2AlCl3 + 3Na2S + 6H2O = 2Al(OH)3 + 3H2S↑ + 6NaCl
4) Бинарные соединения.
Al2 S3 + 8HNO3 = Al2(SO4)3 + 8NO2 + 4H2O
Al2 S3 + 30HNO3(конц. гор.) = 2Al(NO3)3 + 24NO2 + 3H2SO4 + 12H2O
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑
Al4C3 + 12H2O = 4Al(OH)3 + 3CH4
AlN + 3HCl = AlCl3 + NH3
AlN + 3H2O = Al(OH)3↓ + NH3
Алюминий. Соединения алюминия
1. В раствор, полученный при взаимодействии алюминия с разбавленной серной кислотой, по каплям добавили раствор гидроксида натрия до образования осадка. Выпавший осадок белого цвета отфильтровали и прокалили. Полученное вещество сплавили с карбонатом натрия. Напишите уравнения описанных реакций.
2. К раствору сульфата алюминия добавили избыток гидроксида натрия. В полученный раствор небольшими порциями прибавили соляную кислоту, при этом наблюдали образование объемного осадка белого цвета, который растворился при дальнейшем прибавлении кислоты. В образовавшийся раствор прилили раствор карбоната натрия. Напишите уравнения описанных реакций.
3. Газ, выделившийся при взаимодействии хлористого водорода с перманганатом калия, пропустили через раствор тетрагидроксоалюмината натрия. Образовавшийся осадок отфильтровали, прокалили, и твердый остаток обработали соляной кислотой. Напишите уравнения описанных реакций.
4. Твердое вещество, образовавшееся при взаимодействии сернистого газа и сероводорода, при нагревании взаимодействует с алюминием. Продукт реакции растворили в разбавленной серной кислоте и в образовавшийся раствор добавили поташ. Напишите уравнения описанных реакций.
5. Продукт взаимодействия серы с алюминием (реакция протекает при нагревании) растворили в холодной разбавленной серной кислоте и в раствор добавили карбонат калия. Образовавшийся осадок отделили, смешали с едким натром и нагрели. Напишите уравнения описанных реакций.
6. К раствору кальцинированной соды добавили раствор хлорида алюминия, выделившееся вещество отделили и внесли в раствор едкого натра. В образовавшийся раствор по каплям прибавляли раствор хлороводородной кислоты до прекращения образования осадка, который отделили и прокалили. Напишите уравнения описанных реакций.
7. Нитрат алюминия прокалили, продукт реакции смешали с кальцинированной содой и нагрели до плавления. Образовавшееся вещество растворили в азотной кислоте и полученный раствор нейтрализовали раствором аммиака, при этом наблюдали выделение объемного студенистого осадка. Напишите уравнения описанных реакций.
8. Осадок, полученный при добавлении в раствор сульфата алюминия каустической соды, отделили, прокалили, смешали с кальцинированной содой и нагрели до плавления. После обработки остатка серной кислотой была получена исходная соль алюминия. Напишите уравнения описанных реакций.
9. В раствор кристаллической соды добавили хлорид алюминия, выделившийся осадок отделили и обработали раствором едкого натра. Полученный раствор нейтрализовали азотной кислотой, выделившийся осадок отделили и прокалили. Напишите уравнения описанных реакций.
10. Осадок, полученный при взаимодействии раствора соли алюминия и щелочи, прокалили. Продукт реакции растворили в концентрированном горячем растворе щелочи. Через полученный раствор пропустили углекислый газ, в результате чего образовался осадок. Напишите уравнения описанных реакций.
11. Вещество, которое образуется при электролизе расплава боксита в криолите, растворяется как в растворе соляной кислоты, так и в растворе щелочи с выделением одного и того же газа. При смешивании полученных растворов образуется объемный осадок белого цвета. Напишите уравнения описанных реакций.
12. Навеску алюминия растворили в разбавленной азотной кислоте, при этом выделилось газообразное простое вещество. К полученному раствору добавили карбонат натрия до полного прекращения выделения газа. Выпавший осадок отфильтровали и прокалили. Фильтрат упарили, полученный твердый остаток сплавили с хлоридом аммония. Выделившийся газ смешали с аммиаком и нагрели полученную смесь. Напишите уравнения описанных реакций
13. Оксид алюминия сплавили с карбонатом натрия, полученное твердое вещество растворили в воде. Через полученный раствор пропускали сернистый газ до полного прекращения взаимодействия. Выпавший осадок отфильтровали, а к профильтрованному раствору прибавили бромную воду. Полученный раствор нейтрализовали гидроксидом натрия. Напишите уравнения описанных реакций.
14. Навеску сульфида алюминия обработали соляной кислотой. При этом выделился газ и образовался бесцветный раствор. К полученному раствору добавили раствор аммиака, а газ пропустили через раствор нитрата свинца. Полученный при этом осадок обработали раствором пероксида водорода. Напишите уравнения описанных реакций.
15. Порошок алюминия смешали с порошком серы, смесь нагрели, полученное вещество обработали водой, при этом выделился газ и образовался осадок, к которому добавили избыток раствора гидроксида калия до полного растворения. Этот раствор выпарили и прокалили. К полученному твердому веществу добавили избыток раствора соляной кислоты. Напишите уравнения описанных реакций.
16. Газ, выделившийся при взаимодействии хлористого водорода с бертолетовой молью, внесли в реакцию с алюминием. Продукт реакции растворили в воде и добавили гидроксид натрия до прекращения выделения осадка, который отделили и прокалили. Напишите уравнения описанных реакций.
17. Газ, выделившийся при нагревании раствора хлористого водорода с оксидом марганца (IV), внесли во взаимодействие с алюминием. Продукт реакции растворили в воде и добавили сначала избыток раствора гидроксида натрия, а затем соляную кислоту. Напишите уравнения описанных реакций.
18. Металлический алюминий растворили в растворе гидроксида натрия. Через полученный раствор пропустили избыток углекислого газа. Выпавший осадок прокалили, и полученный продукт сплавили с карбонатом натрия. Напишите уравнения описанных реакций.
19) Оксид алюминия сплавили с содой. Полученный продукт растворили в соляной кислоте и обработали избытком аммиачной воды. Выпавший осадок растворили в избытке раствора гидроксида калия. Напишите уравнения описанных реакций.
20) Оксид алюминия сплавили с гидроксидом натрия. Продукт реакции внесли в раствор хлорида аммония. Выделившийся газ с резким запахом поглощен серной кислотой. Образовавшуюся среднюю соль прокалили. Напишите уравнения описанных реакций.
21) Порошок алюминия нагрели с порошком серы, полученное вещество обработали водой. выделившийся при этом осадок обработали избытком раствора гидроксида калия до его полного растворения. К полученному раствору добавили раствор хлорида алюминия и вновь наблюдали образование белого осадка. Напишите уравнения описанных реакций.
22) Осадок, полученный при взаимодействии растворов сульфата алюминия и нитрата бария, отфильтровали. Фильтрат обработали едким натром в мольном соотношении 1: 3. Выпавший осадок отделили и прокалили. Полученное вещество обработали избытком раствора соляной кислоты. Напишите уравнения описанных реакций.
23) При взаимодействии раствора сульфата алюминия с раствором сульфида калия выделился газ, который пропустили через раствор гексагидроксоалюмината калия. Образовавшийся осадок отфильтровали, промыли, просушили и нагрели. Твердый остаток сплавили с едким натром. Напишите уравнения описанных реакций.
24) Алюминиевый порошок смешали с серой и нагрели. Полученное вещество поместили в воду. Образовавшийся осадок разделили на две части. К одной части прилили соляную кислоту, а к другой – раствор гидроксида натрия. Напишите уравнения описанных реакций.
25) Металлический алюминий растворили в растворе гидроксида натрия. Через полученный раствор пропустили избыток углекислого газа. Выпавший осадок прокалили и полученный продукт растворили в разбавленной серной кислоте. Напишите уравнения описанных реакций.
26) При взаимодействии оксида алюминия и азотной кислоты образовалась соль. Соль высушили и прокалили. Образовавшийся при прокаливании остаток подвергли электролизу в расплавленном криолите. Полученный металл нагрели с концентрированными гидроксида калия и нитрата калия. При этом выделился газ с резким запахом. Напишите уравнения описанных реакций.
27) К раствору гидроксида натрия добавили порошок алюминия. Через раствор полученного вещества пропустили избыток углекислого газа. Выпавший осадок отделили и прокалили. Полученный продукт сплавили с карбонатом натрия. Напишите уравнения описанных реакций.
28) Порошок металлического алюминия смешали с твердым иодом, и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка. Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдается выпадение осадка. Напишите уравнения описанных реакций.
29) Алюминий растворили в соляной кислоте. К полученному раствору добавили избыток раствора карбоната калия. Выпавший осадок растворили в избытке раствора едкого калия, а выделившийся газ пропустили над раскаленным углем. Напишите уравнения описанных реакций.
30) Алюминий растворили в водном растворе горячего гидроксида натрия. к полученному раствору добавили по каплям разбавленную соляную кислоту до прекращения выпадения осадка. Выделившийся в период реакции газ пропустили над раскаленным оксидом меди (II). Полученное простое вещество растворили в разбавленной азотной кислоте. Напишите уравнения описанных реакций.
31) Алюминий вступил в реакцию с. Полученную смесь веществ растворили в концентрированном растворе гидроксида натрия и отфильтровали. Твердое вещество сожгли в атмосфере хлора, а фильтрат обработали концентрированным раствором хлорида алюминия. Напишите уравнения описанных реакций.
Алюминий. Соединения алюминия
1) 2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
Al2(SO4)3 + 6NaOH(недостаток) = 2Al(OH)3↓ + 3Na2SO4
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + Na2CO3  2NaAlO2 + CO2↑
2NaAlO2 + CO2↑
2) Al2(SO4)3 + 8NaOH(избыток) = 2Na[Al(OH)4] + 3Na2SO4
Na[Al(OH)4] + НCl(недостаток) = Al(OH)3↓ + NaCl + H2O
Al(OH)3 + 3НCl = AlCl3 + 3H2O
2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 6NaCl + 3CO2↑
3) 2KMnO4 + 16HCl = 2MnCl2 + 5Cl2↑ + 2KCl + 8H2O
2Na[Al(OH)4] + Cl2 = 2Al(OH)3↓ + NaCl + NaClO + Н2О
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + 6HCl = 2AlCl3 + 3H2O
4) SO2 + 2H2S = 3S↓ + 2H2O
2Al + 3S = Al2S3
Al2S3 + H2SO4 = Al2(SO4)3 + H2S↑
Al2(SO4)3 + 3K2CO3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 3K2SO4
5) 2Al + 3S  Al2S3
Al2S3
Al2S3 + 3H2SO4 = Al2(SO4)3 + 3H2S↑
Al2(SO4)3 + 3K2CO3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 3K2SO4
Al(OH)3 + NaOH  NaAlO2 + 2H2O
NaAlO2 + 2H2O
6) 2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 6NaCl + 3CO2↑
Al(OH)3 + NaOH = Na[Al(OH)4]
Na[Al(OH)4] + HCl(недостаток) = Al(OH)3↓ + NaCl + H2O
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
7) 4Al(NO3)3  2Al2O3 + 12NO2↑ + 3O2↑
2Al2O3 + 12NO2↑ + 3O2↑
Al2O3 + Na2CO3  2NaAlO2 + CO2↑
2NaAlO2 + CO2↑
NaAlO2 + 4HNO3 = Al(NO3)3 + NaNO3 + 2H2O
Al(NO3)3 + 3(NH3 ∙ H2O) = Al(OH)3↓ + 3NH4Cl
8) Al2(SO4)3 + 6NaOH = 2Al(OH)3↓ + 3Na2SO4
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + Na2CO3  2NaAlO2 + CO2↑
2NaAlO2 + CO2↑
2NaAlO2 + 4H2SO4 = Al2(SO4)3 + Na2SO4 + 4H2O
9) 2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 6NaCl + 3CO2↑
Al(OH)3 + NaOH = Na[Al(OH)4]
Na[Al(OH)4] + HNO3(недостаток) = Al(OH)3↓ + NaNO3 + H2O
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
10) AlCl3 + 3NaOH = Al(OH)3↓ + 3NaCl
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
Na[Al(OH)4] + CO2 = Al(OH)3↓ + NaHCO3
11)  + 3O2
+ 3O2
на катоде на аноде
2Al + 6HCl = 2AlCl3 + 3H2
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
AlCl3 + 3Na[Al(OH)4] = 4Al(OH)3↓ + 3NaCl
12) 10Al + 36HNO3(разб.) = 10Al(NO3)3 + 3N2 + 48H2O
2Al(NO3)3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 6NaNO3 + 3CO2↑
NaNO3 + NH4Cl  NaCl + N2O + 2H2O
NaCl + N2O + 2H2O
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
13) Al2O3 + Na2CO3  2NaAlO2 + CO2
2NaAlO2 + CO2
NaAlO2 + 2H2O = Na[Al(OH)4]
Na[Al(OH)4] + SO2 = Al(OH)3↓ + NaHSO3
NaHSO3 + Br2 + H2O = NaHSO4 + HBr
NaHSO4 + NaOH = Na2SO4 + H2O
HBr + NaOH = NaBr + H2O
14) Al2S3 + 6HCl = 2AlCl3 + 3H2S↑
AlCl3 + 3(NH3 ∙ H2O) = Al(OH)3↓ + 3NH4Cl
Pb(NO3)2 + H2S = PbS↓ + 2HNO3
PbS + 4H2O2 = PbSO4 + 4H2O
15) 2Al + 3S = Al2S3
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑
Al(OH)3 + KOH = K[Al(OH)4]
K[Al(OH)4]  KAlO2 + 2H2O
KAlO2 + 2H2O
KAlO2 + 4HCl = AlCl3 + KCl + 2H2O
16) KClO3 + 6HCl = KCl + 3Cl2 ↑ + 3H2O
2Al + 3Cl2 = 2AlCl3
AlCl3 + 3NaOH = Al(OH)3↓ + 3NaCl
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
17) MnO2 + 4HCl = MnCl2 + Cl2↑ + 2H2O
2Al + 3Cl2 = 2AlCl3
AlCl3 + 4NaOH = Na[Al(OH)4] + 3NaCl
Na[Al(OH)4] + 4HCl = AlCl3 + NaCl + 4H2O
18) 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Na[Al(OH)4] + CO2 = Al(OH)3↓ + NaHCO3
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + Na2CO3  2NaAlO2 + CO2↑
2NaAlO2 + CO2↑
19) Al2O3 + Na2CO3  2NaAlO2 + CO2↑
2NaAlO2 + CO2↑
NaAlO2 + 4HCl = NaCl + AlCl3 + 2H2O
AlCl3 + 3(NH3 · H2O) = Al(OH)3↓ + 3NH4Cl
Al(OH)3 + 3KOH = K3[Al(OH)6]
20) Al2O3 + 2NaOH  2NaAlO2 + H2O
2NaAlO2 + H2O
NaAlO2 + NH4Cl + H2O = NaCl + Al(OH)3↓ + NH3↑
2NH3 + H2SO4 = (NH4)2SO4
(NH4)2SO4  NH4HSO4 + NH3↑
NH4HSO4 + NH3↑
21) 2Al + 3S = Al2S3
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑
Al(OH)3 + KOH = K[Al(OH)4]
допустимо образование K3[Al(OH)6]
3K[Al(OH)4] + AlCl3 = 4Al(OH)3 + 3KCl
22) Al2(SO4)3 + 3Ba(NO3)2 = 3BaSO4↓ + 2Al(NO3)3
Al(NO3)3 + 3NaOH = Al(OH)3↓ + 3NaNO3
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + 6HCl = 2AlCl3 + 3H2O
23) Al2(SO4)3 + 3K2S + 6H2O = 2Al(OH)3 + 3H2S↑ + 3K2SO4
3H2S + K3[Al(OH)6] = 2Al(OH)3 + 3KHS + 3H2O
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + 2NaOH  2NaAlO2 + H2O
2NaAlO2 + H2O
24) 2Al + 3S  Al2S3
Al2S3
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3 + NaOH = Na[Al(OH)4]
допустимо образование Na3[Al(OH)6]
25) 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Na[Al(OH)4] + CO2 = Al(OH)3↓ + NaHCO3
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
26) Al2O3 + 6HNO3 = 2Al(NO3)3 + 3H2O
4Al(NO3)3  2Al2O3 + 12NO2 + 3O2
2Al2O3 + 12NO2 + 3O2
 + 3O2
+ 3O2
на катоде на аноде
8Al + 3KNO3 + 5KOH + 18H2O = 3NH3 + 8K[Al(OH)4]
27) 2NaOH + 2Al + 6H2O = 2Na[Al(OH)4] + 3H2
Na[Al(OH)4] + CO2 = Al(OH)3 + NaHCO3
2Al(OH)3  Al2O3 + 3H2O
Al2O3 + 3H2O
Al2O3 + Na2CO3 = 2NaAlO2 + CO2
28) 2Al + 3I2 = 2AlI3
AlI3 + 3NaOH = Al(OH)3 + 3NaI
Al(OH)3 + 3HCl = AlCl3 + 3H2O
2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3 + 3CO2 + 6NaCl
29) 2Al + 6HCl = 2AlCl3 + 3H2
2AlCl3 + 3K2CO3 + 3H2O = 2Al(OH)3 + 6KCl + 3CO2
Al(OH)3 + 3KOH = K3[Al(OH)6]
C + CO2 = 2CO
30) 2NaOH + 2Al + 6H2O = 2Na[Al(OH)4] + 3H2
Na[Al(OH)4] + 4HCl = AlCl3 + NaCl + 4H2O
CuO + H2 = Cu + H2O
3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 2NO + 4H2O
31) 8Al + 3Fe3O4 = 9Fe + 4Al2O3
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
2Fe + 3Cl2 = 2FeCl3
3Na[Al(OH)4] + AlCl3 = 4Al(OH)3 + 3NaCl
Железо. Соединения железа.
I. Железо.
При обычных условиях железо малоактивно, но при нагревании, в особенности в мелкораздробленном состоянии, оно становится активным и реагирует почти со всеми неметаллами. Активные неметаллы (фтор, хлор, бром) окисляют железо до устойчивой степени окисления +3, а менее активные (сера, иод) – до степени окисления +2:
2Fe + 3Br2 = 2FeBr3
2Fe + 3Cl2 = 2FeCl3
Fe + I2 = FeI2
Fe + S  FeS
FeS
С углеродом и кремнием железо образует сплавы или соединения:
3Fe + С  Fe3С
Fe3С
3Fe + Si  Fe3Si
Fe3Si
При взаимодействии с кислородом железо образует окалину – двойной оксид железа (II, III)
3Fe + 2O2  Fe3O4
Fe3O4
Fe + Fe3O4  4FeO
4FeO
При высокой температуре раскаленное железо реагирует с водой, образуя двойной оксид железа (II, III)
3Fe + 4H2O(пар)  Fe3O4 + 4H2
Fe3O4 + 4H2
В воде в присутствии кислорода и во влажном воздухе железо окисляется (корродирует)
4Fe + 3O2 + 6H2O = 4Fe(OH)3
Железо реагирует с растворами серной и соляной кислот, вытесняя из них водород и образуя соли железа (II):
Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4(разб) = FeSO4 + H2
Концентрированные серная и азотная кислоты при обычной температуре пассивируют железо. При нагревании железо реагирует с концентрированной H2SO4, образуя сульфат железа (III):
2Fe + 6H2SO4(конц.)  Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 3SO2 + 6H2O
а с концентрированной азотной кислотой, образуя нитрат железа (III):
Fe + 6HNO3(конц.)  Fe(NO3)3 + 3NO2↑ + 3H2O
Fe(NO3)3 + 3NO2↑ + 3H2O
Разбавленная азотная кислота в зависимости от концентрации может восстанавливаться железом до NO, N2O, N2, NH3 (NH4NO3)
Fe + 4HNO3(разб.гор.) = Fe(NO3)3 + NO + 2H2O
10Fe + 36HNO3(разб.) = 10Fe(NO3)3 + 3N2 + 18H2O
4Fe + 10HNO3(оч. разб.) = 4Fe(NO3)2 + NH4NO3 + 3H2O
Из растворов солей железо вытесняет металлы, которые располагаются правее его в электрохимическом ряду напряжений:
Fe + CuSO4 = FeSO4 + Cu
При нагревании железных опилок с щелочным расплавом сильных окислителей образуется феррат:
Fe + 2KOH + 3KNO3 = 3KNO2 + K2FeO4 + H2O
2Fe(NO3)3 + Fe = 3Fe(NO3)2
2FeCl3 + Fe = 3FeCl2
Fe2(SO4)3 + Fe = 3FeSO4
II. Cоединения железа.
1) Оксиды железа.
Оксид железа (II).
Оксид железа (II) проявляет основные свойства, растворяется в кислотах, образуя соли железа (II):
FeO + H2SO4(разб.) = FeSO4 + H2O
FeO + 2H+ = Fe2+ + H2O
Оксид железа (II) проявляет окислительно-восстановительную двойственность, но восстановительные свойства преобладают.
3FeO + 10HNO3(разб.)  3Fe(NO3)3 + NO + 5H2O
3Fe(NO3)3 + NO + 5H2O
FeO + 4HNO3(конц.) = NO2 + Fe(NO3)3 + 2H2O
FeO + CO  Fe + CO2
Fe + CO2
Оксид железа (III) проявляет слабовыраженные амфотерные свойства:
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 6HNO3 = 2Fe(NO3)3 + 3H2O
Fe2O3 + Na2CO3  2NaFeO2 + CO2
2NaFeO2 + CO2
Fe2O3 + 2NaOH  2NaFeO2 + H2O
2NaFeO2 + H2O
Fe2O3 + 3NaH  3NaOH + 2Fe
3NaOH + 2Fe
Fe2O3 + KClO3 + 4KOH  2K2FeO4 + KCl + 2H2O
2K2FeO4 + KCl + 2H2O
Fe2O3 + 3KNO3 + 4KOH  2K2FeO4 + 3KNO2 + 2H2O
2K2FeO4 + 3KNO2 + 2H2O
Fe2O3 + 2Al  2Fe + Al2O3
2Fe + Al2O3
Fe2O3 + 3СO  2Fe + 3CO2
2Fe + 3CO2
Fe2O3 + Fe  3FeO
3FeO
Fe2O3 + 3Н2  2Fe + 3H2O
2Fe + 3H2O
Оксид железа (II, III)
Fe3O4 + 4H2  3Fe + 4H2O
3Fe + 4H2O
4Fe3O4 + O2(воздух)  6Fe2O3
6Fe2O3
Fe3O4 + 4CO = 3Fe + 4CO2
Fe3O4 + 8HCl = FeCl2 + 2FeCl3 + 4H2O
Fe3O4 + 10HNO3(конц.) = NO2↑ + 3Fe(NO3)3 + 5H2O
Fe3O4 + 4H2SO4(разб.) = Fe2(SO4)3 + FeSO4 + 4Н2О
Fe3O4 + 8HI = 3FeI2 + I2 + 4H2O
3Fe3O4 + 28HNO3(разб.) = 9Fe(NO3)3 + NO + 14H2O
3) 2Fe3O4 + 10H2SO4(конц.) = 3Fe2(SO4)3 + SO2 + 10H2O
2) Гидроксиды железа.
Гидроксид железа (II) проявляет основные свойства.
Fe(OH)2 + H2SO4 = FeSO4 + 2H2O
Свежеполученный белый осадок – гидроксид железа (II) на воздухе зеленеет, затем буреет, переходя в гидроксид железа (III):
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
2Fe(OH)2 + H2O2 = 2Fe(OH)3
При растворении Fe(OH)2 в азотной или концентрированной серной кислотах образуются соли железа (III):
2Fe(OH)2 + 4H2SO4(конц.) = Fe2(SO4)3 + SO2 + 6H2O
При нагревании Fe(OH)2 разлагается на оксид железа (II) и воду.
Fe(OH) 2  FeO + H2O
FeO + H2O
Гидроксид железа (III)
Гидроксид железа (III) проявляет слабые амфотерные свойства
2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 + 6H2O
Fe(OH)3 + 3HCl = FeCl3 + 3H2O
Fe(OH)3 + 3NaOH  Na3[Fe(OH)6]
Na3[Fe(OH)6]
2Fe(OH)3 + 6HI = 2FeI2 + I2 + 6H2O
2Fe(OH)3 + 3Br2 + 10KOH = 2K2FeO4 + 6KBr + 8H2O
2Fe(OH)3  Fe2O3 + 3H2O
Fe2O3 + 3H2O
6Fe(OH)3 + H2  2Fe3O4 + 10H2O
2Fe3O4 + 10H2O
3) Соли.
Соли железа (II)
2FeSO4 + Br2 + H2SO4 = Fe2(SO4)3 + 2HBr
FeBr2 + 4HNO3(конц.) = Fe(NO3)3 + 2HBr + NO2 + H2O
6FeSO4 + K2Cr2O7 + 7H2SO4 = 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
2FeSO4 + H2O2 + H2SO4 = Fe2(SO4)3 + 2H2O
6FeSO4 + 2KNO3 + 4H2SO4 = 3Fe2(SO4)3 + 2NO + K2SO4 + 4H2O
2FeSO4 + CuSO4 = Fe2(SO4)3 + Cu
4FeSO4 + O2 + 2H2SO4 = 2Fe2(SO4)3 + 2H2O
10FeSO4 + 2KMnO4 + 8H2SO4 = 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
FeCl2 + NaNO2 + 2HCl = FeCl3 + NO + NaCl + H2O
5FeCl2 + 3KMnO4 + 24HCl = 5FeCl3 + 3MnCl2 + 5Cl2 + 3KCl + 12H2O
2FeCl2 + 2H2O  Fe + H2 + 2Cl2 + Fe(OH)2↓
Fe + H2 + 2Cl2 + Fe(OH)2↓
4FeCl2 + 8NaOH + O2 + 2H2O = 4Fe(OH)3↓ + 8NaCl
2FeCl2 + Cl2 + 6NaOH = Fe(OH)3 + 6NaCl + 3H2O
FeCl2 + 4HNO3(конц.) = Fe(NO3)3 + NO2 + 2HCl↑ + H2O
3FeCl2 + 4HNO3 = Fe(NO3)3 + 2FeCl3 + NO + 2H2O
2FeCl2 + Cl2 = 2FeCl3
2FeI2 + 6H2SO4(конц.) = Fe2(SO4)3 + 2I2 + 3SO2 + 6H2O
Fe(NO3)2 + Na2S = FeS↓ + 2NaNO3
2FeS + 7Cl2 = 2FeCl3 + 2SCl4
10FeS + 6KMnO4 + 24H2SO4 = 5Fe2(SO4)3 + 6MnSO4 + 3K2SO4 + 24H2O
4FeS + 7O2 = 2Fe2O3 + 4SO2
FeS + 12HNO3(конц.) = Fe(NO3)3 + H2SO4 + 9NO2 + 5H2O
Соли железа (III)
FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
2FeCl3 + 3Na2S = 2FeS + S + 6NaCl
2FeCl3 + Fe = 3FeCl2
2FeCl3 + 2KI = 2FeCl2 + I2 + 2KCl
2FeCl3 + H2S = 2FeCl2 + S + 2HCl
2FeCl3 + Cu = 2FeCl2 + CuCl2
2FeCl3 + H2 = 2FeCl2 + 2HCl
FeCl3 + 3CH3COOAg = (CH3COO)3Fe + 3AgCl↓
4FeCl3 + 6H2O 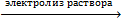 2Fe + 3H2 + 2Fe(OH)3 + 6Cl2
2Fe + 3H2 + 2Fe(OH)3 + 6Cl2
2FeBr3 + K2S + 4KOH = 2Fe(OH)2↓ + S↓ + 6KBr
2Fe(NO3)3 + 3Zn = 2Fe + 3Zn(NO2)2
2Fe(NO3)3 + 4H2SO4(конц.) = Fe2(SO4)3 + SO2 + 4HNO3 + 2H2O
Fe(NO3)2 + Na2S = FeS↓ + 2NaNO3
Fe2(SO4)3 + 2KI = I2 + 2FeSO4 + K2SO4
Fe2(SO4)3 + 3BaI2 = 2FeI2 + 3BaSO4↓ + I2↓
Fe2(SO4)3 + 3BaCl2 = 3BaSO4↓ + 2FeCl3
2NaFeO2 + 3NaNO3 + 2NaOH  2Na2FeO4 + 3NaNO2 + H2O
2Na2FeO4 + 3NaNO2 + H2O
2K2FeO4 + 16HCl = 4KCl + 2FeCl3 + 3Cl2 + 8H2O
4Fe(NO3)3  2Fe2O3 + 12NO2↑ + 3O2↑
2Fe2O3 + 12NO2↑ + 3O2↑
При смешивании растворов происходит гидролиз и по катиону слабого основания, и по аниону слабой кислоты:
2Fe(NO3)3 + 3K2CO3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑ + 6KNO3
2FeCl3 + 3Na2CO3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑ + 6NaCl
2FeCl3 + 3Na2SO3 + 3H2O = 2Fe(OH)3↓ + 3SO2↑ + 6NaCl
2Fe(NO3)3 + 3Na2CO3 + H2O = 2Fe(OH)3↓ + 3CO2↑ + 6NaNO3
Fe2(SO4)3 + 3Na2CO3 + 3H2O = 2Fe(OH)3↓ + 3CO2 + 3Na2SO4
Fe2(SO4)3 + Na2SO3 + H2O = Na2SO4 + 2FeSO4 + H2SO4
Железо. Соединения железа.
1. Соль, полученную при растворении железа в концентрированной серной кислоте, обработали избытком раствора гидроксида натрия. Выпавший бурый осадок отфильтровали и прокалили. Полученное вещество сплавили с железом. Напишите уравнения описанных реакций.
2. Осадок, полученный при взаимодействии хлорида железа (III) и нитрата серебра отфильтровали. Фильтрат обработали раствором едкого кали. Выпавший осадок бурого цвета отделили и прокалили. Полученное вещество при нагревании реагирует с алюминием с выделением тепла и света. Напишите уравнения описанных реакций.
3. Газ, выделившийся при взаимодействии хлористого водорода с перманганатом калия, реагирует с железом. Продукт реакции растворили в воде и добавили к нему сульфид натрия. Более легкое из образовавшихся нерастворимых веществ отделили и ввели в реакцию с горячей концентрированной азотной кислотой. Напишите уравнения описанных реакций.
4.Зловонную жидкость, образовавшуюся при взаимодействии бромистого водорода с перманганатом калия, отделили и нагрели с железной стружкой. Продукт реакции растворили в воде и добавили к нему раствор гидроксида цезия. Образовавшийся осадок отфильтровали и покалили. Напишите уравнения описанных реакций.
5. Вещество, полученное на катоде при электролизе раствора хлорида железа (II), сплавили с серой, и продукт этой реакции подвергли обжигу. Образовавшийся газ пропустили через раствор гидроксида бария. Напишите уравнения описанных реакций.
6. Раствор хлорида железа (III) подвергли электролизу с графитовыми электродами. Осадок бурого цвета, образовавшийся в качестве побочного продукта электролиза, отфильтровали и прокалили. Вещество, образовавшееся на катоде, растворили в концентрированной азотной кислоте при нагревании. Продукт, выделившийся на аноде, пропустили через холодный раствор гидроксида калия. Напишите уравнения описанных реакций.
7. На раствор хлорного железа подействовали раствором едкого натра, выпавший осадок отделили и нагрели. Твердый продукт реакции смешали с кальцинированной содой и прокалили. К оставшемуся веществу добавили нитрат и гидроксид натрия, и длительное время нагревали при высокой температуре. Напишите уравнения описанных реакций.
8. Оксид двухвалентного железа нагрели с разбавленной азотной кислотой. Раствор осторожно выпарили, твердый остаток растворили в воде, в полученный раствор внесли железный порошок и через некоторое время профильтровали. К фильтрату добавили раствор едкого кали, выпавший осадок отделили и оставили на воздухе, при этом цвет вещества изменился. Напишите уравнения описанных реакций.
9. Хлористое железо обработали при нагревании концентрированной азотной кислотой и раствор осторожно выпарили. Твердый продукт растворили в воде, добавили к полученному раствору поташ и выпавший осадок отделили и прокалили. Над полученным веществом пропустили при нагревании газообразный водород. Напишите уравнения описанных реакций.
10. К раствору хлорного железа добавили кальцинированную соду и выпавший осадок отделили и прокалили. Над полученным веществом пропустили при нагревании угарный газ и твердый продукт последней реакции ввели во взаимодействие с бромом. Напишите уравнения описанных реакций.
11. Железную окалину растворили в концентрированной азотной кислоте при нагревании. Раствор осторожно выпарили, и продукт реакции растворили в воде. К полученному раствору добавили железный порошок, через некоторое время раствор отфильтровали, и фильтрат обработали раствором едкого кали, в результате выделился осадок светло-зеленого цвета, который быстро темнеет на воздухе. Напишите уравнения описанных реакций.
12. К раствору хлорного железа добавили железный порошок и через некоторое время раствор профильтровали. К фильтрату добавили гидроксид натрия, выделившийся осадок отделили и обработали перекисью водорода. К полученному веществу добавили избыток раствора едкого кали и бром; в результате протекания реакции окраска брома исчезла. Напишите уравнения описанных реакций.
13. Нерастворимое вещество, образующееся при добавлении в раствор хлористого железа едкого натра, отделили и растворили в разбавленной серной кислоте. В полученный раствор добавили цинковую пыль, выделившийся осадок отфильтровали и растворили в концентрированной соляной кислоте. Напишите уравнения описанных реакций.
14. Железный порошок растворили в большом количестве разбавленной серной кислоты и через полученный раствор пропустили воздух, а затем газ с запахом тухлых яиц. Образовавшуюся нерастворимую соль отделили и растворили в горячем растворе концентрированной азотной кислоты. Напишите уравнения описанных реакций.
15. Неизвестное вещество А растворяется в концентрированной соляной кислоте, процесс растворения сопровождается выделением газа с запахом тухлых яиц; после нейтрализации раствора щелочью образуется объемный осадок белого (светло-зеленого) цвета. При обжиге вещества А образуются два оксида. Один из них – газ, имеющий характерный резкий запах и обесцвечивающий бромную воду с образованием в растворе двух сильных кислот. Напишите уравнения описанных реакций.
16. Серебристо-серый металл, который притягивается магнитом, внесли в горячую концентрированную серную кислоту и нагрели. Раствор охладили и добавили едкий натр до прекращения образования аморфного осадка бурого цвета. Осадок отделили, прокалили и растворили в концентрированной соляной кислоте при нагревании. Напишите уравнения описанных реакций.
17. Вещество, полученное при нагревании железной окалины в атмосфере водорода, внесли в горячую концентрированную кислоту и нагрели. Полученный раствор выпарили, остаток растворили в воде и обработали раствором хлорида бария. Раствор профильтровали и в фильтрат внесли медную пластинку, которая через некоторое время растворилась. Напишите уравнения описанных реакций.
18. Раствор хлорида железа (III) подвергли электролизу. Осадок бурого цвета, образовавшийся при электролизе, отфильтровали, и растворили в растворе гидроксида натрия, после чего добавили такое количество серной кислоты, которое необходимо для образования прозрачного раствора. Продукт, выделившийся на аноде, пропустили через горячий раствор гидроксида калия. Напишите уравнения описанных реакций.
19. Железо сожгли в хлоре. Продукт реакции растворили в воде и в раствор внесли железные опилки. Через некоторое время раствор профильтровали и в фильтрат добавили сульфида натрия. Выделившийся осадок отделили и обработали 20%-ной серной кислотой, получив почти бесцветный раствор. Напишите уравнения описанных реакций.
20. Смесь железного порошка и твердого продукта, полученного при взаимодействии сернистого газа и сероводорода, нагрели без доступа воздуха. Полученный продукт подвергли обжигу на воздухе. Образовавшееся твердое вещество реагирует с алюминием с выделением большого количества тепла. Напишите уравнения описанных реакций.
21. Оксид железа (III) сплавили с содой. Полученный продукт внесли в воду. Выпавший осадок растворили в иодоводородной кислоте. Выделившийся галоген связали тиосульфатом натрия. Напишите уравнения описанных реакций.
22. Хлор прореагировал с горячим раствором гидроксида калия. При охлаждении раствора выпали кристаллы бертолетовой соли. Полученные кристаллы внесли в раствор соляной кислоты. образовавшееся простое вещество прореагировало с металлическим железом. Продукт реакции нагрели с новой навеской железа. Напишите уравнения описанных реакций.
23. Пирит подвергли обжигу, полученный газ с резким запахом пропустили через сероводородную кислоту. Образовавшийся желтоватый осадок отфильтровали, просушили, смешали с концентрированной азотной кислотой и нагрели. Полученный раствор дает осадок с нитратом бария. Напишите уравнения описанных реакций.
24. Железные опилки растворили в разбавленной серной кислоте, полученный раствор обработали избытком раствора гидроксида натрия. Образовавшийся осадок профильтровали и оставили на воздухе до тех пор, пока он не приобрел бурую окраску. Бурое вещество прокалили до постоянной массы. Напишите уравнения описанных реакций.
25. Провели электролиз раствора хлорида натрия. К полученному раствору добавили хлорид железа (III). Выпавший осадок отфильтровали и прокалили. Твердый остаток растворили в иодоводородной кислоте. Напишите уравнения описанных реакций.
26. Хлорат калия нагрели в присутствии катализатора, при этом выделился бесцветный газ. Сжиганием железа в атмосфере этого газа была получена железная окалина. Ее растворили в разбавленной соляной кислоте. К полученному при этом раствору добавили раствор, содержащий дихромат натрия и соляную кислоту. Напишите уравнения описанных реакций.
27. Железо сожгли в хлоре. Полученную соль добавили к раствору карбоната натрия, при этом выпал бурый осадок. Этот осадок отфильтровали и прокалили. Полученное вещество растворили в иодоводородной кислоте. Напишите уравнения описанных реакций.
28. Серу сплавили с железом. Продукт реакции обработали соляной кислотой. Выделившийся при этом газ сожгли в избытке кислорода. Продукты горения поглотили водным раствором сульфата железа (III). Напишите уравнения описанных реакций.
29. В результате неполного сгорания угля получили газ, в токе которого нагрели оксид железа (III). Полученное вещество растворили в горячей концентрированной серной кислоте. Образовавшийся раствор соли обработали избытком раствора сульфида калия. Напишите уравнения описанных реакций.
30. Железо сожгли в атмосфере хлора. Полученное вещество обработали избытком раствора гидроксида натрия. Образовавшийся бурый осадок, ко
 2020-06-29
2020-06-29 157
157








