I. Цинк.
Цинк – довольно активный металл, но на воздухе он устойчив, так как покрывается тонким слоем оксида, предохраняющим его от дальнейшего окисления. При нагревании цинк реагирует с простыми веществами (исключением является азот):
2Zn + О2  2ZnО
2ZnО
Zn + Сl2  ZnCl2
ZnCl2
3Zn + 2Р  Zn3Р2
Zn3Р2
Zn + S  ZnS
ZnS
а также с оксидами неметаллов и аммиаком:
3Zn + SO2  2ZnO + ZnS
2ZnO + ZnS
Zn + CO2  ZnO + CO
ZnO + CO
3Zn + 2NH3  Zn3N2 + 3H2
Zn3N2 + 3H2
При нагревании цинк окисляется под действием водяных паров:
Zn + H2O (пар)  ZnO + H2
ZnO + H2
Цинк реагирует с растворами кислот серной и соляной кислот, вытесняя из них водород:
Zn + 2HCl = ZnCl2 + H2
Zn + H2SO4 = ZnSO4 + H2
Как активный металл цинк реагирует с кислотами-окислителями:
Zn + 2H2SO4(конц.) = ZnSO4 + SO2 + 2H2O
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S + 4H2O
Zn + 4HNO3(конц.)→ Zn(NO4)2 + 2NO2 + 2H2O
4Zn + 10HNO3(оч. разб.) = 4Zn(NO3)2 + NH4NO3 + 3H2O
При сплавлении цинка с щелочами образуется цинкат:
Zn + 2NаОН(крист.)  Nа2ZnО2 + Н2
Nа2ZnО2 + Н2
Цинк хорошо растворяется в растворах щелочей:
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
В отличие от алюминия, цинк растворяется и в водном растворе аммиака:
Zn + 4NH3 + 2H2O = [Zn(NH3)4](OH)2 + H2
Цинк восстанавливает многие металлы из растворов их солей:
CuSO4 + Zn = Zn SO4 + Cu
Pb(NO3)2 + Zn = Zn(NO3)2 + Pb
4Zn + KNO3 + 7KOH = NН3 + 4K2ZnO2 + 2H2O
4Zn + 7NaOH + 6H2O + NaNO3 = 4Na2[Zn(OH)4] + NH3
3Zn + Na2SO3 + 8HCl = 3ZnCl2 + H2S + 2NaCl + 3H2O
Zn + NaNO3 + 2HCl = ZnCl2 + NaNO2 + H2O
II. Соединения цинка (соединения цинка ядовиты).
1) Оксид цинка.
Оксид цинка обладает амфотерными свойствами.
ZnO + 2HCl = ZnCl2 + H2O
ZnO + 2NaOH + H2O = Na2[Zn(OH)4]
ZnO + 2NaOH  Na2ZnO2 + H2O
Na2ZnO2 + H2O
ZnO + Na2O  Na2ZnO2
Na2ZnO2
ZnO + SiO2  ZnSiO3
ZnSiO3
ZnO + BaCO3  BaZnO2 + СО2
BaZnO2 + СО2
Цинк восстанавливают из оксидов действием сильных восстановителей:
ZnO + С(кокс)  Zn + СО
Zn + СО
ZnO + СО  Zn + СО2
Zn + СО2
2) Гидроксид цинка.
Гидроксид цинка обладает амфотерными свойствами.
Zn(OН)2 + 2HCl = ZnCl2 + 2H2O
Zn(OН)2 + 2NaOH  Na2ZnO2 + 2H2O
Na2ZnO2 + 2H2O
Zn(OН)2 + 2NaOH = Na2[Zn(OH)4]
2Zn(OН)2 + СО2 = (ZnOH)2СО3 + H2O
Zn(OН)2 + 4(NH3· H2O) = [Zn(NH3)4](OH)2
Гидроксид цинка термически неустойчив:
Zn(OН)2  ZnO + H2O
ZnO + H2O
3) Соли.
СaZnO2 + 4HCl (избыток) = CaCl2 + ZnCl2 + 2H2O
Na2ZnO2 + 2H2O = Zn(OH)2 + 2NaHCO3
Na2[Zn(OH)4] + 2CO2 = Zn(OH)2 + 2NaHCO3
Zn(NO3)2 + 4NaOH = Na2[Zn(OH)4] + 2NaNO3
2ZnSO4  2ZnO + 2SO2 + O2
2ZnO + 2SO2 + O2
2Zn(NO3)2 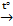 2ZnO + 4NO2 + O2
2ZnO + 4NO2 + O2
Zn(NO3)2 + Mg = Zn + Mg(NO3)2
ZnS + 4H2SO4(конц.) = ZnSO4 + 4SO2 + 4H2O
ZnS + 8HNO3(конц.) = ZnSO4 + 8NO2 + 4H2O
ZnS + 4NaOH + Br2 = Na2[Zn(OH)4] + S + 2NaBr
Цинк. Соединения цинка.
1. Оксид цинка растворили в растворе хлороводородной кислоты и раствор нейтрализовали, добавляя едкий натр. Выделившееся студенистое вещество белого цвета отделили и обработали избытком раствора щелочи, при этом осадок полностью растворился. нейтрализация полученного раствора кислотой, например, азотной, приводит к повторному образованию студенистого осадка. Напишите уравнения описанных реакций.
2. Цинк растворили в очень разбавленной азотной кислоте и в полученный раствор добавили избыток щелочи, получив прозрачный раствор. Напишите уравнения описанных реакций.
3. Соль, полученную при взаимодействии оксида цинка с серной кислотой, прокалили при температуре 800°С. Твердый продукт реакции обработали концентрированным раствором щелочи, и через полученный раствор пропустили углекислый газ. Напишите уравнения описанных реакций.
4. Нитрат цинка прокалили, продукт реакции при нагревании обработали раствором едкого натра. Через образовавшийся раствор пропустили углекислый газ до прекращения выделения осадка, после чего обработали избытком концентрированного нашатырного спирта, при этом осадок растворился. Напишите уравнения описанных реакций.
5. Цинк растворили в очень разбавленной азотной кислоте, полученный раствор осторожно выпарили и остаток прокалили. Продукты реакции смешали с коксом и нагрели. Напишите уравнения описанных реакций.
6. Несколько гранул цинка растворили при нагревании в растворе едкого натра. В полученный раствор небольшими порциями добавляли азотную кислоту до образования осадка. Осадок отделили, растворили в разбавленной азотной кислоте, раствор осторожно выпарили и остаток прокалили. Напишите уравнения описанных реакций.
7. В концентрированную серную кислоту добавили металлический цинк. образовавшуюся соль выделили, растворили в воде и в раствор добавили нитрат бария. После отделения осадка в раствор внесли магниевую стружку, раствор профильтровали, фильтрат выпарили и прокалили. Напишите уравнения описанных реакций.
8. Сульфид цинка подвергли обжигу. Полученное твердое вещество полностью прореагировало с раствором гидроксида калия. Через полученный раствор пропустили углекислый газ до выпадения осадка. Осадок растворили в соляной кислоте. Напишите уравнения описанных реакций.
9. Некоторое количество сульфида цинка разделили на две части. Одну из них обработали соляной кислотой, а другую подвергли обжигу на воздухе. При взаимодействии выделившихся газов образовалось простое вещество. Это вещество нагрели с концентрированной азотной кислотой, причем выделился бурый газ. Напишите уравнения описанных реакций.
10. Цинк растворили в растворе гидроксида калия. Выделившийся газ прореагировал с литием, а к полученному раствору по каплям добавили соляную кислоту до прекращения выпадения осадка. Его отфильтровали и прокалили. Напишите уравнения описанных реакций.
1) ZnO + 2HCl = ZnCl2 + H2O
ZnCl2 + 2NaOH = Zn(OH)2↓ + 2NaCl
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4]
Na2[Zn(OH)4] + 2HNO3(недостаток) = Zn(OH)2↓ + 2NaNO3 + 2H2O
2) 4Zn + 10HNO3 = 4Zn(NO3)2 + NH4NO3 + 3H2O
HNO3 + NaOH = NaNO3 + H2O
NH4NO3 + NaOH = NaNO3 + NH3↑ + H2O
Zn(NO3)2 + 4NaOH = Na2[Zn(OH)4] + 2NaNO3
3) ZnO + H2SO4 = ZnSO4 + H2O
2ZnSO4  2ZnO + 2SO2 + O2
2ZnO + 2SO2 + O2
ZnO + 2NaOH + H2O = Na2[Zn(OH)4]
Na2[Zn(OH)4] + 2CO2 = Zn(OH)2↓ + 2NaHCO3
4) 2Zn(NO3)2 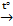 2ZnO + 4NO2 + O2
2ZnO + 4NO2 + O2
ZnO + 2NaOH + H2O = Na2[Zn(OH)4]
Na2[Zn(OH)4] + 2CO2 = Zn(OH)2↓ + 2NaHCO3
Zn(OH)2 + 4(NH3 · H2O) = [Zn(NH3)4](OH)2 + 4H2O
5) 4Zn + 10HNO3 = 4Zn(NO3)2 + NH4NO3 + 3H2O
2Zn(NO3)2 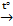 2ZnO + 4NO2 + O2
2ZnO + 4NO2 + O2
NH4NO3  N2O + 2H2O
N2O + 2H2O
ZnO + C 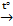 Zn + CO
Zn + CO
6) Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2↑
Na2[Zn(OH)4] + 2HNO3 = Zn(OH)2↓ + 2NaNO3 + 2H2O
Zn(OH)2 + 2HNO3 = Zn(NO3)2 + 2H2O
2Zn(NO3)2 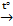 2ZnO + 4NO2 + O2
2ZnO + 4NO2 + O2
7) 4Zn + 5H2SO4 = 4ZnSO4 + H2S↑ + 4H2O
ZnSO4 + Ba(NO3)2 = Zn(NO3)2 + BaSO4
Zn(NO3)2 + Mg = Zn + Mg(NO3)2
2Mg(NO3)2  2Mg(NO2)2 + O2↑
2Mg(NO2)2 + O2↑
8) 2ZnS + 3O2 = 2ZnO + 2SO2↑
ZnO + 2NaOH + H2O = Na2[Zn(OH)4]
Na2[Zn(OH)4] + CO2 = Zn(OH)2 + Na2CO3 + H2O
Zn(OH)2 + 2HCl = ZnCl2 + 2H2O
9) ZnS + 2HCl = ZnCl2 + H2S↑
2ZnS + 3O2 = 2ZnO + 2SO2↑
2H2S + SO2 = 3S + 2H2O
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O
10) Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
H2 + 2Li = 2LiH
K2[Zn(OH)4] + 2HCl = 2KCl + Zn(OH)2↓
Zn(OH)2  ZnO + H2O
ZnO + H2O
 2020-06-29
2020-06-29 444
444








