Физические свойства галогенопроизводных зависят от строения радикала, вида и количества атомов галогена в молекуле. Большинство их обладают специфическим, часто резким запахом, раздражающим слизистую оболочку, некоторые обладают анестезирующим действием (CH2Cℓ2), токсичны, являются антисептиками (CHJ3).
Химические свойства галогеналканов определяются присутствием в молекуле атома галогена. Последний образует с атомом углерода простую σ-связь, которая в отличие от неполярных или особо полярных С – С и С – Н-связей, как правило, заметно поляризо-вана, и электронная плотность смещена к более электроотрицательному атому галогена. Очевидно, что большинство реакций галогенопроизводных связано с разрывом связи:
-Сδ+ -Гδ-.
На полярность связи влияют как природа атома галогена (чем больше ЭО галогена, тем полярнее связь), так и величина и строение углеводородного радикала. На связанном с галогеном углеродном атоме возникает частичный положительный заряд. Поэтому он подвергается действию нуклеофильных реагентов, предоставляющих свою электронную пару для образования новой связи. Подавляющее большинство реакций галогеналканов, широко используемых в органическом синтезе, связано с нуклеофильной атакой электронодефицитного атома углерода и замещением галогена на остаток нуклеофила.
Практика показывает, что в подобных реакциях наименее реакционноспособными оказываются фторпроизводные. Атом фтора очень компактен благодаря маленькому радиусу. При этом, хотя связь С – F наиболее полярная, она также самая короткая и прочная. Поэтому у фторпроизводных легче разорвать связь С – С, нежели С – F. Отсюда многие нижеперечисленные свойства характерны не для фторалканов, а для йод-, бром- и хлорпроизводных. Среди упомянутых производных наибольшую активность проявляют йодзамещенные. Это объясняется наименьшей среди галогенов электроотрицательностью атома йода; его оболочка будучи достаточно большой, легко деформируется под внешним воздействием, то есть связь С – J легко поляризуется. Именно фактор поляризуемости оказывается решающим для химического поведения галогеналканов во многих реакциях.
Для галогеналканов характерны реакции нуклеофильного замещения, отщепления галогеноводородов (элиминирование) с образованием алкенов, взаимодействие с металлами (получение металлорганических соединений), восстановление (образование алкенов). В органическом синтезе особенно широко распространены реакции замещения, позволяющие получать на основе галогеналканов самые разнообразные органические соединения.
Реакции нуклеофильного замещения. Примерами реакций замещения могут служить следующие превращения
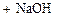

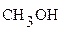
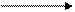
метанол 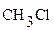

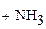
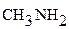

метиламин
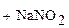
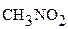

нитрометан
Реагенты (OH-, J-, CN-, NO2-, NH3) называются нуклеофильными (от греческого слова «нуклеус»- ядро), а реакции замещения, протекающие с их участием, - реакциями нуклеофильного замещения. Реакция обнаруживает целый ряд особенностей. Оказывается, в частности, что лёгкость реакции необычным образом зависит от строения исходного галогеналкана. А именно, наиболее реакционноспособными являются третичные соединения, затем следуют первичные, наименьшую активность проявляют вторичные галогеналканы
R
׀
R-С-Г > R-CH2-Г > R – CH-Г.
׀
R
В значительной мере на реакционную способность алкилгалогенидов влияет природа галогена. Реакционная способность падает и в ряду R–J > R–Br > R–Cℓ > R–F,так как увеличивается энергия связи и уменьшается её поляризуемость. Очевидно, чем прочнее связь, тем труднее её разорвать.
Дегидрогалогенирование галогеналканов. Галогеналкилы под действием спиртовых растворов щелочей отщепляют галогеноводороды с образованием непредельных соединений (см. получение алкенов)
спиртовый р-р
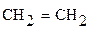
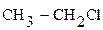 щёлочи
щёлочи

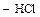
хлористый этил этилен
Реакции отщепления протекают в соответствии с правилом А. М. Зайцева.
 2014-02-02
2014-02-02 2457
2457








