Масса кристаллической фазы (G т) определяется из материального баланса кристаллизации по сумме массы растворенного вещества и растворителя (уравнение (5.1)) и по массе растворенного вещества (уравнение (5.2)):
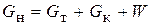 , (5.1)
, (5.1) 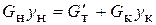 , (5.2)
, (5.2)
где 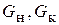 - расход соответственно начального и конечного (маточного) растворов, кг/с;
- расход соответственно начального и конечного (маточного) растворов, кг/с; 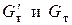 - расход соответственно кристаллической фазы в перерасчете на растворенное вещество и кристаллической фазы, включающей растворитель (кристаллосольвата или кристаллогидрата, если растворитель вода), кг/с; W - расход удаляемого растворителя, кг/с; у н и у к - концентрация соответственно начального и конечного (маточного) растворов, масс. доли.
- расход соответственно кристаллической фазы в перерасчете на растворенное вещество и кристаллической фазы, включающей растворитель (кристаллосольвата или кристаллогидрата, если растворитель вода), кг/с; W - расход удаляемого растворителя, кг/с; у н и у к - концентрация соответственно начального и конечного (маточного) растворов, масс. доли.
Ввиду того что число молей в кристаллической фазе в форме кристаллосольвата и без растворителя одно и то же, расход безводной кристаллической фазы 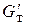 может быть выражен через расход кристаллосольвата:
может быть выражен через расход кристаллосольвата:
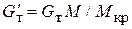 , (5.3)
, (5.3)
где 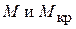 - молекулярная масса соответственно кристаллов без растворителя и кристаллосольвата.
- молекулярная масса соответственно кристаллов без растворителя и кристаллосольвата.
Из уравнений (5.1)- (5.3) получают расход кристаллической фазы:
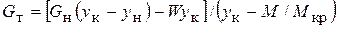 . (5.4)
. (5.4)
Если кристаллическая фаза не включает растворитель (т.е. 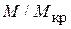 =1), уравнение (5.4) приобретает вид
=1), уравнение (5.4) приобретает вид
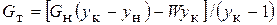 . (5.5)
. (5.5)
В случае изогидрической кристаллизации (W =0) уравнение (5.3) принимает вид
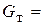
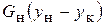 /
/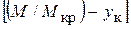 . (5.6)
. (5.6)
При 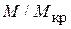 =1 получим
=1 получим
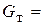
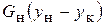 /
/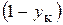 . (5.7)
. (5.7)
Уравнение теплового баланса кристаллизации имеет различные составляющие в случаях изотермической и изогидрической кристаллизации. При изотермической кристаллизации его составляют аналогично уравнению баланса теплоты при выпаривании:
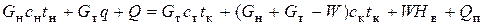 , (5.8)
, (5.8)
где с н, с к, с т, кДж/(кг·К)- теплоемкость соответственно начального, маточного раствора и кристаллов; t н, t к, оС- температуры соответственно начального и маточного растворов; q – теплота кристаллизации, кДж/кг; Q - приход теплоты с теплоносителем, Вт; Q п - потери теплоты, Вт; Н в - энтальпия вторичных паров, Дж/кг.
Если в качестве нагревающего агента используется насыщенный водяной пар, то с помощью уравнения (5.8) можно определить его расход D [с учетом того, что 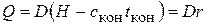 ]:
]:
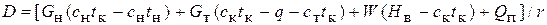 . (5.8а)
. (5.8а)
Здесь Н в и r – соответственно энтальпия и теплота конденсации водяного пара; 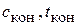 - соответственно теплоемкость и температура конденсата.
- соответственно теплоемкость и температура конденсата.
В случае изогидрической кристаллизации (W =0) тепловой баланс имеет следующий вид:
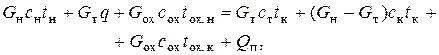 (5.9)
(5.9)
где 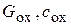 - соответственно расход и теплоемкость охлаждающей жидкости;
- соответственно расход и теплоемкость охлаждающей жидкости; 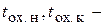 соответственно начальная и конечная температуры охлаждающей жидкости.
соответственно начальная и конечная температуры охлаждающей жидкости.
Тогда расход охлаждающей жидкости будет определяться по формуле
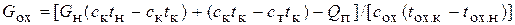 . (5.10)
. (5.10)
 2014-02-09
2014-02-09 1610
1610