



|
 |  |  |
1.  По числу атомов водорода (основности):
По числу атомов водорода (основности):
 |
HCl H2CO3 H3PO4
2. По наличию атомов кислорода:
|
|
HBr H2SO4
3. По степени растворимости в воде:
 |  |
HNO3 H2SiO3
4. По степени диссоциации (α):
 | 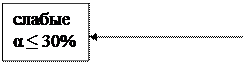 |
 Необходимо запомнить 7 сильных кислот и 16 слабых, а также названия их анионов.
Необходимо запомнить 7 сильных кислот и 16 слабых, а также названия их анионов.
Таблица 1 – Классификация кислот по степени диссоциации
| Формула кислоты | Название кислоты | Название солей |
| Сильные кислоты | ||
| H2SO4 | Серная | Сульфаты |
| HNO3 | Азотная | Нитраты |
| HCl | Соляная (хлороводородная) | Хлориды |
| HBr | Бромоводородная | Бромиды |
| HI | Йодоводородная | Йодиды |
| HClO4 | Хлорная | Перхлораты |
| HMnO4 | Марганцовая | Перманганаты |
| Слабые кислоты | ||
| H2SO3 | Сернистая | Сульфиты |
| HNO2 | Азотистая | Нитриты |
| Окончание таблицы 1 | ||
| Формула кислоты | Название кислоты | Название солей |
| HF (H2F2) | Димер плавиковой кислоты, Фтороводородная | Фториды |
| H2S | Сероводородная | Сульфиды |
| H2CO3 | Угольная | Карбонаты |
| H2SiO3 | Метакремниевая | Метасиликаты |
| H4SiO4 | Ортокремниевая | Ортосиликаты |
| H3PO4 | Ортофосфорная | ортофосфаты |
| HPO3 | Метафосфорная | Метафосфаты |
| HPO2 | Метафосфористая | Метафосфиты |
| H3PO3 | Ортофосфористая | Ортофосфиты |
| HCN | Синильная | Цианиды |
| H2CrO4 | Хромовая | Хроматы |
| H2Cr2O7 | Двухромовая | Дихроматы |
| CH3COOH | Уксусная | Ацетаты |
| HCOOH | Муравьиная | Формиаты |
Химические свойства кислот:
1) с основаниями: H2SO4 + 2 NaOH → Na2SO4 + 2 H2O;
2) с основными оксидами: H2SO4 + CuO → CuSO4 + H2O;
3) с металлами (до Н) HCl и разб. H2SO4: 2 HCl + Zn → ZnCl2 + H2;
4) с солями слабых и летучих кислот: 2 HCl+Na2CO3 → 2 NaCl+H2O+CO2


 3. Основания и амфотерные гидроксиды
3. Основания и амфотерные гидроксиды
Основания и амфотерные гидроксиды ● соединения,состоящие из атомов металлов и одной или нескольких гидроксильных групп (ОН−1)
Основания ● электролиты, которые при растворении в воде диссоциируют на анионы гидроксильных групп (ОН−1) и катионы металлов
Амфотерные гидроксиды ● электролиты, которые диссоциируют либо по типу кислоты, либо по типу основания
 |
 2015-01-07
2015-01-07 854
854








