Условие: Представить бутанол С4Н9ОН как вещество сложного элементного состава. Определить объем и состав в объемных % продуктов горения, образовавшихся при сгорании 1 кг этого вещества. Начальная температура окружающей среды 300С, давление 95 кПа, коэффициент избытка воздуха a = 1,4.
Решение:
1. Вычислим массовые доли элементов в веществе:
Молярная масса бутанола составляет
М(С4Н10О) = 12×4 + 10 + 16 = 74 кг/кмоль
w (С) = 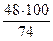 = 64,9 %;
= 64,9 %;
w (Н) = 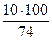 = 13,5 %;
= 13,5 %;
w (О) = 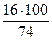 = 21,6 %.
= 21,6 %.
2. Условия отличаются от нормальных, следовательно, необходимо определить, какой объем будет занимать 1 кмоль любого газообразного вещества при данных условиях (расчет VМ).
Для заданных в задаче условий:
VМ = 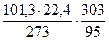 = 26,5 м3/кмоль.
= 26,5 м3/кмоль.
3. Вычислим число киломолей каждого компонента продуктов горения.
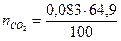 = 0,053 кмоль
= 0,053 кмоль
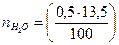 = 0,0675 кмоль
= 0,0675 кмоль
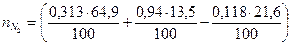 = 0,305 кмоль
= 0,305 кмоль
В состав продуктов горения входит избыточный воздух
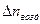 = 0,0119×
= 0,0119× 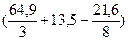 × (1,4 – 1) = 0,154 кмоль
× (1,4 – 1) = 0,154 кмоль
n(ПГ) = 0,053 + 0,0675 + 0,305 + 0,154 = 0,580 кмоль
4. Суммарный объем продуктов горения составит:
V(ПГ) = n(ПГ)× VМ = 0,580 × 26,5 = 15,4 м3
5. Процентный состав продуктов горения
j (СО2) = 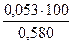 = 9,2 %;
= 9,2 %;
j (Н2О) = 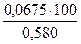 = 11,6 %;
= 11,6 %;
j (N2) = 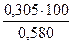 = 52,6 %;
= 52,6 %;
j (D возд) = 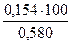 = 26,6 %
= 26,6 %
Ответ: объем продуктов горения бутанола при заданных условиях составляет 15,4 м3/кг; объемные доли продуктов горения составляют:
j (СО2) = 9,2 %; j (Н2О) = 11,6 %; j (N2) = 52,6 %; j (D возд) = 26,6 %.
 2015-03-27
2015-03-27 1909
1909
