pH = – lg [4,47 ⋅ 10-5]
pH = 5 – lg 4,47
pH =4,35
Ответ:
pH раствора 4,35.
Вычислите концентрацию ионов
Вычислите концентрацию ионов (ОН-) водного раствора, имеющего значение pH = 8,2.
Решение задачи
Из соотношения:
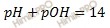
Находим:
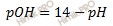
pOH – показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:
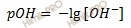
Используя, формулу, вычислите концентрацию ионов:
pOH = 14 – 8,2 = 5,8
Отсюда:
- lg [OH-] = 5,8
Вычислите концентрацию ионов:
[OH-] = 10-5,8 = 0,0000016 = 1,6 ⋅ 10-6 (моль/л).
Ответ:
концентрацию ионов (ОН-)водного раствора равна 1,6 ⋅ 10-6 моль/л.
Концентрация уксусной кислоты
Рассчитайте концентрацию уксусной кислоты (CH3COOH) в винном уксусе (рН=2,80), полагая, что кислотность определяется только уксусной кислотой (CH3COOH).
Решение задачи
Запишем уравнение диссоциации уксусной кислоты (CH3COOH):
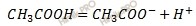
Водородный показатель (pH) раствора численно равен отрицательному десятичному логарифму концентрации ионов водорода в этом растворе.
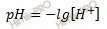
Используя, формулу, найдем концентрацию ионов водорода (H+):
-lg С(H+) = 2,8
С(H+) = 10-2,8 = 0,0016 (моль/л).
Учитывая, что концентрация уксусной кислоты (CH3COOH) равна концентрации ионов водорода (смотри уравнение диссоциации уксусной кислоты), следовательно, концентрация уксусной кислоты (CH3COOH) равна 0,0016 моль/л.
Ответ:
концентрация уксусной кислоты 0,0016 моль/л.
Раствор карбоната натрия (pH раствора)
Определить pH раствора карбоната натрия (Na2CO3) с молярной концентрацией эквивалента 0,02 моль-экв/л.
 2015-05-26
2015-05-26 11176
11176








