Автор: студент, Неизвестен, Неизвестен. Тип материала: Учебное пособие
Найдем молярную концентрацию уксусной кислоты (CH3COOH). Для этого будем использовать формулу перехода от массовой доли к молярности:
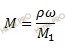
Где:
ρ — плотность раствора, г/л;
ω — массовая доля растворенного вещества в долях от 1;
M1 — молярная масса растворенного вещества, г/моль.
Вычислить pH
Молярная концентрация показывает количество растворенного вещества (моль), содержащегося в 1 л раствора.
Учитывая, что молярная масса уксусной кислоты (CH3COOH) равна 60 г/моль (смотри таблицу Менделеева) и если раствор 1-процентный, то массовая доля уксусной кислоты (CH3COOH) в нем 0,01 получаем:
M = 1000 ⋅ 0,01 /60 = 0,17 (моль/л).
Вычислить pH
Учитывая, что уксусная кислота (CH3COOH) – это слабая одноосновная кислота, найдем равновесную концентрацию ионов водорода по формуле:
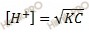
Где:
K – константа диссоциации кислоты;
C – молярная концентрация кислоты.
Получаем:
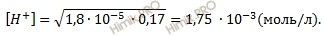
Вычислить pH раствора по формуле:
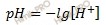
Водородный показатель (pH) раствора численно равен отрицательному десятичному логарифму концентрации ионов водорода в этом растворе.
pH = – lg [1,75 ⋅ 10-3]
pH = 3 – lg 1,75
pH = 2,76
Ответ:
pH раствора 2,76.
Рассчитать pH
Рассчитать рН 0,04 М раствора хлорноватистой кислоты (HClO).
Решение задачи
Запишем уравнение диссоциации хлорноватистой кислоты (HClO):
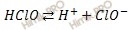
Учитывая, что хлорноватистая кислота (HClO) – это очень слабая одноосновная кислота, которая существует лишь в растворах, найдем равновесную концентрацию ионов водорода по формуле:
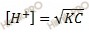
Где:
K – константа диссоциации кислоты;
C – молярная концентрация кислоты.
Получаем:
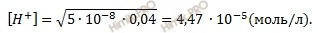
Константа диссоциации хлорноватистой кислоты (HClO) равна 5 ⋅ 10-8(смотри таблицу Константы диссоциации).
Рассчитать pH раствора по формуле:
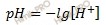
Водородный показатель (pH) раствора численно равен отрицательному десятичному логарифму концентрации ионов водорода в этом растворе.
 2015-05-26
2015-05-26 57673
57673







