В водных растворах сильные электролиты обычно полностью диссоциированы. В несильно разбавленных растворах сильных электролитов среднее расстояние между ионами вследствие значительной концентрации мало. В таких растворах ионы не вполне свободны, движение их стеснено взаимным притяжением друг другу.
Вследствие этого притяжения каждый ион как бы окружен шарообразным роем противоположно заряженных ионов, получившим название «ионной атмосферы».
В отсутствие внешнего электрического поля ионная атмосфера симметрична и силы, действующие на центральный ион, взаимно уравновешиваются. Если же приложить к раствору постоянное электрическое поле, то разноименно заряженные ионы будут перемещаться в противоположных направлениях. При этом каждый ион стремится двигаться в одну сторону, а окружающая его ионная атмосфера – в противоположную, вследствие чего уменьшается сила тока.
Чем больше концентрация раствора, тем сильнее проявляется тормозящее действие ионной атмосферы на электропроводность раствора, о чем свидетельствуют следующие данные:
| СKCl, н | 0,01 | 0,1 | ||
| α, % | 94,2 | 86,2 | 75,6 | 71,2 |
Однако падение α объясняется не образованием молекул, а увеличением тормозящего действия ионной атмосферы. В связи с этим α сильных электролитов называется кажущейся степенью диссоциации.
Для оценки состояния ионов в растворе пользуются величиной, называемой активностью.
Под активностью иона понимают ту эффективную концентрацию его, соответственно которой он действует при химических реакциях. Активность иона а равна произведению его моляльной концентрации (Сm) на коэффициент активности (f):
a = f∙Cm
Коэффициенты активности различных ионов различны. Они изменяются с изменением концентрации растворов. В концентрированных растворах f<1, а с разбавлением раствора f→1. Если f<1, то это указывает на сильное межионное взаимодействие, если f≈1, то это свидетельствует о слабом межионном взаимодействии (приложение, табл. 2).
Коэффициенты активности ионов зависят от состава и концентрации раствора, от заряда и природы иона и от других условий.
В разбавленных растворах природа иона мало влияет на значение f. Поэтому приближенно можно считать, что в разбавленных растворах коэффициент активности иона в данном растворителе зависит только от заряда иона и ионной силы раствора I, которая равна полусумме произведений концентрации Cm каждого иона на квадрат его заряда z:
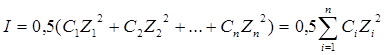
Приближенно коэффициент активности иона в разбавленном растворе можно также вычислить по формуле
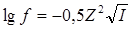 (табл. 2).
(табл. 2).
 2015-05-26
2015-05-26 1574
1574
