У больных циррозом печени часто обнаруживаются лейкопения и тромбоцитопения, обычно в сочетании с незначительной анемией {гиперспленизм).
Лейкоциты
Отмечается лейкопения в пределах 1,5—3,0•109/л, в основном уменьшается количество полиморфноядерных клеток. Иногда лейкопения бывает более выраженной.
Холангит, фульминантный гепатит, алкогольный гепатит, абсцесс печени и онкологические заболевания сопровождаются лейкоцитозом. Последний также наблюдается при внепеченочных опухолях, вырабатывающих колониестимулирующий фактор, что может сочетаться с поражением печени |32|. При вирусных инфекциях, например при инфекционном мононуклеозе и вирусном гепатите, в периферической крови выявляются атипичные лимфоциты.
Тромбоциты
При всех формах заболеваний печени наблюдаются сходные отклонения в количестве, структуре и функции тромбоцитов.
У больных с портальной гипертензией тромбоцитопения, редко тяжёлая, является следствием усиления секвестрации клеток в селезёнке. Это вызвано значительным повышением селезёночного пула тромбоцитов. Разрушение тромбоцитов при этом минимальное. Т1/2 тромбоцитов остаётся в пределах нормы, объём их уменьшается [15]. Аналогичные гематологические изменения встречаются при тромбозе портальной вены и других заболеваниях, сопровождающихся спленомегалией.
У части больных может отмечаться повышенное разрушение тромбоцитов. Антитромбоцитарные IgG выявляются при хроническом вирусном гепатите, в частности при гепатите С (в 88% случаев) и гепатите В (в 47% случаев) [21]. Количество антител коррелирует со степенью тромбоцитопении.
У больных циррозом печени, в частности группы С по Чайлду, нарушена функция тромбоцитов, особенно агрегация. При этом происходит нарушение потребления арахидоновой кислоты, необходимой для синтеза простагландинов [231, а также снижение содержания в тромбоцитах АТФ и 5-гидрокситриптамина |17|.
Нарушение агрегации тромбоцитов вследствие диссеминированного внутрисосудистого свёртывания может играть важную роль в патогенезе тяжёлой печёночной недостаточности.
Снижение образования тромбоцитов костным мозгом может быть обусловлено избыточным употреблением алкоголя, дефицитом фолиевой кислоты и вирусным гепатитом.
Тромбоцитопения (обычно в пределах 60,0—90,0•109/л) при хронических заболеваниях печени встречается чрезвычайно часто и в основном обусловлена гиперспленизмом. Она проявляется клинически очень редко. Если состояние больного от лейкопении и тромбоцитопении не страдает, селезёнку не следует удалять; для принятия решения о спленэктомии факт наличия уменьшенного количества тромбоцитов и лейкоцитов сам по себе недостаточен. Если функция циркулирующих, хотя и в недостаточном количестве, лейкоцитов и тромбоцитов не нарушена в отличие от таковой у больных лейкозом, то спленэктомия противопоказана. Послеоперационная смертность больных с заболеваниями печени высокая. Сама операция может осложниться тромбозом воротной и селезёночной вен. А это в свою очередь требует проведения последующих оперативных вмешательств на воротной вене, которые могут осложнить осуществление трансплантации печени.
Печень и свёртывающая система крови
[20, 25. 36]
Механизмы нарушений свёртывания крови при болезнях печени и жёлчных путей очень сложны. Это является следствием изменений пути как образования фибрина, так и его распада — фибринолиза (рис. 4-2, табл. 4-1). Об изменениях количества и функций тромбоцитов говорилось в предыдущем разделе. Конечным результатом этих нарушений, несмотря на всю их сложность, становится гипокоагуляция, что требует терапевтического вмешательства в случае кровотечения или при планировании проведения какой-либо процедуры, чреватой кровотечением.
Гепатоцит является основным местом синтеза всех белков свёртывающей системы, за исключением фактора Виллебранда и фактора VIII С. К этим белкам относятся витамин К-зависимые факторы II, VII, IX и X, а также лабильный фактор V, фактор VIII, контактные факторы XI и XII, фибриноген и фибринстабилизирующий фактор XIII. Т1/2 всех перечисленных выше белков системы свёртывания очень короткий. Отсюда следует, что острый некроз печёночных клеток может быстро привести к снижению уровня этих белков. Наиболее заметно падает концентрация фактора VII, ^ которого составляет 100-300 мин.
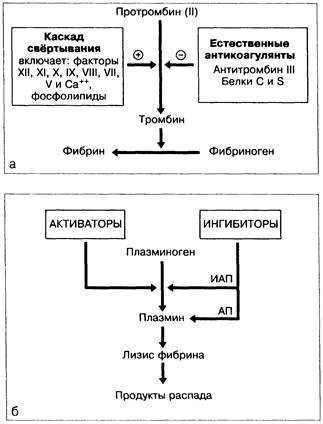
Рис. 4-2. Нормальные пути свёртывания крови (а) и фибринолиза (б). При заболеваниях печени могут поражаться практически все этапы этого процесса. ИАП — ингибитор активатора плазминогена; АП — антиплазмин.
Таблица 4-1. Влияние заболеваний печени на гемостаз
Снижение синтеза факторов свёртывания: нарушение функции печени недостаточность/нарушение всасывания витамина К
Снижение синтеза ингибиторов свёртывания: образование аномальных/ неполноценных белков повышение фибринолитической активности уменьшение выведения активаторов фибринолиза уменьшение образования ингибиторов фибринолиза уменьшение выведения печенью активированных факторов свёртывания
Диссеминированное внутрисосудистое свёртывание: многофакторное, в том числе эндотоксемия нарушения тромбоцитарного звена гемостаза уменьшение количества тромбоцитов нарушение функции тромбоцитов
Витамин К — жирорастворимый витамин, вырабатываемый кишечными бактериями. Наиболее частой причиной его недостаточности является внутри- и внепеченочный холестаз, однако снижение его концентрации может быть также обусловлено лечением хелаторами жёлчных кислот (холестирамин) или перорально применяемыми антибиотиками. Витамин К-зависимые белки синтезируются в зернистой эндоплазматической сети. На своём азотистом конце они содержат несколько остатков глутаминовой кислоты, которые должны после этапа синтеза на рибосомах с участием фермента карбоксилазы трансформироваться в g-карбоксиглутаминовую кислоту. Для функционирования карбоксилазы необходим витамин К [12]. Функция белков свёртывания зависит от этой конверсии. При холестазе парентеральная заместительная терапия витамином К быстро (в течение 24—48 ч) восстанавливает до нормы протромбиновое время и используется в диагностических целях. Если коагулопатия является следствием болезни печени, протромбиновое время может улучшиться, но не нормализуется.
Ингибиторы, влияющие на каскад свёртывания, также синтезируются печенью. К ним относятся антитромбин III, белки С и S и кофактор II гепарина. Белки С и S являются витамин К-зависимыми. При фульминантной печёночной недостаточности [18] и циррозе печени [2] количество этих ингибиторов уменьшено, однако их недостаточность не приводит к тромбозам, возможно, вследствие других изменений в системе свёртывания крови. При гомозиготной недостаточности белка С прибегают к трансплантации печени [8].
Болезни печени могут сопровождаться образованием структурно и функционально неполноценных белков и факторов свёртывания. Особенно часто при циррозе, хроническом гепатите и острой печёночной недостаточности обнаруживается дисфибриногенемия. Фибриноген может содержать избыток остатков сиаловой кислоты. Считается, что последние приводят к нарушению полимеризации фибриновых мономеров. Может также выявляться фибриноген с низкой молекулярной массой. Аномалии фибриногена у многих больных с заболеваниями печени вызывают увеличение протромбинового времени (ПВ). Это увеличение можно заподозрить при повышении частичного тромбопластинового времени (ЧТВ) в сочетании с нормальным содержанием фибриногена и при отсутствии нарастания продуктов его распада.
У больных с заболеваниями печени обнаруживается усиление фибринолитической активности. В 1914 г. Гудпасчер впервые описал ускоренный лизис сгустка крови у больных циррозом печени. Гепатоциты синтезируют плазминоген и ингибиторы плазмина, такие как a2-антиплазмин и ингибиторы тканевого активатора плазминогена (ТАП-1). У больных циррозом печени отмечается уменьшение количества антигена ингибитора ТАП-1 даже без признаков активации свёртывания (повышение отношения фибрин/продукты распада фибриногена; D-димеров) [35]. Считается, что повышение активности ТАП-1, относительно активности ингибитора ТАП-1 и a2-антиплазмина ведёт к повышению фибринолиза [19]. Больные с тяжёлым заболеванием печени и признаками гиперфибринолиза имеют более высокий риск кровотечения [34].
Вопрос о диссеминированном внутрисосудистом свёртывании крови (ДВС-синдром) у больных с циррозом печени, хроническим гепатитом и острым гепатитом был предметом дискуссий.
При заболеваниях печени могут быть комплексные изменения со стороны белков свёртывания, ингибиторов и фрагментов белков, обычно сочетающихся с ДВС-синдромом. Результаты исследования тромбин-антитромбиновых комплексов, растворимого фибрина, продуктов деградации фибрина и фибриногена (D-димер, D-мономер) позволяют предположить, что ДВС-синдром лёгкой степени участвует в патогенезе коагулопатии у некоторых больных с тяжёлыми заболеваниями печени [1, 16, 24]. К стимулирующим его механизмам относятся нарушение выведения активированных факторов свёртывания и эндотоксемия [33].
Независимо от исходного состояния у больных циррозом печени, однако имеется больший риск развития развёрнутого ДВС-синдрома по сравнению с больными с нормальной функцией печени, особенно при наличии сепсиса и артериальной гипотензии [6].
Асцитическая жидкость содержит мономеры фибрина, продукты его распада и небольшое количество фибриногена, что указывает на активный внутрибрюшинный процесс свёртывания. Фибринолиз, вызванный введением активаторов плазминогена, обусловливает коагулопатию [31], которая осложняет внутривенную инфузию асцитической жидкости, как при шунтировании по Левину.
Цирроз печени может также осложняться тромбозами. Предстоит выяснить взаимосвязь между антифосфолипидными антителами (волчаночный антикоагулянт, антикардиолипиновые антитела) у больных циррозом печени [29], снижением уровня естественных антикоагулянтов (антитромбин III, белки С и S) и тромботическими осложнениями.
Исследование свёртывания крови
Наиболее адекватный тест, выявляющий нарушение свёртывания крови у больных с поражением печени и жёлчных путей, — исследование ПВ до и после внутримышечного введения 10 мг витамина К. Этот тест является также наиболее достоверным показателем: он имеет прогностическое значение и позволяет судить о наличии печёночно-клеточного некроза. Иногда определяют ЧТВ, которое является более чувствительным показателем, чем ПВ. Его удлинение указывает на дефицит не только протромбинового комплекса, но и факторов XI и XII.
Необходимость исследования отдельных факторов свёртывания возникает редко, хотя уровень фактора V является прогностическим критерием у больных с фульминантной печёночной недостаточностью. Так, у больных с печёночной недостаточностью, вызванной интоксикацией парацетамолом, падение уровня фактора V ниже 10% при поступлении свидетельствует о плохом прогнозе [26]. Соотношение факторов VIII (содержание его повышено при заболевании печени) и V при поступлении также представляет клиническую ценность.
Исследуют также количество тромбоцитов. Определение времени кровотечения позволяет оценить роль количества и функции тромбоцитов в поддержании гемостаза.
Фибринолиз и ДВС-синдром диагностируют на основании значительного увеличения ПВ, снижения уровня фибриногена ниже 1 г/л, увеличения количества продуктов деградации фибриногена более 100 мкг/л и тромбоцитопении менее 100•109/л.
 2015-06-10
2015-06-10 866
866







