Вода является очень слабым амфотерным электролитом:
H2O «H+ + OH-; D H°» 56 кДж. (7.6.8.)
Свободные ионы водорода H+ не способны к существованию в водном растворе - они мгновенно гидратируются водой до гидратов переменного состава (H2n+1O n +). Однако, для простоты записи часто используют обозначение H+:
Константа диссоциации воды равна:
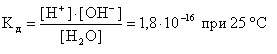 (7.6.9.)
(7.6.9.)
В воде и разбавленных водных растворах электролитов молярная концентрация воды практически постоянна и равна
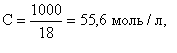
где 1000 - масса 1 л воды, г; 18 - молярная масса воды, г/моль.
 2015-06-14
2015-06-14 293
293








