Большинство оксидов галогенов неустойчивы и получаются косвенным путем, так как галогены с кислородом не взаимодействуют. Известны следующие оксиды галогенов (табл.6).
Таблица 6. Оксиды галогенов.
| Степень окисления | +1 | +4 | +5 | +6 | +7 |
| F | F2O | - | - | - | - |
| Сl | Cl2O | ClO2 | - | Cl2O6 | Cl2O7 |
| Br | Br2O | BrO2 | - | BrO3 | Br2O7 |
| I | - | I2O4 | I2O5 | - | I2O7 |
F2O (иногда его называют дифторидом кислорода) - бесцветный газ (т.пл. -2240С, т.кип. -1450С), который может быть получен при пропускании фтора через 2%-ный водный раствор NaOH: 2F2+ 2NaOH = F2О + 2NaF +H2O. Оксид хлора (I) Cl2O - желто-коричневый газ (т.пл. -1160С, т.кип. 40С).Его получают, пропуская ток хлора через трубку со свежеосажденным и затем высушенным оксидом ртути (II):2HgO + 2Cl2 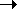 Hg2OСl2+ Cl2O.____Cl2O хорошо растворим в воде (при 0оС 1 об.H2O растворяет 200 об. Cl2O), его водный раствор проявляет свойства слабой кислоты:
Hg2OСl2+ Cl2O.____Cl2O хорошо растворим в воде (при 0оС 1 об.H2O растворяет 200 об. Cl2O), его водный раствор проявляет свойства слабой кислоты:
H2O + Cl2O = 2HClO. Оксид брома (I) Br2O напоминает по свойствам и методу синтеза Cl2O. Диоксиды ClO2и BrO2. Диоксид хлора ClO2при стандартных условиях - желтый газ (т.пл.-600С, т.кип. 100С). Это единственный из оксидов галогенов, который используется в промышленности, например, как отбеливающее вещество. В технике его получают пропусканием SO2в подкисленный раствор хлората натрия:
2NaClO3+ SO2+ H2SO4= 2NaHSO4+ 2ClO2. I2O4 - желтое кристаллическое вещество, построенное из ионов IO+и IO-3. При нагревании выше 1000С разлагается на I2и O2. Оксид хлора (VI) Cl2O6 - красная маслообразная жидкость (т.пл. 3.50С, т.кип. 2030С), взрывоопасная, легко разлагается на ClO2и O2. В твердой фазе построен из ионов 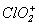 и
и 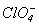 . Является смешанным ангидридом кислот HClO3и HClO4. ____Cl2O6+ H2O = HClO3+ HClO4. Оксид иода (V) I2O5 - белое твердое вещество (т.пл. 3000С), единственный термодинамически устойчивый из оксидов галогенов. Твердый оксид I2O5состоит из молекул O2IOIO2,, связанных между собой слабым межмолекулярным взаимодействием. Получают I2O5дегидратацией HIO3при 200-2500С в потоке сухого воздуха. I2O5 используется как окислитель в количественном анализе для определения СО:5СО + I2O5
. Является смешанным ангидридом кислот HClO3и HClO4. ____Cl2O6+ H2O = HClO3+ HClO4. Оксид иода (V) I2O5 - белое твердое вещество (т.пл. 3000С), единственный термодинамически устойчивый из оксидов галогенов. Твердый оксид I2O5состоит из молекул O2IOIO2,, связанных между собой слабым межмолекулярным взаимодействием. Получают I2O5дегидратацией HIO3при 200-2500С в потоке сухого воздуха. I2O5 используется как окислитель в количественном анализе для определения СО:5СО + I2O5 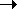 I2+ 5CO2. Оксид хлора (VII) Cl2O7 - маслянистая бесцветная жидкость (т.пл.-930С, т.кип. 800С), легко взрывается. Молекула Cl2O7построена из двух тетраэдров ClO4, имеющих общую вершину. Cl2O7- ангидрид хлорной кислоты HClO4. Его получают дегидратацией концентрированной хлорной кислоты с помощью P2O5с последующей осторожной перегонкой в вакууме:6HClO4+ P2O5
I2+ 5CO2. Оксид хлора (VII) Cl2O7 - маслянистая бесцветная жидкость (т.пл.-930С, т.кип. 800С), легко взрывается. Молекула Cl2O7построена из двух тетраэдров ClO4, имеющих общую вершину. Cl2O7- ангидрид хлорной кислоты HClO4. Его получают дегидратацией концентрированной хлорной кислоты с помощью P2O5с последующей осторожной перегонкой в вакууме:6HClO4+ P2O5 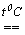 3Cl2O7+ 2H3PO4.
3Cl2O7+ 2H3PO4.
 2015-06-04
2015-06-04 3434
3434







