Рассчитаем рН а) 0,001 М раствора КОН и б) 0,01 М раствора HCl.
Согласно правилу «ионного произведения воды» для воды и разбавленных водных растворов произведение равновесных концентраций ионов водорода и гидроксид-ионов является величиной постоянной и при 298 К равно 10-14 моль/л, т.е. [H+]·[OH  ] = 10-14. В связи с тем, что концентрации ионов Н+ и ОН
] = 10-14. В связи с тем, что концентрации ионов Н+ и ОН  связаны между собой, среду (кислую, нейтральную и щелочную) выражают только через [H+]. Для простоты работы используется величина рН,
связаны между собой, среду (кислую, нейтральную и щелочную) выражают только через [H+]. Для простоты работы используется величина рН,
рН = – lg[H+].
Для кислой среды рН изменяется от 0 до 7, нейтральная среда имеет рН = 7, а щелочная от 7 до 14.
а) КОН диссоциирует на ионы:
КОН 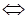 К+ + ОН
К+ + ОН  .
.
Считаем, что степень диссоциации составляет 100 %, тогда концентрация ионов ОН  равна концентрации раствора щелочи, то есть 10-3 М. Из правила «ионного произведения воды» определяем концентрацию ионов [H+]:
равна концентрации раствора щелочи, то есть 10-3 М. Из правила «ионного произведения воды» определяем концентрацию ионов [H+]:
[H+] = 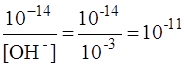 .
.
Определяем рН раствора: рН = -lg [H+] = -lg 10-11 = 11. рН > 7, среда щелочная;
б) по аналогии: HCl 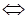 H+ + Cl
H+ + Cl  ;
;
[H+] = 10-2 М. рН = -lg [H+] = -lg 10-2 = 2. рН < 7, среда кислая.
Задание 5.3. Составить молекулярное и ионно-молекулярное уравнения реакций гидролиза 4-х солей и оценить рН раствора (табл. V.3):
а) соль образована слабым основанием и сильной кислотой;
б) соль образована сильным основанием и слабой кислотой;
в) соль образована слабым основанием и слабой кислотой;
г) соль образована сильным основанием и сильной кислотой.
 2015-06-05
2015-06-05 888
888








