Продолжительность доводки 0,82 ч, продолжительность продувки 0,72 ч. В течение доводки выгорает 1,5 – 0,1 = 14 кг углерода.
При продувке ванны 10% S, содержащейся в металле, окислится до SO2, т.е. 0,003 кг серы.
Принято, что фосфора остается в металлической ванне перед раскислением 0,012%.
Расход кислорода и количество окисляющихся примесей во время доводки отображен в таблице 19.
Таблица 19 − Расход кислорода и количество окислов в период доводки
| Окисление | Угар элементов, кг | Расход кислорода, кг | Масса окисла, кг |
| С → СО | 1,400 | 1,865 | 3,265 |
| Р → Р2О5 | 0,003 | 0,004 | 0,007 |
| S → SO2 | 0,003 | 0,003 | 0,006 |
| Fe → Fe2O3 | 0,600 | 0,257 | 0,857 |
| Итого | 2,006 | 2,129 | 4,135 |
Проверяем основность шлака после спуска из ванны части более кислого шлака и в случае необходимости определяем необходимую добавку извести.
Количество SiO2, вносимое материалами, кг:
1) Шлака 1 периода 0,594;
2) Доломита 0,008;
3) Магнезитохромита 0,006;
Итого: 0,608.
Количество СаО, вносимое материалами, кг:
1) Шлака 1 периода 1,547;
2) Доломита 0,4 · 0,55 = 0,220;
3) Магнезитохромита 0,1 · 0,02 = 0,002;
Итого: 1,769.
Основность шлака равна:
В = 1,769 / 0,608 = 2,92.
Такое повышение основности обусловлено тем, что со сбегающими шлаками из ванны уносится много кислотных окислов. Основность шлака достаточная, и доводку ведут без присадки извести. Количество окислов, переходящих в шлак, определено в таблице 13.
Примем содержание FeO и Fe2O3 в конечном шлаке равным соответственно 15 и 5% (базовый показатель 25 и 8%).
Количество шлака без окислов железа составляет 3,086 кг., что соответствует 80%, тогда количество конечного шлака II периода будет равняться:
3,086: 0,8 = 3,858 кг.
В том числе окислов железа, кг:
3,858 – 3,086 = 0,772.
Из них:
0,772 · 15: 20 = 0,579 кг FeO;
0,772 – 0,579 = 0,193 кг Fe2O3.
Должно получиться FeO за счет окисления железа:
0,579 – 0,534 = 0,046 кг.
Должно восстановиться Fe2O3:
0,211 – 0,193 – 0,018 кг,
где 0,534; 0,211 – соответственно количества FeO и Fe2O3..
Затрачивается кислорода на окисление железа до FeO:
0,046 · 16 /72 = 0,010 кг.
Окислится железа:
0,046 – 0,010 = 0,036 кг.
Выделится кислорода при восстановлении железа из Fe2O3:
0,018 · 48 / 160 = 0,005 кг.
В таблице 20 определим количество составляющих шлака.
Таблица 20 - Определение количества составляющих шлака, кг
| Источники | SiO2 | Al2O3 | MnO | MgO | CaO | P2O5 | S | Cr2O3 | FeO | Fe2O3 | Σ |
| Шлак1периода | 0,594 | 0,098 | 0,084 | 0,233 | 2,547 | 0,039 | 0,007 | 0,007 | 0,534 | 0,200 | 4,343 |
| Доломит* | 0,008 | 0,008 | - | 0,144 | 0,220 | - | - | - | - | 0,001 | 0,381 |
| Магнезито-хромит | 0,006 | 0,004 | - | 0,066 | 0,002 | - | - | 0,012 | - | 0,010 | 0,100 |
| Металличес-кая шихта | - | - | - | - | - | 0,007 | - | - | - | 0,007 | |
| Всего | 0,608 | 0,110 | 0,084 | 0,443 | 1,769 | 0,046 | 0,007 | 0,019 | 0,579 | 0,193 | 4,858 |
| % | 15,70 | 2,85 | 2,18 | 11,50 | 45,80 | 1,20 | 0,18 | 0,49 | 15,00 | 5,00 | 100,00 |
| Примечание - В доломите еще содержится 0,009 кг Н2О и 0,01 СО2 |
Должно восстановиться Fe2O3:
0,211 – 0,193 = 0,018 кг,
где 0,534; 0,211 – соответственно количества FeO и Fe2O3 (таблица 20).
Затрачивается кислорода на окисление железа до FeO:
0,046 · 16 /72 = 0,010 кг.
Окислится железа:
0,046 – 0,010 = 0,036 кг.
Выделится кислорода при восстановлении железа из Fe2O3:
0,018 · 48 /160 = 0,005 кг.
Восстановится железа:
0,018 – 0,005 = 0,013 кг.
Выход стали до раскисления с учетом запутавшегося в шлаке (3% количества конечного шлака):
92,999 – 2,006 – 0,036 + 0,013 + 0,041 – 0,115 = 90,896 кг.
Здесь содержание растворенного кислорода в стали определено по формуле Г.Н. Ойкса:
[%С] · [%О] = 0,0035 + 0,006 [%С], (7)
[%С] = 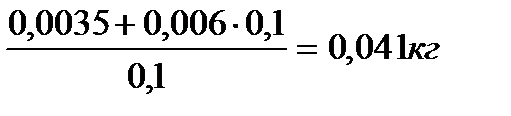 .
.
Поступит кислорода из атмосферы печи:
5 · 50 · 0,72 / 2500 = 0,09 кг.
Требуется кислорода:
2,129 + 0,10 – 0,005 + 0,041 – 0,09 = 2,085 кг.
Потребуется технического кислорода:
Vкисл техн = 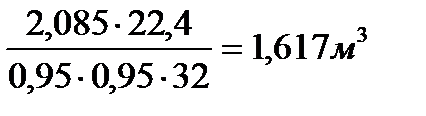 .
.
т.е. на 1 т металлической шихты расходуется 16,17 м3,
где 0,95 – коэффициент усвоения кислорода во II периоде.
Расход чистого кислорода:
2,085 · 22,4 / 32 = 1,46 м3.
С учетом усвоения расход чистого кислорода составит:
1,46 / 0,95 = 1,537 м3.
Количество неусвоенного кислорода:
1,537 – 1,46 = 0,077 м3, или 0,110 кг.
Количество азота:
1,617 – 1,537 = 0,080 м3, или 0,10 кг.
Количество технического кислорода равно:
2,085 + 0,110 + 0,1 = 2,295 кг.
Общий расход технического кислорода на 100 кг металлической шихты за оба периода равен 2,21 + 1,617 = 3,827 м3, или на 1 т металлической шихты 38,27 м3.
На 1 т стали расход технического кислорода составит:
38,27 / 0,919 = 41,64 м3/т.
Расход аргона на 100 кг металлошихты определяется из расчета 0,28 м3/т:
0,28 · 0,04 / 22,4 · 1000 = 0,0000005 кг.
В таблице 21 представлен материальный баланс II периода плавки.
Таблица 21 − Материальный баланс II периода плавки
| Поступило, кг | Получено, кг | ||
| Название | кг | Название | кг |
| Металла 1 периода | 92,999 | Стали | 90,896 |
| Шлака 1 периода | 4,343 | Металла в шлаке | 0,115 |
| Доломита | 0,400 | Шлака | 4,858 |
| Магнезитохромита | 0,100 | СО2 | 0,010 |
| Кислорода из атмосферы печи | 0,090 | СО | 3,265 |
| Технического кислорода | 2,295 | SO2 | 0,006 |
| Fe2O3 (в дым) | 0,857 | ||
| Азота | 0,100 | ||
| Неусвоенного кислорода | 0,110 | ||
| Н2О | 0,009 | ||
| Невязка | - 0,001 | ||
| Итого | 100,227 | 100,227 |
Материальный баланс всей плавки представлен в таблице 22.
Таблица 22 − Материальный баланс всей плавки
| Поступило, кг | Получено, кг | ||
| Металлической шихты | 100,000 | Стали | 90,896 |
| Известняка | 3,582 | Шлака | 9,858 |
| Доломита | 1,700 | Потери металла | 0,615 |
| Магнезитохромита | 0,200 | СО | 5,913 |
| Кислорода из атмосферы Печи | 0,350 | СО2 | 1,528 |
| Аргона | 0,5 · 10-5 | SO2 | 0,014 |
| Технического кислорода | 5,432 | Азота | 0,237 |
| Неусвоенного кислорода | 0,410 | ||
| H2O | 0,220 | ||
| Fe2O3 (в дым) | 1,571 | ||
| Невязка | - 0,002 | ||
| Итого | 111,264 | 111,264 |
 2015-06-24
2015-06-24 498
498








