1. Важнейшим свойством всех оснований является взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации).
НС1 + NaОН =NаС1 + н2О
Ионные уравнения:
Н+ + С1– + Na+ + ОН– = Na+ + с1– + н2О
Н + + ОН– = н2О
Таким образом, сущность реакции нейтрализации раствора сильной кислоты раствором щелочи заключается в соединении ионов Н+ и ОН- в недиссоциированные молекулы воды.
Слабая кислота, например, сероводородная, реагирует со щелочью потому, что продукт реакции вода, связывает ионы водорода более прочно, чем сероводородная кислотам
Н2S + 2 NaOH = Nа2S + 2H2O
Ионные уравнения:
Н2S + 2Nа+ + 2ОН– = 2Nа+ + S2– + 2Н2О
Н2S + 2ОН– = S2– + 2Н2О
Нерастворимое основание, например, гидроксид железа (III), реагирует с соляной кислотой потому, что продукт реакции - вода, связывает гидроксид-ионы более прочно, чем гидроксид железа (III).
Fe(OH)3 + 3HCl = FeCl3 + 3Н2О
Ионные уравнения:
Fe(OH)3 + 3H+ + 3Cl – = Fe3+ + 3Cl – + 3Н2О
Fe(OH)3 + 3H+ = Fe3+ + 3Н2О
В зависимости от условий проведения реакции нейтрализации можно получить среднюю, кислую или основную соль. Так, если кислота и основание берутся в эквивалентных отношениях, то образуется средняя соль.
Ca(OH)2 + H2SO4 = CaSO4 + 2Н2О [CaSO4 - сульфат кальция]
Если в реакции нейтрализации многоосновная кислота берется в избытке, то образуется кислая соль.
Ca(OH)2 + 2H2SO4 = Ca(HSO4)2 + 2Н2О [Ca(HSO4)2 - гидросульфат кальция]
избыток
Кислую соль можно перевести в среднюю. Для этого ее нужно донейтрализовать. При донейтрализации тем же основанием, которое образует данную соль, получаем одну среднюю соль (а), а при донейтрализации другим основанием - две средние соли (б):
а) Ca(HSO4)2 + Ca(OH)2 = 2 CaSO4 + 2Н2О
б) Ca(HSO4)2 + 2 NaOH = CaSO4 + Nа2SO4 + 2Н2О
Если в реакции нейтрализации многокислотное основание берется в избытке, то образуется основная соль.
2Ca(OH)2 + H2SO4 = (CaOH)2SO4 + 2Н2О
избыток гидроксосульфат
кальция
Основную соль можно перевести в среднюю. Для этого ее нужно донейтрализовать. При донейтрализации той же кислотой, которая образует данную соль, получаем одну среднюю соль (а), а при донейтрализации другой кислотой - две средние соли (б):
а) (CaOH)2SO4 + H2SO4 = 2 CaSO4 + 2Н2О
б) (CaOH)2SO4 + 2HCl = CaSO4 + CaCl2 + 2Н2О
Иначе ведут себя Ni(OH)3 и Co(OH)3 : при их взаимодействии с кислотами не образуются соли с Э3+, а происходит восстановление никеля и кобальта до Э2+, сопровождающееся выделением свободного кислорода или хлора (в отсутствие веществ способных окисляться):
4Ni(OH)3 + 4H2SO4 = NiSO4 + O2 + 10Н2О
2Ni(OH)3 + 6HCl = NiCl2 + Cl2 + 6Н2О
2. Растворимые основания взаимодействуют с солями, если образуются нерастворимые в воде новое основание (а) или новая соль (б).
а) Mg SO4 + 2NaОН = Mg(OH)2 ¯ + Na2SO4
б) K2SO4 + Ba(OH)2 = Ba SO4 ¯0 + 2KOH
3. Растворимые основания реагируют также с кислотными (а) и амфотерными (б) оксидами:
а) 2NaОН + CO2 = Nа2CO3 + н2О
б) 2NaОН + ZnO + н2О = Nа2[Zn(OH)4]
тетрагидроксоцинкат (II) натрия
4. Щелочи устойчивы к нагреванию, нерастворимые основания, как правило, при нагревании разлагаются:
Cu(OH)2 = CuO + н2О
5. Амфотерные гидроксиды в зависимости от условий реакции могут проявлять свойства как нерастворимых в воде оснований, так и нерастворимых воде кислот. Например, гидроксид алюминия реагирует с кислотами; при сплавлении с гидроксидом натрия он образует соли метаалюминиевой кислоты метаалюминаты....:
Al(OH)3 + 3HCl = AlCl3 + 3Н2О
Zn(OH)2 + SO3 = ZnSO4 + Н2О
Al(OH)3 + NaОН 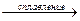 NaAlO2 + 2Н2О
NaAlO2 + 2Н2О
2NaОН(р) + Zn(OH)2 = Nа2[Zn(OH)4]
тетрагидроксоцинкат (II) натрия
Zn(OH)2 + K2О = K2ZnO2 + н2О
Диссоциацию амфотерного гидроксида, например, цинка можно выразить следующей схемой:
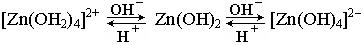
 2015-06-24
2015-06-24 1773
1773
