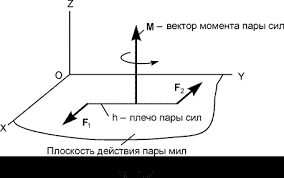
Амфотерность (двойственность свойств) гидроксидов и оксидов многих элементов проявляется в образовании ими двух типов солей. Например, для гидроксида и оксида алюминия:
а) 2Al(OH)3 + 3SO3 = Al2(SO4)3 + 3H2O
Al2О3 + 3H2SO4 = Al2(SO4)3 + 3H2O
б) 2Al(OH)3 + Na2O = 2NaAlO2 + 3H2O (в расплаве)
Al2О3 + 2NaOH(т) = 2NaAlO2 + H2O (в расплаве)
В реакциях (а) Al(OH)3 и Al2О3 проявляют свойства оснóвных гидроксидов и оксидов, то есть они подобно щелочам реагируют с кислотами и кислотными оксидами, образуя соль, в которой алюминий является катионом Al3+.
Напротив, в реакциях (б) Al(OH)3 и Al2О3 выполняют функцию кислотных гидроксидов и оксидов, образуя соль, в которой атом алюминия AlIII входит в состав аниона (кислотного остатка) AlО2−.
Сам элемент алюминий проявляет в этих соединениях свойства металла и неметалла. Следовательно, алюминий - амфотерный элемент.
Подобные свойства имеют также элементы А-групп - Be, Ga, Ge, Sn, Pb, Sb, Bi и другие, а также большинство элементов Б-групп - Cr, Mn, Fe, Zn, Cd и другие.
Например, амфотерность цинка доказывают такие реакции:
а) Zn(OH)2 + N2O5 = Zn(NO3)2 + H2O
ZnO + 2HNO3 = Zn(NO3)2 + H2O
б) Zn(OH)2 + Na2O = Na2ZnO2 + H2O
ZnO + 2NaOH(т) = Na2ZnO2 + H2O
Если амфотерный элемент имеет в соединениях несколько степеней окисления, то амфотерные свойства наиболее ярко проявляются для промежуточной степени окисления.
Например, у хрома известны три степени окисления: +II, +III и +VI. В случае CrIII кислотные и оснóвные свойства выражены примерно в равной степени, тогда как у CrII наблюдается преобладание оснóвных свойств, а у CrVI - кислотных свойств:
CrII → CrO, Cr(OH)2 → CrSO4
CrIII → Cr2O3, Cr(OH)3 → Cr2(SO4)3 или KCrO2
CrVI → CrO3, H2CrO4 → K2CrO4
Очень часто амфотерные гидроксиды элементов в степени окисления +III существуют также в мета-форме, например:
AlO(OH) - метагидроксид алюминия
FeO(OH) - метагидроксид железа (орто-форма "Fe(OH)3" не существует).
Амфотерные гидроксиды практически нерастворимы в воде, наиболее удобный способ их получения - осаждение из водного раствора с помощью слабого основания - гидрата аммиака:
Al(NO3)3 + 3(NH3 · H2O) = Al(OH)3↓ + 3NH4NO3 (20 °C)
Al(NO3)3 + 3(NH3 · H2O) = AlO(OH)↓ + 3NH4NO3 + H2O (80 °C)
В случае использования избытка щелочей в обменной реакции подобного типа гидроксид алюминия осаждаться не будет, поскольку алюминий в силу своей амфотерности переходит в анион:
Al(OH)3(т) + OH− = [Al(OH)4]−
Примеры молекулярных уравнений реакций этого типа:
Al(NO3)3 + 4NaOH(избыток) = Na[Al(OH)4] + 3NaNO3
ZnSO4 + 4NaOH(избыток) = Na2[Zn(OH)4] + Na2SO4
Образующиеся соли относятся к числу комплексных соединений (комплексных солей): они включают комплексные анионы [Al(OH)4]− и [Zn(OH)4]2−. Названия этих солей таковы:
Na[Al(OH)4] - тетрагидроксоалюминат натрия
Na2[Zn(OH)4] - тетрагидроксоцинкат натрия
Продукты взаимодействия оксидов алюминия или цинка с твердой щелочью называются по-другому:
NaAlO2 - диоксоалюминат(III) натрия
Na2ZnO2 - диоксоцинкат(II) натрия
Подкисление растворов комплексных солей этого типа приводит к разрушению комплексных анионов:
H+ H+
[Al(OH)4]− → Al(OH)3 → Al3+
Например: 2Na[Al(OH)4] + CO2 = 2Al(OH)3↓ + NaHCO3
Для многих амфотерных элементов точные формулы гидроксидов низвестны, поскольку из водного раствора вместо гидроксидов выпадают гидратированные оксиды, например MnO2 · nH2O, Sb2O5 · nH2O.
Амфотерные элементы в свободном виде взаимодействуют как с типичными кислотами, так и со щелочами:
2Al + 3H2SO4(разб.) = Al2(SO4)3 + H2↑
2Al + 6H2O + 4NaOH(конц.) = 2Na[Al(OH)4] + 3H2↑
В обеих реакциях образуются соли, причем рассматриваемый элемент в одном случае входит в состав катиона, а во втором - в состав аниона.
Галогениды алюминия в обычных условиях - бесцветные кристаллические
вещества. В ряду галогенидов алюминия AlF3 сильно отличается по свойствам
от своих аналогов. Он тугоплавок, мало растворяется в воде, химически
неактивен. Основной способ получения AlF3 основан на действии безводного HF
на Al2O3 или Al:
Al2O3 + 6HF = 2AlF3 + 3H2O
Соединения алюминия с хлором, бромом и иодом легкоплавки, весьма
реакционноспособны и хорошо растворимы не только в воде, но и во многих
органических растворителях. Взаимодействие галогенидов алюминия с водой
сопровождается значительным выделением теплоты. В водном растворе все они
сильно гидролизованы, но в отличие от типичных кислотных галогенидов
неметаллов их гидролиз неполный и обратимый. Будучи заметно летучими уже
при обычных условиях, AlCl3, AlBr3 и AlI3 дымят во влажном воздухе
(вследствие гидролиза). Они могут быть получены прямым взаимодействием
простых веществ.
Комплексные галогениды (галогенометаллаты) содержат комплексные анионы, в к-рых атомы галогенов являются лигандами, напр. гексахлороплатинат(IV) калияK2[PtCl6], гептафторотанталат(V) натрия Na[TaF7], гексафтороарсенат(V) лития Li[AsF6]. наиб. термич. устойчивостью обладают фторо-, оксофторо- и хлорометаллаты. По характеру связей к комплексным галогенидам близки ионные соед. с катионами NF4+, N2F3+, C1F2+, XeF+ и др.
Для многих галогенидов характерны ассоциация и полимеризация в жидкой и газовой фазах с образованием мостиковых связей. наиб. склонны к этому галогенидыметаллов I и II групп, А1С13, пентафториды Sb и переходных металлов, оксофториды состава MOF4. Известны галогениды со связью металл - металл, напр. Hg2Cl2.
Фториды значительно отличаются по св-вам от др. галогенидов. Однако в простых галогенидах эти отличия выражены менее резко, чем в самих галогенах, а в комплексных галогенидах-слабее, чем в простых.
Многие ковалентные галогениды (особенно фториды)-сильные к-ты Льюиса, напр. AsF5, SbF5, BF3, A1C13. Фториды входят в состав сверхкислот. Высшие галогениды восстанавливаются металлами и Н2, напр.:
Галогениды металлов V-VIII групп, кроме Сr и Мn, восстанавливаются Н2 до металлов, напр.: WF6 + 3Н2 -> W + 6HF
Многие ковалентные и ионные галогениды металлов взаимодействуют между собой с образованием комплексных галогенидов, напр.: КС1 + ТаС15 -> К[ТаС16]
Более легкие галогены могут вытеснять более тяжелые из галогенидов. Кислород может окислять галогениды с выделением С12, Вr2 и I2. Одна из характерных р-ций ковалентных галогенидов-взаимод. с водой (гидролиз) или ее парами при нагр. (пирогидролиз), приводящее к образованию оксидов, окси- или
оксогалогенидов, гидроксидов и галогеноводородов. Исключение составляют CF4, CC14 и SF6, устойчивые к парам воды при высоких т-рах.
Галогениды получают непосредственно из элементов, взаимод. галогеноводородов или галогеноводородных к-т с элементами, оксидами, гидроксидами или солями, а также обменными р-циями.
Галогениды широко используют в технике как исходные в-ва для получения галогенов, щелочных и щел.-зем. металлов, как компоненты стекол и др. неорг. материалов; они являются промежут. продуктами в произ-ве редких и нек-рых цветных металлов, U, Si, Ge и др.
В природе галогениды образуют отдельные классы минералов, в к-рых представлены фториды (напр., минералы флюорит, криолит) и хлориды (сильвин, карналлит).Бром и иод входят в состав нек-рых минералов в виде изоморфных примесей. Значительные кол-ва галогенидов содержатся в воде морей и океанов, в соляных и подземных рассолах. Некоторые галогениды, напр. NaCl, К.С1, СаС12, входят в состав живых организмов.
Криоли́т (от др.-греч. κρύος — мороз + λίθος — камень) — редкий минерал из класса природных фторидов, гексафтороалюминат натрия Na3[AlF6]. Кристаллизуется в моноклинной сингонии; кубовидные кристаллы и двойниковые пластины встречаются редко. Обычно образует бесцветные, белые или серые кристаллические скопления со стеклянным блеском, часто заключают в себе кварц, сидерит, пирит, галенит, халькопирит, колумбит, касситерит. Возможна окраска примесями органических веществ.
В настоящее время разработаны методы получения искусственного криолита. Искусственно получается путём взаимодействия фторида алюминия с фторидом натрия, а также действием плавиковой кислоты на гидроксид алюминия в присутствии соды. Используется в процессе электролитического получения алюминия, в производстве плавиковой кислоты, стекла и эмалей.
Квасцы. Квасцы - групповое название двойных солей состава МЭ(SO4)2. 12H2O, где М - калий K, рубидий Rb, цезий Cs, аммоний NH4, а Э - алюминий Al, хром Cr, железо Fe и другие элементы в степени окисления (+III), дающие при диссоциации солей трехзарядные катионы.
Квасцы хорошо растворяются в воде, их водные растворы имеют вяжущий кисловатый вкус и кислую реакцию из-за гидролиза, например:
[Al(H2O)6]3+ + H2O <<здесь знак обратимости >> [Al(H2O)5(OH)]2+ + H3O+
При нагревании квасцы сначала плавятся в содержащейся в них воде, а затем эту воду теряют, образуя безводные соли. Дальнейшее нагревание превращает квасцы в смесь оксидов металлов. Алюмо-калиевые квасцы могут быть получены при видоизменении процесса производства очищенного сульфата алюминия. Вначале производят варку каолина с серной кислотой. По окончании нейтрализации серной кислоты в реактор добавляют сульфат натрия из расчета получения натриевых квасцов. Последние, вследствие своей большой растворимости, находятся в растворе. После разбавления раствора до плотности 1,33 г/см3 его отделяют от осадка кремнезема, охлаждают и смешивают с насыщенным раствором хлорида калия. При этом в осадок выделяются алюмо-калиевые квасцы, плохо растворимые при невысокой температуре. В маточном растворе после отделения кристаллов алюмо-калиевых квасцов остаются растворимые примеси — соединения железа и хлорид натрия 89.
В процессе гидролиза гидратированные ионы алюминия теряют протоны, образуя последовательные гидро-оксо-комплексы. Когда последний нейтральный комплекс теряет воду, образуется нерастворимая гидроокись А1(ОН)3.
Комплексные ионы [А1(Н20)5ОН]2+ и [А1(Н20)4(ОН)2]+ остаются в растворе, тогда как гидроокись А1(ОН)3 осаждается сразу после своего образования. Осаждение происходит при значениях рН > 3. Полностью до образования гидроокиси алюминия гидролиз протекает при условии нейтрализации образующихся протонов, например щелочью.
Глубокий гидролиз соли сернокислого алюминия широко применяют для очистки питьевых и сточных вод. Выделяющийся при гидролизе гидроксоний вступает в реакцию с обычно содержащимися в воде бикарбонатами Н30+ + НС03 = С02 + 2Н20. В этом случае конечными продуктами гидролиза являются коллоидная гидроокись алюминия и углекислота.
При коагуляции золя гидроокиси алюминия получается объемистый студенистый осадок, который захватывает взвешенные частицы и бактерии и увлекает их на дно отстойника. Расход сернокислого алюминия, необходимый для очистки воды, зависит от состава и количества находящихся в воде загрязнений. Дозы сернокислого алюминия для очистки природных вод и для до-очистки сточных вод колеблются в пределах 3 — 15 мг/л по А1203, а для физико-химической очистки городских сточных вод достигают 30—50 мг/л по А1203. Расход сернокислого алюминия должен обеспечить образование достаточно большой массы хлопьев, что необходимо для изъятия из воды находящихся в ней загрязнений. Значение рН раствора должно быть снижено до 6,5—7,6, что соответствует минимальной растворимости в воде гидроокиси алюминия. При большем или меньшем значении рН часть алюминия остается в воде в растворенном состоянии. В водах с малой щелочностью, когда содержание бикарбонатов недостаточно для нейтрализации выделяющейся кислоты, процесс гидролиза из-за сильного понижения рН не доходит до конца. Для повышения щелочности, завершения процесса гидролиза и уменьшения содержание в воде растворенного алюминия в воду одновременно с коагулян1 том вводят известь и соду.
Если не проводить нейтрализацию накапливающихся при гидролизе протонов, то процесс гидролиза замедляется, что приводит к наступлению гидролитического равновесия, которое может быть охарактеризовано степенью и константой гидролиза. Гидролиз растворов сернокислого алюминия, который является реакцией замещения сульфатных ионов в А12(804)3 ионами ОН", образующимися за счет диссоциации воды, может быть представлен в общем виде уравнением
2А13+ + (3 - -|-) ЭОГ + аОН" + ад^АЦОНЦБОЖ --^ЭОГ + ад,
где а — степень и основность замещения.
Это уравнение показывает, что решающее влияние на смещение вправо оказывает концентрация ионов ОН- в растворе, т. е. степень диссоциации воды. Как известно, для солей со слабым основанием и сильной кислотой степень гидролиза к связана с константой гидролиза А-,,, концентрацией соли (с, моль'л), ионным произведением воды кю и константой диссоциации основания кь следующим соотношением:
/г = УкЦс = УкиЛъс.
Если А-,, мало изменяется с температурой, то кш увеличивается значительно, что и вызывает существенный рост степени гидролиза с повышением температуры.
Н. И. Еремин на основании полученных экспериментальных данных вывел уравнения зависимости степени гидролиза раствора от температуры и концентрации
для сернокислого алюминия:
1ё к = - 2,23 + 0,05с + 0,0036т7 + 18 УЦс, для аммониевых квасцов:
18 Л = —1,19 +0,29с+ 0,0016Г + 18угЩ для калиевых квасцов:
\ёк= - 1,17 + 0,29с + 0,00167 + 18 УПс,
для натриевых квасцов:
18к = — 1,18 + 0,29с + 0,0016т7 + \ё УПс.
Как видно из этих уравнений, влияние концентрации на степень гидролиза для квасцов более значительно, чем сернокислого алюминия.
Бор. Получение бора. Химические свойства. Диагональное сходство бора с кремнием. Гидриды бора. Диборан. Особенности химической связи в молекуле диборана. Галогениды бора. Кислородные соединения бора. Оксид бора и борные кислоты. Бура. Получение борной кислоты. Боросиликатные стёкла. Борноэтиловый эфир.
Бор — элемент тринадцатой группы (по устаревшей классификации — главной подгруппы третьей группы), второго периода периодической системы химических элементов с атомным номером 5. Обозначается символом B (лат. Borum). В свободном состоянии бор — бесцветное, серое или красное кристаллическое либо тёмное аморфное вещество. Известно более 10 аллотропных модификаций бора, образование и взаимные переходы которых определяются температурой, при которой бор был получен
Получение. Наиболее чистый бор получают пиролизом бороводородов. Такой бор используется для производства полупроводниковых материалов и тонких химических синтезов.
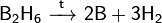
Метод металлотермии (чаще восстановление магнием или натрием):

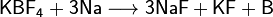
Термическое разложение паров бромида бора на раскаленной (1000—1200 °C) вольфрамовой проволоке в присутствии водорода (метод Ван-Аркеля):
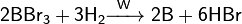
Физические свойства. Чрезвычайно твёрдое вещество (уступает только алмазу, нитриду бора (боразону), карбиду бора, сплаву бор-углерод-кремний, карбиду скандия-титана). Обладает хрупкостью и полупроводниковыми свойствами (широкозонный
полупроводник). У бора самый высокий предел прочности на разрыв 5,7 ГПа
В природе бор находится в виде двух изотопов 10В (20 %) и 11В (80 %)[.
10В имеет очень высокое сечение поглощения тепловых нейтронов, поэтому 10В в составе борной кислоты применяется в атомных реакторах для регулирования реактивности.
Химические свойства. Ионы бора окрашивают пламя в зелёный цвет.
По многим физическим и химическим свойствам неметалл бор напоминает кремний.
Химически бор довольно инертен и при комнатной температуре взаимодействует только со фтором:
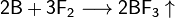
При нагревании бор реагирует с другими галогенами с образованием тригалогенидов, с азотом образует нитрид бора BN, с фосфором — фосфид BP, с углеродом — карбиды различного состава (B4C, B12C3, B13C2). При нагревании в атмосфере кислорода или на воздухе бор сгорает с большим выделением теплоты, образуется оксид B2O3:
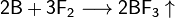
С водородом бор напрямую не взаимодействует, хотя известно довольно большое число бороводородов (боранов) различного состава, получаемых при обработке боридов щелочных или щелочноземельных металлов кислотой:
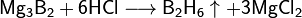
При сильном нагревании бор проявляет восстановительные свойства. Он способен, например, восстановить кремний или фосфор из их оксидов:
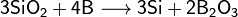
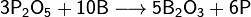
Данное свойство бора можно объяснить очень высокой прочностью химических связей в оксиде бора B2O3.
При отсутствии окислителей бор устойчив к действию растворов щелочей. В горячей азотной, серной кислотах и в царской водке бор растворяется с образованием борной кислоты 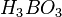
Оксид бора — типичный кислотный оксид. Он реагирует с водой с образованием борной кислоты: 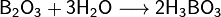
При взаимодействии борной кислоты со щелочами возникают соли не самой борной кислоты — бораты (содержащие анион BO33−), а тетрабораты, например:
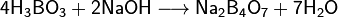
Бор - полупроводник, диагональное сходство с кремнием:
1) Оба тугоплавкие, твердые, полупроводники. В – серо-черный, Si- серый.
I1(B)=8.298 эВ; I1(Si)=8.151 эВ. Оба не склонны к образованию катионов.
2) Оба химически инертны (хотя бор все-таки растворяется в горячих кислотах-окислителях. Оба растворяются в щелочах.
2B + KOH + 2H2O ® 2KBO2 + 3H2
Si + 2KOH + H2O®K2SiO3+ 2H2
3) При высоких температурах реагируют с металлами, образуя бориды и силициды - Ca3B2;Mg2Si- тугоплавкие, электропроводные соединения.
Кислородные соединения бора. В2О3- кислотный оксид (SiO2 тоже) - оба полимерные, стеклообразные, только В2О3образует плоские сетки, аSiO2- трехмерные структуры. Отличие между ними в том, что оксид бора легко гидратируется, а песок (SiO2), как известно, нет.
H3BO3- ортоборная кислота.
H3BO3«HBO2+H2Oметаборная кислота (100оС)
4HBO2«H2B4O7+H2Oтетраборная кислота (140оС) - слабая, обе Кд
H2B4O7«2B2O3+H2Oпрактически одинаковы - нет кислых солей
Ортоборная кислота слабая, иногда ее диссоциацию пишут
B(OH)3 + H2O «B(OH)4 + H+
Образует сложные эфиры со спиртами: H3BO3+3CH3OH®B(OCH3)3+3H2O
Свойства. Бор известен в аморфной (коричневой) и кристаллической (черной) формах, т.пл. 2300°С, т.кип. 3700°С, р = 2,34 г/см3. Кристаллическая решетка бора очень прочна, это проявляется в его высокой твердости, низкой энтропии,[7 Дж/(моль-К)] и высокой температуре плавления. Бор—полупроводник. Неметалличность бора отвечает его положению в периодической системе - между бериллием и углеродом и по диагонали— рядом с кремнием. Поэтому у бора проявляется сходство не только с алюминием, но и с кремнием. Из его положения следует также, что соединения бора с азотом должны быть по электронному строению и свойствам похожи на углерод.
2ВН3(г) — В2Н6(г);
дельта G= - 126 кДж
3NaBH4+4BF3 —>2В2Н6 + 3NaBF4
6H2 (г) + 2ВС13 (г) —>В2Н6(г) + 6НСl(г)
Диборан В2Н6 — энергичный восстановитель, на воздухе он самовоспламеняется
В2Н6+3О2 =>В2О3+ЗН2О
С водой взаимодействует с выделением водорода;
В2Н6+6Н2О =>. 2Н3ВО3+6Н2
В среда эфира В2Н6 реагирует с гидридом лития, образуя борогидрид
B2H6+2LiH => 2LiBH4
Чаще, чем Li[BH4], используютNa[BH4], получаемый по реакции-
4NaH + B(OCH3)3 => Na[BН4] + 3NаОСН3
В2О3 + ЗС => 2В + ЗСО
2B2O3+P4O10 => 4BPO4
Н3ВО3+Н2O => [В(ОН)4] + H
При нейтрализации Н3ВО3 не образуются ортобораты, содержащие ион (ВО3)3-, а получаются тетрабораты, метабораты или соли других полиборных кислот:
4Н3ВО3+2NаОН => Na2BO4 + 7Н2О Н3ВО3 +NaOH=>NaBO2 + 2Н2О
Окси́д бо́ра B2O3 — ангидрид борной кислоты, бесцветное, довольно тугоплавкое стекловидное или кристаллическое вещество горьковатого вкуса, диэлектрик.
Стеклообразный оксид бора имеет слоистую структуру (расстояние между слоями 0.185 нм), в слоях атомы бора расположены внутри равносторонних треугольников ВО3 (d В—О=0.145 нм). Эта модификация плавится в интервале температур 325—450 °C и обладает высокой твёрдостью. Она получается при нагревании бора на воздухе 700 °C или обезвоживанием ортоборной кислоты. Кристаллический В2О3, который получают осторожным отщеплением воды от метаборной кислоты НВО2, существует в двух модификациях — с гексагональной кристаллической решёткой, при 400 °C и 2200 МПа переходящей в моноклинную.
В промышленности из природных боратовсплавлением с содой получают буру. При обработке природных минералов бора серной кислотой образуется борная кислота. Из борной кислоты H3BO3 прокаливанием получают оксид B2O3, а затем его или буру восстанавливают активными металлами (магнием или натрием) до свободного бора:
B2O3 + 3Mg = 3MgO + 2B,
2Na2B4O7 + 3Na = B + 7NaBO2.
При этом в виде серого порошка образуется аморфный бор. Кристаллический бор высокой чистоты можно получить перекристаллизацией, но в промышленности его чаще получают электролизом расплавленных фтороборатов или термическим разложением паров бромида бора BBr3 на раскаленной до 1000-1500 °C танталовой проволоке в присутствии водорода:
2BBr3 + 3H2 = 2B + 6HBr
Возможно также использование крекинга бороводородов:
В4H10 = 4B + 5H2.
Бо́рная кислота́ (ортоборная кислота) — слабая кислота, имеющая химическую формулу H3BO3. Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решетку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями (d= 0,318 нм).
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трех модификациях — наиболее устойчивой γ-НВО2 с кубической решеткой, β-НВО2 с моноклинной решеткой и α-НВО2 с ромбической решеткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Борная кислота проявляет очень слабые кислотные свойства. Она сравнительно мало растворима в воде. Ее кислотные свойства обусловлены не отщеплением протона Н+, а присоединением гидроксильного аниона:
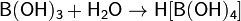
Ka = 5.8·10−10 моль/л; pKa = 9.24.
Она легко вытесняется из растворов своих солей большинством других кислот. Соли ее, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная. Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3−, поскольку ортобораты гидролизуются практически полностью, вследствие слишком малой константы образования [В(ОН)4]−. В растворе образуются тетрабораты, метабораты или соли других полиборных кислот:
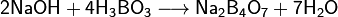
Избытком щелочи они могут быть переведены в метабораты:
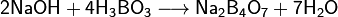
Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведенным).
В подкисленных водных растворах боратов устанавливаются следующие равновесия:
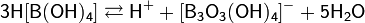
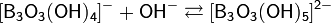
Наиболее распространенной солью борной кислоты является декагидрат тетрабората натрия Na2B4O7·10H2O (техническое название — бура).
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
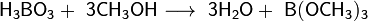
Образование борнометилового эфира В(ОСН3)3 является качественной реакцией на Н3ВО3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Боросиликатное стекло — стекло обычного состава, в котором заменяют щелочные компоненты в исходном сырье на окись бора (B2O3). Этим достигается повышенная химическая стойкость и малый коэффициент температурного расширения — до 3,3·10−6 при 20 °C у лучших образцов. У боросиликатного стекла он очень мал, меньше только у кварцевого стекла (почти в 10 раз). Это позволяет стеклу не трескаться при резких изменениях температуры. Этим обусловлено его применение в качестве противопожарного и в других случаях, когда необходима термическая стойкость.
Использование В быту, для изготовления посуды для открытого огня, заварочных чайников. Применяется как материал для лабораторной посуды, а также для химической промышленности и других отраслей, например, в качестве материала теплообменника для тепловых электростанций. Также применяется для изготовления дешевых гитарных слайдов. Также боросиликатное стекло может применяться для изготовления пипеток для ИКСИ, биопсии бластомера, которая проводится для проведения предимплантационной генетической диагностики с использованием в качестве генетического материала биопсийных клеток. Существует 3 варианта пипеток с внутренним диаметром от 4 µм до 7,5 µм. Длина пипетки составляет от 60 до 75 мм и имеет угол скоса 30°. Пипетки предназначены для одноразового использования.
Общая характеристика элементов IVA подгруппы. Строение атомов. Степени окисления. Распространённость и формы нахождения в природе. Аллотропные модификации углерода. Физические и химические свойства. Разновидности чёрного графита: кокс, древесный уголь, сажа.
Общая характеристика элементов IVA группы К элементам главной подгруппы IV группы относятся C, Si, Ge, Sn, Pв. Электронная формула внешнего валентного уровня nS2np2, то есть имеют 4 валентных электрона и это р - элементы, поэтому находятся в главной подгруппе IV группы. │↑│↑││ │↑↓│ np nS В основном состоянии атома два электрона спарены, а два – неспарены. Предвнешняя электронная оболочка углерода имеет 2 электрона, кремния – 8, а Ge, Sn, Pв – по 18 электронов. Поэтому Ge, Sn, Pв объединены в подгруппу германия (это – полные электронные аналоги). В этой подгруппе р – элементов, как и в остальных подгруппах р–элементов, свойства атомов элементов изменяются периодически.
Таким образом, сверху вниз в подгруппе радиус атома увеличивается, поэтому энергия ионизации уменьшается, поэтому способность отдавать электроны увеличивается, а тенденция к дополнению внешней электронной оболочки до октета резко уменьшается, поэтому от С к Рв увеличиваются восстановительные свойства и металлические свойства, а неметаллические свойства уменьшаются. Углерод и кремний – типичные неметаллы, у Ge уже появляются металлические свойства и по внешнему виду он похож на металл, хотя и является полупроводником. У олова уже металлические свойства преобладают, а свинец – типичный металл. Имея 4 валентных электрона, атомы в своих соединениях могут проявлять степени окисления от минимальной (-4) до максимальной (+4), причём для них характерны чётные С.О.: -4, 0, +2, +4; С.О. = -4 характерна для С и Si с металлами. Характер связи с другими элементами. Углерод образует только ковалентные связи, кремний тоже преимущественно образует ковалентные связи. Для олова и свинца, особенно в С.О. = +2, более характерен ионный характер связи (например, Рв(NO3)2). Ковалентность определяется валентной структурой атома. У атома углерода 4 валентные орбитали и максимальная ковалентность равна 4. У остальных элементов ковалентность может быть больше четырех, так как есть валентный d-подуровень (например, H2[SiF6]). Гибридизация. Тип гибридизации определяется типом и числом валентных орбиталей. У углерода есть лишь S- и р-валентные орбитали, поэтому может быть Sp (карбин, СО2, CS2), Sp2 (графит, бензол, COCl2), Sp3-гибридизация (CH4, алмаз, CCl4). Для кремния самая характерная Sp3 – гибридизация (SiO2, SiCl4), но у него есть валентный d-подуровень, поэтому есть также Sp3d2-гибридизация, например, H2[SiF6]. IV группа ПСЭ – это середина таблицы Д.И.Менделеева. Здесь ярко прослеживается резкое изменение свойств от неметаллов к металлам. Отдельно рассмотрим углерод, затем – кремний, затем элементы подгруппы германия.
Атом (от греческого atomos - неделимый) — одноядерная, неделимая частица химического элемента, носитель свойства вещества. Вещества состоят из атомов. Сам атом состоит из положительно заряженного ядра и отрицательно заряженного электронного облака. В целом атом электронейтрален. Размер атома полностью определяется размером его электронного облака, поскольку размер ядра ничтожно мал по сравнению с размером электронного облака. Ядро состоит из Z положительно заряженных протонов (заряд протона соответствует +1 в условных единицах) и N нейтронов, которые не несут на себе заряда (протоны и нейтроны называют нуклонами). Таким образом, заряд ядра определятся только количеством протонов и равен порядковому номеру элемента в таблице Менделеева. Положительный заряд ядра компенсируется отрицательно заряженными электронами (заряд электрона -1 в условных единицах), которые формируют электронное облако. Количество электронов равно количеству протонов. Массы протонов и нейтронов равны (соответственно 1 и 1 а.е.м.). Масса атома определятся массой его ядра, поскольку масса электрона примерно в 1850 раз меньше массы протона и нейтрона и в расчетах редко учитывается. Количество нейтронов можно узнать по разности между массой атома и количеством протонов (N=A-Z). Вид атомов какого-либо химического элемента с ядром, состоящим из строго определённого числа протонов (Z) и нейтронов (N) называется нуклидом.
Поскольку в ядре атома сосредоточена практически вся масса, но его размеры ничтожно малы по сравнению с общим объемом атома, то ядро условно принимается материальной точкой покоящейся в центре атома, а сам атом рассматривается как система электронов. При химической реакции ядро атома не затрагивается (кроме ядерных реакций), как и внутренние электронные уровни, а участвуют только электроны внешней электронной оболочки. По этой причине необходимо знать свойства электрона и правила формирования электронных оболочек атомов.
Сте́пень окисле́ния (окислительное число, формальный заряд) — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле (см. #Условность).
Представления о степени окисления элементов положены в основу и используются при классификации химических веществ, описании их свойств, составлении формул соединений и их международных названий (номенклатуры). Но особенно широко оно применяется при изучении окислительно-восстановительных реакций.
Понятие степень окисления часто используют в неорганической химии вместо понятия валентность.
Степень окисления атома равна численной величине электрического заряда, приписываемого атому в предположении, что электронные пары, осуществляющие связь, полностью смещены в сторону более электроотрицательных атомов (то есть исходя из предположения, что соединение состоит только из ионов).
Степень окисления соответствует числу электронов, которое следует присоединить к положительному иону, чтобы восстановить его до нейтрального атома, или отнять от отрицательного иона, чтобы окислить его до нейтрального атома:
Al3+ + 3e− → Al
S2− → S + 2e− (S2− − 2e− → S)
Углерод — вещество с самым[источник не указан 1528 дней] большим числом аллотропических модификаций (более 8 уже обнаружены).
Аллотропные модификации углерода по своим свойствам наиболее радикально отличаются друг от друга, от мягкого к твёрдому, непрозрачного к прозрачному, абразивного к смазочному, недорогого к дорогому. Эти аллотропы включают аморфные аллотропы углерода (уголь, сажа), нанопена, кристаллические аллотропы — нанотрубка, алмаз, фуллерены, графит, лонсдейлит и церафит.
Классификация аллотропов углерода по характеру химической связи между атомами:
sp3 формы:
Алмаз (куб)
Лонсдейлит (гексагональный алмаз)
sp2 формы
Графит
Графены
Фуллерены (C20+)
Нанотрубки
Нановолокна
Астралены
Стеклоуглерод
Колоссальные нанотрубки
sp формы:
Карбин
Смешанные sp3/sp2 формы:
Аморфный углерод
Углеродные нанопочки
Углеродная нанопена
Другие формы: C1 — C2 — C3 — C8
Углеро́д (химический символ — C, лат. Carboneum) — химический элемент четырнадцатой группы (по устаревшей классификации — главной подгруппы четвёртой
группы), 2-го периода периодической системы химических элементов. порядковый номер 6, атомная масса — 12,0107.
Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими свойствами. Разнообразие модификаций обусловлено способностью углерода образовывать химические связи разного типа.
 2015-01-30
2015-01-30 7605
7605