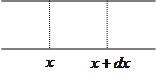Диффузия (от латинского diffusio – распространение, растекание) – взаимное проникновение соприкасающихся веществ друг в друга вследствие теплового движения частиц вещества. Диффузия происходит в направлении уменьшения концентрации вещества и ведет к его равномерному распределению по занимаемому объему (выравниванию химического потенциала). Наиболее быстро диффузия происходит в газах, медленнее – в жидкостях, ещё медленнее – в твердых телах. Это обусловлено характером теплового движения частиц в этих средах.
Траектория движения каждой частицы газа представляет собой ломаную линию, т.к. при столкновениях она меняет направление и скорость движения. Поэтому диффузионное проникновение значительно медленнее свободного движения.
5.1. Самодиффузия.
Если два газа, помещенные в сосуд, разделить перегородкой, а затем перегородку убрать, то газы начнут перемешиваться. Такое взаимопроникновение одного газа в среду другого называется взаимной или концентрационной диффузией газов.
 Однако, если по обе стороны сосуда находится одинаковый газ,
Однако, если по обе стороны сосуда находится одинаковый газ,
то после удаления перегородки диффузия все равно будет
происходить. Такой процесс называется самодиффузией.
На опыте, вообще говоря, самодиффузию наблюдать нельзя, т.к. из-за
тождественности молекул она не может проявиться ни в каком
макроскопическом явлении.
Для наблюдении самодиффузии надо «пометить» часть молекул газа. На практике с этой целью используют смесь изотопов, один из которых, например, радиоактивный. Мысленно разделим молекулы, условно назвав их молекулами ²1-го сорта² и ²2-го сорта², тогда при удалении перегородки начнется выравнивание их концентраций. Таким образом, переносимым качеством является в этом случае концентрация рассматриваемого сорта молекул.
Обозначим концентрацию молекул 1-го сорта 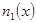 и рассмотрим их поток из занимаемой части сосуда. Т.к.
и рассмотрим их поток из занимаемой части сосуда. Т.к. 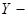 это переносимое качество, отнесенное к одной молекуле, тогда для газа, состоящего из молекул 1-го сорта, имеем:
это переносимое качество, отнесенное к одной молекуле, тогда для газа, состоящего из молекул 1-го сорта, имеем: 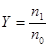 , где
, где 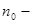 их равновесная концентрация. Из общего уравнения переноса получаем
их равновесная концентрация. Из общего уравнения переноса получаем
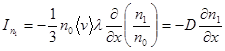 . (5.1)
. (5.1)
Мы получили уравнение Фика:
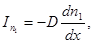 (5.2)
(5.2)
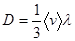 . (5.3)
. (5.3)
1). При постоянной температуре 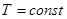 ,
, 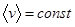 ,
, 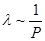 и тогда
и тогда 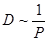 .
.
2). При постоянном давлении 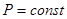 имеем
имеем 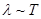 ,
, 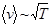 и
и 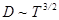 .
.
3). При постоянном объеме 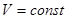 имеем
имеем 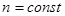 и тогда
и тогда 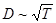 .
.
Заметим, что последние две зависимости справедливы при пренебрежении зависимости эффективного сечения от температуры.
4). Размерность коэффициента диффузии 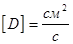 .
.
5.2. Взаимная диффузия.
В газах, состоящих из различных молекул может наблюдаться в заимная диффузия. Если взять два различных газа, молекулы которых отличаются динамическими свойствами и характером взаимодействия, то процесс диффузии значительно усложняется.
Пусть в составе газа имеются легкие и тяжелые молекулы, и их концентрации равны, соответственно, 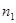 и
и 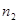 . Условие постоянства давления и температуры по всему объему имеет вид:
. Условие постоянства давления и температуры по всему объему имеет вид:
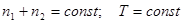 . (5.3)
. (5.3)
Общее уравнение переноса применимо для каждой из компонент газа, однако длина свободного пробега 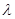 должна быть вычислена с учетом столкновений с молекулами как одного сорта, так и другого:
должна быть вычислена с учетом столкновений с молекулами как одного сорта, так и другого:
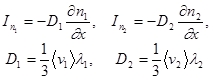 (5.4)
(5.4)
Если коэффициенты диффузии не равны друг другу 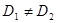 , диффузионные потоки не компенсируют друг друга
, диффузионные потоки не компенсируют друг друга 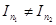 , вследствие чего нарушается постоянство давления по объему газа. Из-за этого, в свою очередь, наряду с диффузионными потоками возникает гидродинамический поток, т.е. движение газа как целого для выравнивания давления.
, вследствие чего нарушается постоянство давления по объему газа. Из-за этого, в свою очередь, наряду с диффузионными потоками возникает гидродинамический поток, т.е. движение газа как целого для выравнивания давления.
Пусть 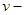 скорость гидродинамического потока газа как целого. Тогда, исходя из условия постоянства давления по занимаемому газом объему, должно быть
скорость гидродинамического потока газа как целого. Тогда, исходя из условия постоянства давления по занимаемому газом объему, должно быть
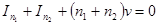 .
.
Отсюда получаем
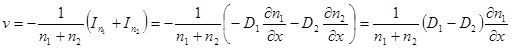 .
.
Здесь учтено, что из условия 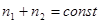 следует
следует 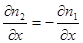 .
.
Поэтому полный поток первой компоненты равен сумме диффузионного и гидродинамического потоков:
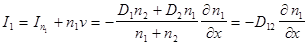
где коэффициент взаимной диффузии 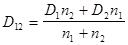 .
.
Полный поток второй компоненты:
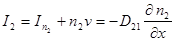
где 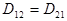 - коэффициенты взаимной диффузии.
- коэффициенты взаимной диффузии.
............
5.3. Уравнение диффузии, зависящее от времени.
Если система предоставлена самой себе, то температура и концентрация со временем становятся постоянными. Время, в течение которого происходит достижение равновесия называется временем релаксации. Рассмотрим снова самодиффузию. Получим уравнение как в случае с теплопроводностью.
|
Изменение количества частиц в объеме 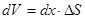 равно
равно
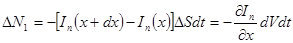
минус в формуле означает, что число частиц уменьшается.
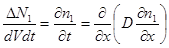
Итак, уравнение диффузии, зависящее от времени:
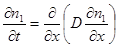
Если коэффициент диффузии не зависит от координат (что верно для самодиффузии):
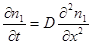
Если рассматривается взаимная диффузия, то пишем 2-го уравнения с коэффициентами 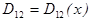
5.4. Термическая диффузия.
Если в объеме находится смесь газов и в нем создать градиент температуры, то равномерное распределение газа по объему нарушается: обычно в более теплых областях объема увеличивается концентрация легкой компоненты смеси, а в более холодных - тяжелой. Это явление носит название термической диффузии.
Если разность температур поддерживается постоянной, то вследствие термодиффузии в объеме смеси возникает градиент концентрации. Это вызывает и обычную диффузию. Эти процессы идут в разные стороны, поэтому термодиффузия может уравновешиваться обычной диффузией, что приводит к стационарному протеканию процессов.
Коэффициент термодиффузии сильно зависит от межмолекулярного взаимодействия. Поэтому изучение термодиффузии позволяет исследовать межмолекулярные силы в газах.
5.5. Диффузия в жидкостях.
В жидкостях, в соответствии с характером теплового движения молекул, диффузия осуществляется в результате перескоков молекул из одного устойчивого положения в другое. Каждый скачок происходит при сообщении молекуле энергии, достаточной для разрыва её связей с соседними молекулами и перехода в окружение других молекул (новое положение должно быть энергетически выгодно, т.е. определяться локальным минимумом энергии). Среднее перемещение при таком скачке не превышает межмолекулярного расстояния.
Диффузионное движение частиц в жидкости можно рассматривать как движение с трением. К нему применимо соотношение, полученное для коэффициента диффузии Эйнштейном:
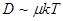 ,
,
где 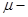 подвижность диффундирующих частиц, т.е. коэффициент пропорциональности между скоростью частицы
подвижность диффундирующих частиц, т.е. коэффициент пропорциональности между скоростью частицы 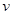 и движущей её силой
и движущей её силой 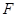 при стационарном движении с трением (
при стационарном движении с трением (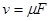 ).
).
Если частицы сферически симметричны, то
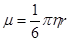 ,
,
где 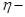 коэффициент вязкости жидкости,
коэффициент вязкости жидкости, 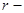 радиус частицы.
радиус частицы.
В жидкости коэффициент диффузии 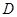 растет с температурой, что обусловлено «разрыхлением» её структуры (ослаблением межмолекулярных связей) при нагреве и соответствующим увеличением числа перескоков в единицу времени.
растет с температурой, что обусловлено «разрыхлением» её структуры (ослаблением межмолекулярных связей) при нагреве и соответствующим увеличением числа перескоков в единицу времени.
5.6. Диффузия в твердых телах.
В твердом теле могут действовать несколько механизмов диффузии: обмен местами атомов с вакансиями (незанятыми узлами кристаллической решетки), преобладающий при образовании твердых растворов замещения; перемещение атомов по междоузлиям, наблюдающееся при образовании твердых растворов внедрения; одновременное циклическое перемещение нескольких атомов; прямой обмен местами двух соседних атомов и т.д.
Коэффициент диффузии в твердых телах крайне чувствителен к дефектам кристаллической решетки, возникающим при нагреве, напряжениях, деформациях и других воздействиях. Увеличение числа дефектов, главным образом вакансий, облегчает перемещение атомов в твердом теле и приводит к росту диффузии. Для твердых тел характерна экспоненциальная коэффициента диффузии 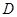 от температуры
от температуры 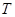 . Например, коэффициент диффузии цинка в медь при повышении температуры от
. Например, коэффициент диффузии цинка в медь при повышении температуры от 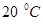 до
до 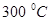 возрастает в
возрастает в 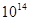 раз.
раз.
 2015-06-26
2015-06-26 3963
3963