Гетерофункциональные соединения, молекулы которых содержат одновременно амино- и карбоксильную группы, называются аминокислотами (а/к). Общее число, встречающихся в природе аминокислот, достигает 100. При этом в организме человека их найдено около 70, из которых > 20 входят в состав белков. Ф.Крик назвал их “магической двадцаткой”. Только они шифруются генетическим кодом. Эти вещества относятся к a-аминокислотам (a, потому что NH2 - расположена у a-С атома по рациональной номенклатуре) и называются протеиногенными (Приложение 1):
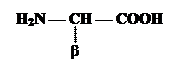
Существуют различные классификации аминокислот, входящих в состав белков, в зависимости от признака, положенного в основу их деления. По химической природе боковой цепи выделяют алифатические (ациклические), ароматические, гетероциклические. По количеству функциональных групп: моноаминомонокарбоновые, диаминомонокарбоновые, моноаминодикарбоновые, диаминодикарбоновые. От наличия иных функциональных групп в радикале различают: включающие гидрокси- (окси)аминокислоты, амидо-, серо- и иминосодержащие. В зависимостиот вариантов происхождения аминокислоты бывают незаменимые, не способные синтезироваться в организме, отсюда должны поступать с пищей (вал, лей, иле, лиз, тре, мет, фен, три) и заменимые – которые могут и содержаться в продуктах питания, и образовываться при необходимости в клетках. При некоторых, чаще всего наследственных заболеваниях, перечень незаменимых кислот расширяется. Так при фенилкетонурии нарушены реакции, с помощью которых создаётся тирозин (отсюда – условнозаменимые а/к).
По отношению к воде (растворимости их радикалов) подразделяются на:
По степени ионизации их можно рассматривать как кислые, основные и нейтральные. В организме все полярные радикалы гидрофильных кислот находятся в диссоциированном состоянии, что обеспечивает им заряд. Он обусловлен соотношением кислотных и основных центров в молекуле. Если преобладают первые (асп, глу) – заряд будет отрицательным; если - основные (арг, лиз, гис) – положительным. В формировании данного параметра важную роль играет рН среды, в которой соединение растворено. В нейтральной среде аминокислоты, содержащие дополнительную карбоксильную группу, имеют суммарный отрицательный заряд и называются кислыми:
 2015-06-26
2015-06-26 760
760








