Это генетически запрограммированная последовательность a-аминокислот L-ряда в полипептидной цепи. Она имеет зигзагообразное конформационное строение:
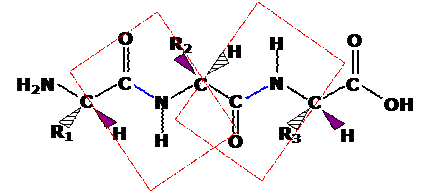
Стабилизируется с помощью пептидных связей.
Каждый белок организма имеет уникальную последовательность аминокислот.
Биороль данной структуры: специфические особенности чередования различных по строению а/к обусловливают индивидуализацию формирования пространственных структур (вторичной, третичной и четвертичной), а следовательно и свойства, и функции получившегося протеина.
Варианты вторичной структуры белка
Данный уровень образуется благодаря вращению пептидных групп относительно друг друга или появлению в полипептидной цепи одноимённо заряженных либо крупных радикалов, пролина.
 Различают a-спираль и β-складчатый слой. Радикалы этих структур, как гидрофобные, так и гидрофильные, направлены перпендикулярно цепи, имея наиболее выгодное расположение заместителей - транс-конформацию, поэтому белки, обладающие лишь вторичной структурой, плохо растворимы в воде.
Различают a-спираль и β-складчатый слой. Радикалы этих структур, как гидрофобные, так и гидрофильные, направлены перпендикулярно цепи, имея наиболее выгодное расположение заместителей - транс-конформацию, поэтому белки, обладающие лишь вторичной структурой, плохо растворимы в воде.
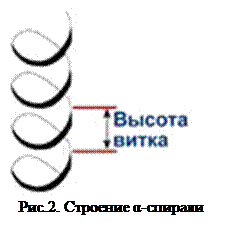
Правозакрученная α-спираль (Рис.2) содержит 3,6 аминокислотных остатка в одном витке; это создает возможность для взаимодействия карбонильного атома кислорода одной пептидной группы с атомом водорода аминогруппы соседнего витка. В результате возникают многочисленные водородные связи, которые стабилизируют данную структуру.
β-структура представляет складчатый слой, образованный одной или несколькими полипептидными цепями, располагающимися параллельно или антипараллельно (Рис.3).
Эта пространственная организация молекулы похожа на «вытянутую» спираль, где радикалы аминокислот препятствуют спирализации и увеличивают расстояние между витками (одноименно заряженные или крупные радикалы).
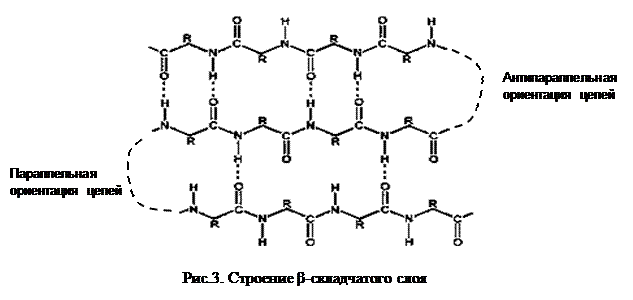
Оба варианта стабилизируются за счёт водородных связей, а β-складчатый слой может и с помощью дисульфидных мостиков.
Биороль данной структуры: отвечает за формирование третичной структуры и свойства белка.
 2015-06-26
2015-06-26 1128
1128
