|

|





|
Уравнение Гиббса не описывает всю экспериментально полученную изотерму адсорбции.
Основные положения теории Ленгмюра
1. Адсорбция идет на активных центрах. В энергетическом отношении все активные центры одинаковы (имеет место равномерное распределение энергии по поверхности раствора).
2. Адсорбция идет под действием сил Ван-дер-Ваальса. На малых расстояниях эти силы очень интенсивны и характеризуются малым радиусом действия. Поэтому только одна частица (молекула) может зафиксироваться на поверхности.
3. Каждый центр работает автономно.
4. Отсутствует миграция адсорбированных частиц вдоль поверхности раздела.
5. В системе устанавливается динамическое равновесие, когда число адсорбирующихся частиц равно числу частиц, покидающих поверхностный слой (при равновесии скорость адсорбции равна скорости десорбции).
Для описания изотермы адсорбции Ленгмюром предложено уравнение.
Рассмотрим поверхность раздела жидкость-газ площадью 1 м2.
Пусть Q – площадь поверхности, занятая молекулами ПАВ;
(1- Q) – свободная площадь;
n а – число адсорбирующихся в единицу времени частиц (молекул);
n д – число десорбирующихся частиц.
При равновесии скорость адсорбции равна скорости десорбции, т.е.
n а = n д.
Скорость адсорбции пропорциональна доле свободной площади поверхностного слоя и концентрации ПАВ в растворе
n а = k а с (1- Q),
скорость десорбции зависит только от доли площади поверхности, заполненной молекулами ПАВ:
n д = k д Q.
Тогда
k а с (1- Q) = k д Q.
Решаем относительно Q:
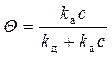 .
.
Разделим числитель и знаменатель на k д:
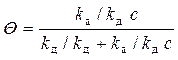 ,
,
k а/ k д = k – константа адсорбционно-десорбционного равновесия,
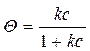 . (1)
. (1)
Установим связь между Q, Г и Г max.
Площадь поверхностного слоя, заполненную молекулами ПАВ, можно найти как произведение площади, занимаемой одной молекулой ПАВ S 0, на количество молекул в поверхностном слое N = n Na, где n – количество вещества в поверхностном слое, Na – число Авогадро, Na = 6,02×1023 моль-1.
Количество вещества, отнесенное к единице площади поверхностного слоя, есть адсорбция Г данного вещества. Поскольку при выводе уравнения рассматривается поверхностный слой площадью 1 м2, n = Г. При насыщении поверхностного слоя молекулами ПАВ Q = 1 м2n = Г max.
Тогда
S 0 Г Na = Q,
S 0 Г max Na = 1,
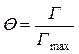 .
.
Подставим в уравнение (1):
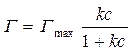 . (2)
. (2)
Уравнение (2) – уравнение Ленгмюра, описывающее изотерму адсорбции ПАВ. Уравнение Ленгмюра было выведено для адсорбции газа на твердой поверхности, но оно применимо и для описания адсорбции на границе раздела раствор ПАВ-воздух. Более того, именно для границы твердое тело-газ, для которой оно было выведено, чаще наблюдаются различного рода отклонения от ленгмюровской изотермы адсорбции.
1) при очень маленьких концентрациях ПАВ kc << 1, уравнение Ленгмюра принимает вид уравнения прямой и описывает прямолинейный участок изотермы адсорбции (до перегиба)
Г = Г max kc;
2) при больших концентрациях kc >> 1 и Г = Г max – горизонтальный участок изотермы адсорбции.
Таким образом, в отличие от уравнения Гиббса, уравнение Ленгмюра описывает всю изотерму адсорбции.
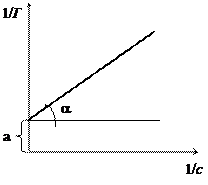 Строят график в координатах
Строят график в координатах
1/ Г = f(1/ с) (рис.). По графику определяют свободный член а и угловой коэффициент b (тангенс угла наклона tg a), по которым находят значения Г max и k.
Для нахождения констант уравнения Ленгмюра Г max и k его приводят к линейному виду. После линеаризации
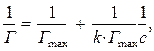
где у = 1/Г, х = 1/С, 1/ Г max = a (свободный член), 1/ k Г max = b (угловой коэффициент)
Зная предельную адсорбцию Г max, можно рассчитать длину молекулы ПАВ l и площадь, занимаемую одной молекулой в поверхностном слое S 0.
На поверхности раздела фаз площадью 1 м2 находится Г max Nа молекул поверхностно-активного вещества В состоянии плотнейшей упаковки, соответствующем насыщенному поверхностному слою, эти частицы занимают площадь Г max× Nа × S 0 = 1 Поэтому
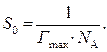
Объем насыщенного поверхностного слоя, соответствующий площади 1 м2, равен, с одной стороны, Г max× М /r и 1× l – с другой. Последнее утверждение правильно, если принять, что толщина поверхностной зоны равна длине молекулы l. В этом случае выполняется равенство
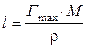 ,
,
где М – молярная масса ПАВ;
r – плотность поверхностно-активного вещества.
 2015-02-27
2015-02-27 1351
1351
