Первая стадия процесса взаимодействия металла с коррозионной средой – хемосорбция окислителя (O2,CO2,H2O,SO2) на поверхности металла,например:
Me(тв) + {O2} = Me(тв) + 2Oадс
При наличии химического сродства между металлом и окислителем реализуется вторая стадия взаимодействия металла с коррозионной средой – переход хемосорби-рованной пленки в оксидную. Этот процесс может быть условно описан реакцией вида:
XMe(тв) + yOадс = MexOy
Образующаяся на поверхности металла оксидная пленка может замедлять процесс коррозии, вследствие торможения подвода окислителя к поверхности окисляющегося металла.
В этом случае пленка обладает защитными свойствами.
Сплошность пленки, образующейся на поверхности металла, можно оценить по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла (α - фактор Пиллинга—Бэдворса). 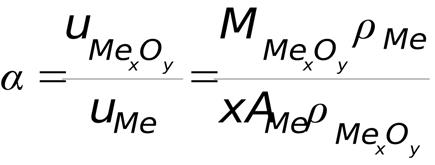
М – молекулярная масса
ρ – плотность
А – атомная масса
Х – число атомов металла в молекуле оксида
Металлы, у которых α<1, не могут создавать сплошные оксидные слои, и через несплошности в слое (трещины) кислород свободно проникает к поверхности металла.
Сплошные и устойчивые оксидные слои образуются при α = 1,2—1,6, но при больших значениях α пленки получаются не сплошные, легко отделяющиеся от поверхности металла (железная окалина) в результате возникающих внутренних напряжений.
 2015-07-04
2015-07-04 1257
1257








