А. Похідні піролу
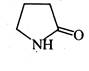 Піролідон-2 є лактамом α-аміномасляної кислоти. У промисловості добувають взаємодією бутиролактону з аміаком.
Піролідон-2 є лактамом α-аміномасляної кислоти. У промисловості добувають взаємодією бутиролактону з аміаком.
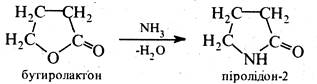
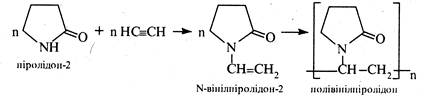
При конденсації піролідону-2 з ацетиленом утворюється N-вінілпіролідон-2, який легко полімеризується, утворюючи полівінілпіролідон (ПВП).
Низькомолекулярний ПВП (молекулярна маса 12-13 тис.) утворює колоїдні розчини у воді та застосовується для приготування кровозамінника «Гемодезу», середньомолекулярний ПВП (м. м. 35-40 тис.) використовують у фармацевтичній промисловості як зв'язуючий засіб у виробництві таблеток.
При сополімеризації вінілпіролідону, акриламіду та етилакрилату добувають біорозчинний полімер для очних лікарських плівок, який забезпечує тривалу дію лікарських речовин (пролонгуючий ефект).
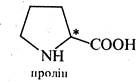
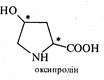 Пролін (2-піролідинкарбонова кислота) і оксипролін (4-гідрокси-2-піролідинкарбонова кислота) — це α-амінокислоти гетероциклічного, ряду, в яких спільний α-амінокислотний фрагмент— NH—СН(—СООН)— включений до складу піролідинового циклу. Пролін має один асиметричний атом вуглецю і тому існує у вигляді двох оптично активних ізомерів і одного рацемату. Оксипролін містить два хіральні центри та через це може існувати у вигляді двох пар енантіомерів і двох рацематів. L-Пролін і L-оксипролін входять до складу білків. Особливо багатий ними колаген.
Пролін (2-піролідинкарбонова кислота) і оксипролін (4-гідрокси-2-піролідинкарбонова кислота) — це α-амінокислоти гетероциклічного, ряду, в яких спільний α-амінокислотний фрагмент— NH—СН(—СООН)— включений до складу піролідинового циклу. Пролін має один асиметричний атом вуглецю і тому існує у вигляді двох оптично активних ізомерів і одного рацемату. Оксипролін містить два хіральні центри та через це може існувати у вигляді двох пар енантіомерів і двох рацематів. L-Пролін і L-оксипролін входять до складу білків. Особливо багатий ними колаген.
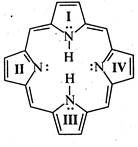 Порфін — кристалічна речовина темно-червоного кольору. За хімічною структурою являє собою макроциклічну спряжену систему, котра складається з пірольного (III), піролінового (І) та двох ізопірольних (II, IV) ядер, зв'язаних між собою метановими групами =СН —. Порфін є ароматичною сполукою. Він має площинну будову молекули, містить замкнену спряжену систему з кількістю π-електронів, яка дорівнює 26 (11 π-зв'язків і дві пари неподілених електронів при азоті), що відповідає правилу Хюккеля (4n+2 при n=6). Похідні порфіну дістали загальну назву порфірини. У вигляді комплексів з металами порфірини входять до складу таких важливих природних сполук, як гемоглобін і хлорофіл.
Порфін — кристалічна речовина темно-червоного кольору. За хімічною структурою являє собою макроциклічну спряжену систему, котра складається з пірольного (III), піролінового (І) та двох ізопірольних (II, IV) ядер, зв'язаних між собою метановими групами =СН —. Порфін є ароматичною сполукою. Він має площинну будову молекули, містить замкнену спряжену систему з кількістю π-електронів, яка дорівнює 26 (11 π-зв'язків і дві пари неподілених електронів при азоті), що відповідає правилу Хюккеля (4n+2 при n=6). Похідні порфіну дістали загальну назву порфірини. У вигляді комплексів з металами порфірини входять до складу таких важливих природних сполук, як гемоглобін і хлорофіл.
Гемоглобін — це красильна речовина крові, що міститься в ерітроцитах. Він являє собою складний білок - хромопротеїд, який складається з білка глобіну та забарвленої на червоний колір небілкової частини — гему. За хімічною структурою гем є комплексом порфірину з Fe (II). При кислотному гідролізі гемоглобіну вільний гем легко окислюється на повітрі з утворенням геміну, котрий має ту саму структуру, що і гем, але містить Fe (III).
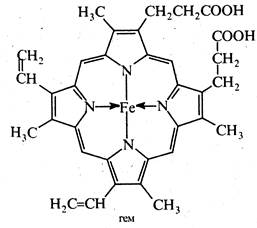
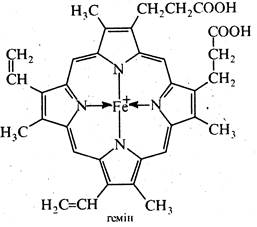
Будову геміну встановив у 1929 р. Г.Фішер і в тому ж році він здійснив синтез геміну.
Гем, координаційно сполучений з глобіном (за рахунок координаційного зв'язку між Fe2+ та імідазольним фрагментом гістидину білкової молекули) утворює гемоглобін.
Гемоглобін в організмі виконує роль перенощика кисню з легенів у тканини. При цьому, молекула кисню зворотньо реагує з гемоглобіном з утворенням оксигемоглобіну згідно зі схемою:
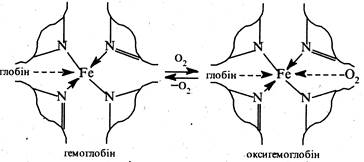
Деякі речовини, зокрема, оксид вуглецю (II) та солі синильної кислоти, утворюють з гемоглобіном стабільніші комплекси, ніж кисень, і тим самим блокують дію гемоглобіну. Такі сполуки відносять до дихальних отрут.
Частково гідрований порфіновий цикл, координаційно зв'язаний з магнієм, входить до складу зеленого пігменту рослин — хлорофілу. З рослин виділено хлорофіл α та хлорофіл β.
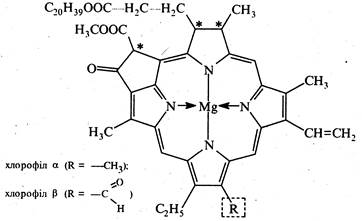
Хлорофіли містять три асиметричні атоми вуглецю та через це виявляють оптичну активність. Синтез хлорофілів було вперше здійснено у 1960 р. Р.Вудвордом. Хлорофіли виконують важливу роль у процесі фотосинтезу, перетворюючи світлову енергію сонячного випромінювання на енергію хімічних зв'язків.
Вітамін В12 (ціанокобаламін). Вітамін В12 було вперше виділено з печінки теплокровних тварин американським хіміком К.Фолкерсом у 1948 р. Проте, тільки в 1956 р. англійський хімік Д.Кроуфут-Ходжкін встановила за допомогою рентгеноструктурного аналізу його будову. В основі структури вітаміну В12 лежить макроцикл, що складається з чотирьох частково гідрованих пірольних ядер, у якому атоми азоту утворюють координаційний комплекс з атомом кобальту та ціанід-іоном:
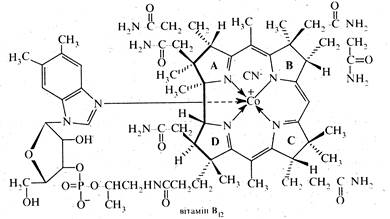
Зважаючи на наявність ціаногрупи, зв'язаної з кобальтом, вітамін B12 називають також ціанокобаламіном.
За теперішнього часу вітамін В12 добувають у промисловому масштабі мікробіологічно. Він застосовується у медичній практиці для лікування анемій, захворювань нервової системи та печінки.
Б. Похідні фурану
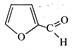 Найважливішим похідним фурану є фурфурол (2-фуранкарб-альдегід) - безбарвна або трохи жовтувата масляниста рідина (т. кип. 162 °С), яка має приємний запах свіжовипеченого житнього хліба. Вперше його було виділено з висівків. Від лат. furfur «висівки» він і дістав свою назву. В промисловості фурфурол добувають у великих кількостях кислотним гідролізом полісахаридів пентозанів, які містяться в сільськогосподарських відходах (соломі, луззі соняшників, кукурудзяних качанах, бавовняних коробочках та ін.)
Найважливішим похідним фурану є фурфурол (2-фуранкарб-альдегід) - безбарвна або трохи жовтувата масляниста рідина (т. кип. 162 °С), яка має приємний запах свіжовипеченого житнього хліба. Вперше його було виділено з висівків. Від лат. furfur «висівки» він і дістав свою назву. В промисловості фурфурол добувають у великих кількостях кислотним гідролізом полісахаридів пентозанів, які містяться в сільськогосподарських відходах (соломі, луззі соняшників, кукурудзяних качанах, бавовняних коробочках та ін.)
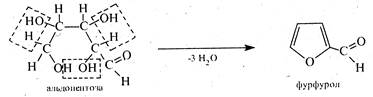
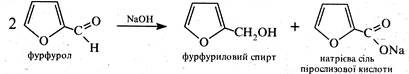
За хімічними властивостями фурфурол багато в чому схожий з ароматичними альдегідами, зокрема, з бензальдегідом. Як ароматичний альдегід фурфурол вступає в реакцію Канніццаро:
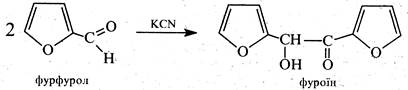
З ціанідом калію зазнає конденсації типу бензоїнової:
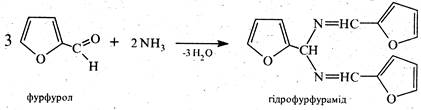
З аміаком утворює гідрофурфурамід (аналог гідробензаміду):
Фурфурол, як альдегід, окислюється аміачним розчином оксиду срібла, утворюючи пірослизову кислоту, відновлюється у фурфуриловий спирт, приєднує гідросульфіт натрію, з гідроксиламіном утворює оксим, а з фенілгідразином— фенілгідразон та ін.
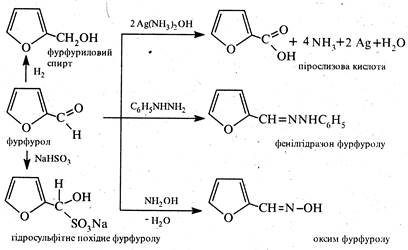
Крім реакцій по альдегідній групі, для фурфуролу характерні реакції по фурановому ядру. Фурфурол легко вступає в реакції SE, при цьому найбільш реакційноздатне положення 5. Внаслідок електроно-акцепторного впливу альдегідної групи, що приводить до зменшення електронної густини на вуглецевих атомах фуранового циклу, фурфурол менш ацидофобний, ніж фуран.
Нітрування фурфуролу проводять концентрованою азотною кислотою в середовищі оцтового ангідриду. В процесі реакції добувають 5-нітрофурфуролдіацетат, який при гідролізі у присутності розведеної H2SO4 утворює 5-нітрофурфурол,
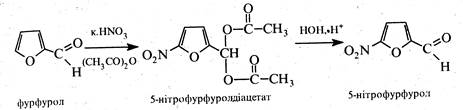
5-Нітрофурфурол є вихідною речовиною для синтезу ряду лікарських препаратів. Так, при взаємодії 5-нітрофурфуролу з семікарбазидом утворюється семікарбазон 5-нітрофурфуролу, котрий застосовується у медицині під назвою фурацилін.
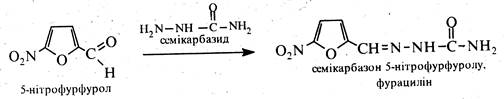
Представниками групи лікарських препаратів нітрофуранового ряду є також фурадонін і фуразолідон.
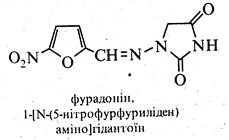
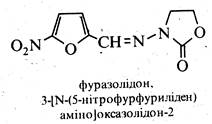
Препарати нітрофуранового ряду виявляють високу антибактеріальну активність. Вони знаходять широке застосування у медицині для лікування гнійних і запальних процесів. Особливо цінною властивістю цих препаратів є їх здатність у ряді випадків виявляти ефект проти форм, стійких до сульфаніламідів і антибіотиків.
В. Похідні тіофену
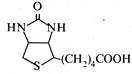 Біотин (вітамін Н). Гетероциклічна частина молекули біотину складається з повністю гідрованих тіофенового та імідазольного кілець, а боковий ланцюг представлений залишком валеріанової кислоти. Біотин вперше виділено у 1935 р. з яєчного жовтка, при цьому для добування 1 мг речовини було потрібно 225 кг сухого яєчного жовтка. Особливо багаті на біотин нирки, печінка, горіх, боби, картопля. Біотин входить до складу активного центру ферментів, які беруть участь у синтезі вищих жирних кислот, білків, нуклеїнових кислот та ін. При нестачі біотину в організмі розвиваються запальні захворювання шкіри (дерматити), що супроводжуються випаданням волосся та ураженням нігтів.
Біотин (вітамін Н). Гетероциклічна частина молекули біотину складається з повністю гідрованих тіофенового та імідазольного кілець, а боковий ланцюг представлений залишком валеріанової кислоти. Біотин вперше виділено у 1935 р. з яєчного жовтка, при цьому для добування 1 мг речовини було потрібно 225 кг сухого яєчного жовтка. Особливо багаті на біотин нирки, печінка, горіх, боби, картопля. Біотин входить до складу активного центру ферментів, які беруть участь у синтезі вищих жирних кислот, білків, нуклеїнових кислот та ін. При нестачі біотину в організмі розвиваються запальні захворювання шкіри (дерматити), що супроводжуються випаданням волосся та ураженням нігтів.
ІНДОЛ
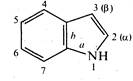 Молекула індолу (бензо[b]піролу) являє собою конденсовану гетероциклічну систему, що складається з пірольного та бензольного кілець. Нумерацію атомів у індолі починають з гетероатома, атоми вуглецю у пірольному циклі позначають також літерами α та β.
Молекула індолу (бензо[b]піролу) являє собою конденсовану гетероциклічну систему, що складається з пірольного та бензольного кілець. Нумерацію атомів у індолі починають з гетероатома, атоми вуглецю у пірольному циклі позначають також літерами α та β.
 2015-07-14
2015-07-14 3972
3972








