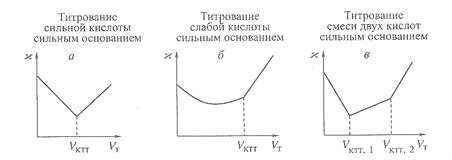
Точку эквивалентности определяют по резкому излому кривой зависимости электропроводности от объема титранта. При этом могут быть использованы все типы реакций (нейтрализации, осаждения, комплексообразования), при которых достаточно резко изменяется электропроводность. Три примера кривых титрования приведены на рисунке 26
|
|
|
рис.26
Чтобы объяснить первую кривую, обратимся к реакции
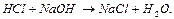
При добавлении в ячейку NaOH подвижные ионы Н+ связываются с гидроксил-ионами и заменяются на менее подвижные ионы Na+. Поэтому электропроводность ячейки снижается и в критической точке титрования (VKTT) она минимальна. Далее при добавлении избыточных количеств ионов Na+ и OH-, которые уже ни с чем не связываются и ничего не замещают, а просто накапливаются в ячейке, электропроводность снова повышается.
При титровании слабого электролита (рис.26, б) небольшой подъём 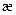 наблюдается задолго до VКТТ – из-за того, что увеличивается степень диссоциации электролита. Но после VКТТ проводимость начинает увеличиваться гораздо быстрей.
наблюдается задолго до VКТТ – из-за того, что увеличивается степень диссоциации электролита. Но после VКТТ проводимость начинает увеличиваться гораздо быстрей.
Для получения резкого излома на кривой титрования следует учитывать эффект разбавления. Его сводят к минимуму, титрованием больших объемов (100 см3) исследуемого вещества концентрированным раствором титранта из микробюретки (2 – 5 см3). Для получения надежных результатов следует учитывать различные факторы, влияющие на электропроводность (константа диссоциации, подвижность ионов, ионная сила раствора и т. д.). При правильном подборе титранта и растворителя создают благоприятные условия кондуктометрического титрования.
Достоинства: возможность раздельного определения смесей кислот и оснований, титрование мутных и окрашенных растворов при точности 2 %.
 2015-07-14
2015-07-14 1002
1002








