 Поверхностными называют физико-химические процессы самопроизвольного накопления (концентрирования) веществ на границе раздела фаз, вызванные особенностями состава и строения поверхностного (граничного) слоя. При соприкосновении газов и жидкостей, газов и твердых тел, двух несмешивающихся жидкостей, жидкостей и твердых тел на границе раздела всегда формируется поверхностный слой атомов, молекул или ионов, который, согласно Гиббсу, представляет собой промежуточную фазу (рис. 2.1). Толщина этого слоя невелика и составляет один (моно-) или несколько (полимолекулярный слой) молекулярных диаметров. Поверхностный слой резко отличается по физико-химическим характеристикам (удельной энергии, плотности, вязкости, электрической проводимости и т.п.) от свойств фазы в глубине объема. Отличия связаны с иной ориентацией молекул в поверхностном слое и иным энергетическим состоянием их в сравнении с молекулами внутри фазы. Кроме того, в многокомпонентных системах (растворах) состав поверхностного слоя зачастую не совпадает с составом фазы в объеме. Особенности поверхностного слоя обусловлены наличием у формирующих его молекул (как правило, более плотной фазы – жидкости или твердого тела) избытка поверхностной энергии, что приводит к концентрированию на такой поверхности молекул растворенного вещества или менее плотной фазы (жидкости или газа).
Поверхностными называют физико-химические процессы самопроизвольного накопления (концентрирования) веществ на границе раздела фаз, вызванные особенностями состава и строения поверхностного (граничного) слоя. При соприкосновении газов и жидкостей, газов и твердых тел, двух несмешивающихся жидкостей, жидкостей и твердых тел на границе раздела всегда формируется поверхностный слой атомов, молекул или ионов, который, согласно Гиббсу, представляет собой промежуточную фазу (рис. 2.1). Толщина этого слоя невелика и составляет один (моно-) или несколько (полимолекулярный слой) молекулярных диаметров. Поверхностный слой резко отличается по физико-химическим характеристикам (удельной энергии, плотности, вязкости, электрической проводимости и т.п.) от свойств фазы в глубине объема. Отличия связаны с иной ориентацией молекул в поверхностном слое и иным энергетическим состоянием их в сравнении с молекулами внутри фазы. Кроме того, в многокомпонентных системах (растворах) состав поверхностного слоя зачастую не совпадает с составом фазы в объеме. Особенности поверхностного слоя обусловлены наличием у формирующих его молекул (как правило, более плотной фазы – жидкости или твердого тела) избытка поверхностной энергии, что приводит к концентрированию на такой поверхности молекул растворенного вещества или менее плотной фазы (жидкости или газа).
Живые организмы представляют системы с очень развитыми поверхностями раздела, к которым относятся кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны, мембраны ядер, митохондрий, лизосом и т.п. Поверхность кожи взрослого человека составляет примерно 1,5-1,6 м2, площадь поверхности капилляров печени – около 400 м2, поверхность эритроцитов всей крови – 2500-3800 м2, поверхность скелета – около 2 тыс. м2. Исследования показали, что пищевые вещества продуктов питания в большинстве своем поверхностно-активны и первым этапом их усвоения всегда является накопление их у стенок желудочно-кишечного тракта, а дальнейшее химическое превращение в клетке уже вторично. Многие физиологические процессы (дыхание, транспорт, экскреция и др.) протекают на поверхности биомембран и понимание механизмов их осуществления невозможно без знания основных закономерностей, которым подчиняются поверхностные явления.
Поверхностные явления широко распространены в природе. Там, где контактируют газы или пары, жидкости и твердые тела происходит накопление веществ на поверхности раздела. Почва хорошо поглощает (накапливает) не только растворенные в воде органические и минеральные вещества, но и воздух, углекислоту, пары воды, аммиак. Поглощение корнями питательных элементов из почвы начинается с накопления их на поверхности корневых волосков и тонких неопробковевших корней. Усвоение растениями углекислого газа при фотосинтезе возможно лишь после концентрирования диоксида углерода на внутренней поверхности листа.
Процессы накопления газов или растворенных веществ твердыми материалами или жидкостями могут протекать по разным механизмам и носят общее название сорбции. Принято различать четыре основных сорбционных явления: адсорбцию, абсорбцию, хемосорбцию и капиллярную конденсацию. К типично поверхностным процессам относится адсорбция. Адсорбция – это самопроизвольное концентрирование на твердой или жидкой поверхности раздела фаз вещества с меньшим поверхностным натяжением. Например, если внести в водную среду несколько капель масла, то масло не распределится равномерно во всем объеме жидкости, а сконцентрируется на поверхности водной среды. Вещество, которое адсорбируется, называется адсорбтивом или адсорбатом; вещество, на поверхности которого происходит адсорбция – адсорбентом. Адсорбция – обратимый процесс. Процесс, обратный адсорбции, называется десорбцией.
В зависимости от того, адсорбируются молекулы или ионы выделяют молекулярную и ионную адсорбцию. По характеру взаимодействия частиц адсорбента и адсорбтива адсорбция бывает физическая и химическая. Физическая адсорбция обусловлена проявлением остаточных ван-дер-ваальсовых сил, действующих на очень малых расстояниях. Ван-дер-ваальсово взаимодействие возможно при «согласованном» движении электронов подобно тому, как показано на
рис. 2.2. При таком движении у молекулы возникают наведенные диполи, а между молекулами появляются индукционные силы притяжения, называемые ван-дер-ваальсовой связью или межмолекулярным взаимодействием. Энергия такой связи намного (в сотни раз) меньше энергий ковалентных, ионных или металлических связей. Поэтому физическая адсорбция малоспецифична и обратима. Для нее свойственна низкая энергия адсорбции (ΔН от –4 до –40 кДж/моль), высокая скорость процесса, определяемая в основном скоростью диффузии
 |
адсорбтива с поверхности адсорбента.
При химической адсорбции, называемой хемосорбцией, происходит химическое взаимодействие адсорбента и адсорбтива, в котором задействованы адсорбционные силы химической природы (ионные, ковалентные, водородные связи). Химическая адсорбция ведет к образованию поверхностных соединений, когда поверхность адсорбента покрывается пленкой продукта реакции:
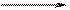 4 AI + 3 O2 2 AI2O3,
4 AI + 3 O2 2 AI2O3,
адсорбент адсорбтив
или соединений, в формировании которых участвует вся масса твердого тела:
 СаО + СО2 СаСО3.
СаО + СО2 СаСО3.
Энергия химической адсорбции находится в пределах от – 40 до – 400 кДж/моль, имеет порядок, близкий к порядку энергий химических реакций (200-800 кДж/моль), из-за чего химическая адсорбция, как правило, необратима.
Проявляющиеся при адсорбции сорбционные силы слагаются из совокупности параллельно действующих валентных химических и более слабых физических сил, вклад которых в каждом отдельном случае может быть различен и зависит, главным образом, от природы адсорбента и адсорбтива. Помимо естественных, существенное влияние на адсорбцию оказывают внешние факторы: концентрация и давление адсорбтива, температура среды. Увеличение концентрации вещества или давления газа усиливает адсорбцию. Повышение температуры понижает физическую адсорбцию, так как при этом усиливается скорость движения молекул в поверхностном слое и нарушается ориентация адсорбированных молекул, но увеличивает энергию адсорбируемых частиц, что, согласно теории активации молекул, повышает химическую адсорбцию.
Вещество может не только накапливаться на поверхности, но и поглощаться всем объемом адсорбента. Процесс поглощения газа или пара всем объемом адсорбента называется абсорбцией. Осуществляется абсорбция за счет диффузии молекул газа или пара в массу адсорбента и представляет, по существу, растворение одного вещества (адсорбтива) в другом (адсорбенте). Получение соляной кислоты в заводских условиях целиком основано на абсорбции газообразного хлористого водорода водой.
При капиллярной конденсации помимо поглощения происходит конденсация твердым пористым адсорбентом, например, активированным углем, паров и газов в порах-капиллярах. Она вызвана тем, что давление насыщенного пара над вогнутым мениском смачивающей стенки капилляров жидкости всегда меньше давления ее насыщенного пара над плоской поверхностью. В результате, в узких порах-капиллярах легко сжижаемые пары или газы конденсируются раньше, чем над плоской поверхностью.
В реальных условиях разделить процессы адсорбции, абсорбции, хемосорбции и капиллярной конденсации не представляется возможным. Обычно сочетается несколько сорбционных процессов. Исключение представляет адсорбция, которая иногда встречается в чистом виде. Абсорбция и хемосорбция почти всегда начинаются с адсорбции, т.е. с поверхностной концентрации вещества на границе раздела. Из всех сорбционных явлений для биологии и медицины наибольшее значение представляет адсорбция.
 2015-07-14
2015-07-14 2979
2979
