Найти степени окисления элементов в а) Cl2; б) S2F10; в) Cr2(SO4)3.
Решение.
а) Cl2 – это формула простого вещества, значит, согласно правилу 1., степень окисления атомов в нем равна нулю, Cl 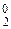 .
.
б) S 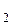 F
F 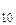 – это формула сложного вещества, степень окисления фтора в котором, согласно п. г) правила 1., равна −1, S
– это формула сложного вещества, степень окисления фтора в котором, согласно п. г) правила 1., равна −1, S 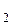 F
F 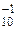 . Обозначим неизвестную степень окисления S буквой x, то есть S
. Обозначим неизвестную степень окисления S буквой x, то есть S 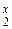 F
F 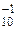 . Составим уравнение, на основании правила 4., учтя, что числа атомов S и F в молекуле S
. Составим уравнение, на основании правила 4., учтя, что числа атомов S и F в молекуле S 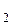 F
F 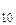 равны соответственно 2 и 10 (индексам в формуле молекулы):
равны соответственно 2 и 10 (индексам в формуле молекулы):
2∙ x + 10∙(-1) = 0.
Решая это уравнение, находим искомую степень окисления S:
x = +5.
в) Cr2(SO4)3 – это формула сложного вещества, степень окисления кислорода в котором, согласно п. в) правила 2., составляет −2, то есть Cr2(SO 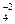 )3. Это вещество − соль (см. примечания к схеме 1), причем сульфат (соль серной кислоты Н2SО4), значит, степень окисления S, согласно правилу 3., равна +6, Cr2(S
)3. Это вещество − соль (см. примечания к схеме 1), причем сульфат (соль серной кислоты Н2SО4), значит, степень окисления S, согласно правилу 3., равна +6, Cr2(S 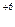 O
O 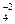 )3. Обозначим неизвестную степень окисления Cr буквой x, то есть Cr
)3. Обозначим неизвестную степень окисления Cr буквой x, то есть Cr 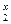 (S
(S 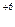 O
O 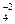 )3. Составим уравнение, на основании правила 4., учтя, что числа атомов Cr, S и O в формульной единице Cr2(SO4)3 равны соответственно 2 (индекс в формуле при символе Cr), 3 (индекс в формуле при формуле атомной группы SО4) и 3∙4 = 12 (произведение индексов при формуле атомной группы SО4 и при символе О):
)3. Составим уравнение, на основании правила 4., учтя, что числа атомов Cr, S и O в формульной единице Cr2(SO4)3 равны соответственно 2 (индекс в формуле при символе Cr), 3 (индекс в формуле при формуле атомной группы SО4) и 3∙4 = 12 (произведение индексов при формуле атомной группы SО4 и при символе О):
2∙ x + 3∙6 + 12∙(-2) = 0.
Решая это уравнение, находим искомую степень окисления Cr:
x = +3.
1. Уравнение окислительно-восстановительной реакции/реакции, не являющейся окислительно-восстановительной – это...
Решение.
Надо определить все степени окисления (см. ПРАВИЛА ОПРЕДЕЛЕНИЯ СТЕПЕНЕЙ ОКИСЛЕНИЯ) в предлагаемых уравнениях. Если степени окисления изменяются, то это уравнение окислительно-восстановительной реакции, а если не изменяются, то это уравнение реакции, не являющейся окислительно-восстановительной.
 2015-07-14
2015-07-14 368
368








