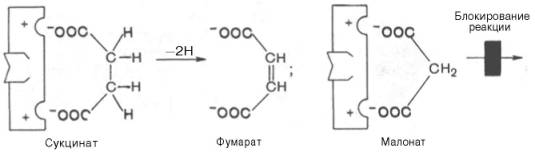
 - ингибитор присоединяется к ферменту не в активном центре.
- ингибитор присоединяется к ферменту не в активном центре.
Константа Кмих не меняется, но меняется скорость реакции.
Пример: тяжелые металлы, соли синильной кислоты, СО.
g) 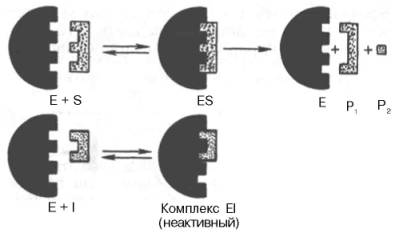 аллостерическое
аллостерическое
- отрицательный эффектор (ингибитор) присоединяется к аллостерическому центру фермента => изменяется 3 и 4 структура белка-фермента => взаимодействие субстрата с ферментом в активном центре становится невозможным.
 2015-08-13
2015-08-13 785
785








