
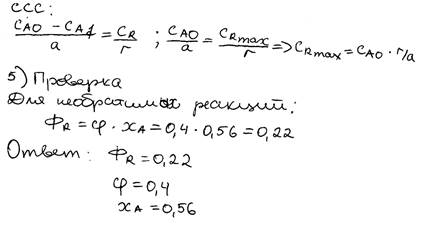
Скорость химической реакции и ее зависимость от концентрации реагирующих веществ и от температуры. Классификация химических реакций. Расчет скорости реакции при протекании параллельных и последовательных реакций.
Скорость химической реакции это количество реагента или продукта, которое исчезает или появляется вновь в единице объема за единицу времени. Она зависит: 1) от реакционной способности химических веществ, 2) концентрации, температуры и др., 3) подвижности компонентов, степени их перемешивания, 4) наличия катализатора.
W= -dCA/dτ
wrA=kCACB=kCA(CB0-CA0+CA)
Принципы химической кинетики.
Скорость химической реакции пропорциональна концентрациям исходных реагентов.
aA+bB→rR
W≈CaA * CbB
2) Принцип независимости протекания элементарных реакций;
3) Скорость реакции по одному из компонентов равна алгебраической сумме скоростей реакции, в которой участвует этот компонент.
Функциональная зависимость скорости химической реакции от концентраций компонентов реакционной смеси называется кинетическим уравнением.
Согласно закону действующих масс, число элементарных актов превращения будет пропорционально числу встреч частиц А и В.
W≈KCaA*CbB - элементарная реакция
W≈KCαA*CβB - неэлементарная реакция
Из кинетического уравнения следует, что скорость простой реакции пропорциональна концентрациям веществ, являющихся реагентами в данной реакции. Значит, для простых реакций увеличение концентрации исходных веществ практически всегда приводит к увеличению скорости (за исключением реакции нулевого порядка, скорость которых не зависит от концентрации).
Если реакция, описываемая уравнением aA+bB→rR+sS, характеризуется различающимися частными порядками по компонентам А и В, наибольшее влияние на скорость реакции будет оказывать изменение концентрации реагента, имеющего больший частный порядок.
Например, W≈KC2A*C0,25B
Увеличение концентрации реагента А в 2 раза вызовет рост скорости в 4 раза, а повышение В в 2 раза – лишь в 1,19 раз.
Как происходит реакция:
1) столкновение исходных молекул, соударение
2) не любое столкновение приводит к химической реакции
3) столкновение должно иметь достаточную энергию.
При увеличении температуры на 10 градусов скорость реакции возрастает в 2-4 раза.
Распределение Больцмана – доля молекул с энергией >Еа
exp(-Ea/RT)
Более строго зависимость скорости от температуры выражается уравнением Аррениуса: WrA≈Zexp(-Ea/RT)
Z-частота столкновений.
Энергия активации Еа – величина энергетического барьера для осуществления реакции (минимальный избыток энергии над средней внутренней энергией молекул, необходимый для того, чтобы произошло химическое взаимодействие).
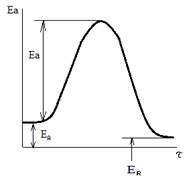
ЕА – средняя энергия компонента А.
Выводы:
lnK=lnK0-(Ea/R)*1/T
В силу неравномерности распределения температуры вдоль оси абсцисс химическая реакция более чувствительна к изменению температуры в области низких температур.
1) при различных значениях энергии активации
При изменении температуры от Т1=500К до Т2=600К скорость первой реакции
Е1=165кДж/кмоль Wr↑ в 820 раза, а второй
Е2=40кДж/кмоль Wr↑ в 5 раз
2) при постоянной энергии активации
Е1,2=165 кДж/кмоль
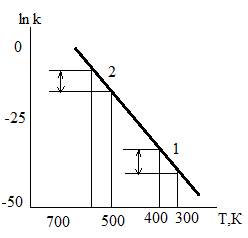
На прямой, соответствующей химической реакции с энергией активации 165 кДж/кмоль, выбраны два участка с разностью температур по 100К на в разных температурных интервалах: 1 участок-в области температур, близких к комнатной, 2 – в области более высоких температур (600К). Для участка 1 константа скорости за 100К увеличится в 1,9*107 раз, а для 2 участка за те же 100К константа увеличилась лишь в 820 раз.
В зависимости от того, какие признаки взяты за основу, существует несколько видов классификации химических реакций.
Классификация по механизму осуществления реакции:
- простые (одностадийные)
- сложные (многостадийные), в частности параллельные, последовательные и последовательно-параллельные.
Простыми называют реакции, для осуществления которых требуется преодоление лишь одного энергетического барьера (одна стадия).
Сложные реакции включают в себя несколько параллельных или последовательных стадий (простых реакций).
Простая реакция: aA+bB→rR
W≈CaA * CbB
Сложные реакции:
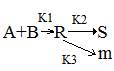
WrR= -K1*CA*CB+K2*CR+K3*CR
Классификация реакций по молекулярности учитывает, сколько молекул участвует в элементарном акте реакции: моно-, би- и тримолекулярные реакции.
По порядку реакции (сумма показателей степеней у концентраций реагентов в кинетическом уравнении): реакции первого, второго, третьего и дробного порядков.
По тепловому эффекту: экзотермические (выделение теплоты Q>0, энтальпия реакционной смеси ∆H<0) и эндотермические (Q<0, ∆H>0).
В зависимости (фазовый состав) от того, одну или несколько фаз образуют исходные реагенты и продукты реакции, химические реакции делятся на гомофазные и гетерофазные.
В зависимости от зоны протекания реакции делятся на гомогенные (реагенты и продукты находятся в одной фазе и реакция протекает в объеме этой фазы) и гетерогенные (один из реагентов или продуктов находится в фазовом состоянии, отличающемся от фазового состояния остальных участников, и при ее анализе обязательно должна учитываться поверхность раздела фаз).
Согласно закону действующих масс: скорость реакции пропорциональна произвольной концентрации исходных реагентов.
Правило составления кинетического уравнения.
1) для исходных реагентов знаку «+»
2) для продуктов реакции знаку «-»
Тогда для последовательных реакций:
A→(k1) R
R→(k2) S
wrR= -k1*CA+k2*CR
wrA=k1*CA
Для параллельных реакций:
A→(k1) R
A→(k2) S
wrA1=k1*CA
wrA2=k2*CA
wrA=(k1+k2)*CA
Для последовательно-параллельных:
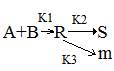
WrR= -k1*CA*CB+k2*CR+k3*CR
3) Паровая конверсия метана в производстве технологического газа для синтеза аммиака. Физико-химические особенности процесса. Выбор технологического режима, аппаратурное оформление.
Химическая схема производства HNO3.
I Получение азотно-водородной смеси.
1) очистка СН4 от сернистых соединений.
2) Паровая конверсия.
CH4+H2O↔3H2+CO-Q
3) Кислородная конверсия
СH4+0,5O2↔2H2+CO-Q
4) конверсия СО
CO+H2O↔H2+CO2+Q
5) Очистка конвертированного газа.
II Синтез NH3.
III Получение HNO3.
Принципиальная схема получения азотоводородной смеси.
1) трубчатая печь.
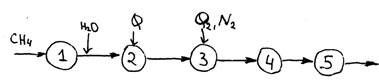
1 – очистка СН4
2 – трубчатая печь, паровая конверсия
3 – кислородная конверсия
4 – конверсия СО
5 – очистка СО и СО2
Синтез-газ - состоит из СО и Н2. Получают конверсией природного горючего газа с водным паром и О2, а также газификацией топлив. Сырье в производстве углеводородов, метилового спирта и др.
Синтез-газ из углеводородных газов является основным источником получения аммиака и метанола.
Конверсия газов - переработка газов с целью изменения состава исходной газовой смеси.
Паровая конверсия метана при получении синтез-газа протекает по следующей реакции:
CH4+H2O↔3H2+CO-Q - реакция обратимая, эндотермическая, идет с увеличением числа молей газообразных веществ (∆V>0).
Равновесный состав газовой смеси определяется температурой и давлением в системе, а также соотношением реагирующих компонентов.
При атмосферном давлении и стехиометрическом соотношении исходных компонентов достаточно полная конверсия метана достигается при температуре примерно 800ᵒС. С увеличением расхода водяного пара такой же степени разложения метана можно достичь при более низких температурах. Применение давления существенно снижает полноту конверсии.
Для смещения равновесия вправо: Т↑ (900ᵒС), Р↓ (Р=3-4 МПа), увеличить избыток водяных паров, Н2О:СН4=2:1. Тогда степень превращения составит хА=0,9.
Также для интенсификации процесса можно использовать катализатор – Ni (Al2O3).
Для достижения остаточного содержания СН4 примерно 0,5% конверсию ведут в две стадии: паровая конверсия под давлением и паровоздушная конверсия с использованием кислорода воздуха.
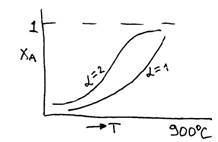
α=υH2O/υстехиом.Н2О
При 900ᵒС степень превращения 99,5%.
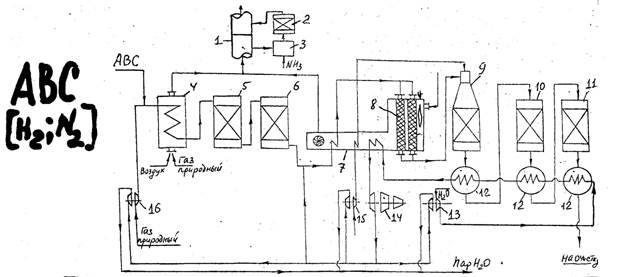
Природный газ сжимают в компрессоре 16, смешивают с азотоводородной смесью и подают в подогреватель 4, где реакционная смесь нагревается до 370-400ᵒС. Далее нагретый газ подвергают очистке от сернистых соединений: в реаторе 5, а затем в адсорбере 6 сероводород поглощается сорбентом. Очищенный газ смешивается с водяным паром и полученная парогазовая смесь поступает в конвекционную зону трубчатой печи 8. В радиационной камере печи размещены реакционные трубы, заполненные катализатором конверсии метана, и горелки, в которых сжигается природный или горючий газ (паровая конверсия метана, I ступень). Парогазовая смесь нагревается в подогревателе 7 и затем под давлением распределяется сверху вниз по большому числу труб, заполненных катализатором. В трубчатой печи 8 выделяется большое количество тепла, и это тепло расходуется на подогрев в реакторе 9, где происходит паровоздушная конверсия. Температура на выходе 800-900ᵒС. При этой температуре газ направляется в котел-утилизатор12, вырабатывающий пар. Здесь реакционная смесь охлаждается до 500ᵒС и идет в конвертор СО I ступени10, где на железохромовом катализаторе протекает конверсия основного количества оксида углерода водяным паром. Выходящая из реактора газовая смесь поступает в паровой котел 12, где охлаждается до 220ᵒС и подается в конвертор СО II ступени 11, заполненный низкотемпературным катализатором, где содержание СО снижается до 0,5%. После охлаждения конвертированный газ при температуре окр. среды поступает на очистку.
Из 13 насоса вода поступает в 12 холодильник, вода испаряется, получаем пар низкого давления. Затем пар идет в следующий 12 холодильник (400-500ᵒС). Получаем пар среднего давления и затем в последний 12 холодильник, получаем пар высокого давления. Пар поступает в трубчатую печь 7, перегревается и идет на 14 турбину. На ней вырабатывается электроэнергия. Пар теряет свои свойства и становится паром среднего давления. Идет в 15 и 16 турбины и приводит в действие насосы.
Таким образом, паровая конверсия проводится в трубчатом реакторе №8.
Смесь нагревается в 7 аппарате, добавляются водяные пары, и идет реакция.
Трубчатая печь:
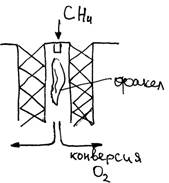
Факел большой. Теплопередача идет за счет радиации (900-1000ᵒС).
1,2,3 аппараты – для очистки.
 2015-08-13
2015-08-13 1802
1802
